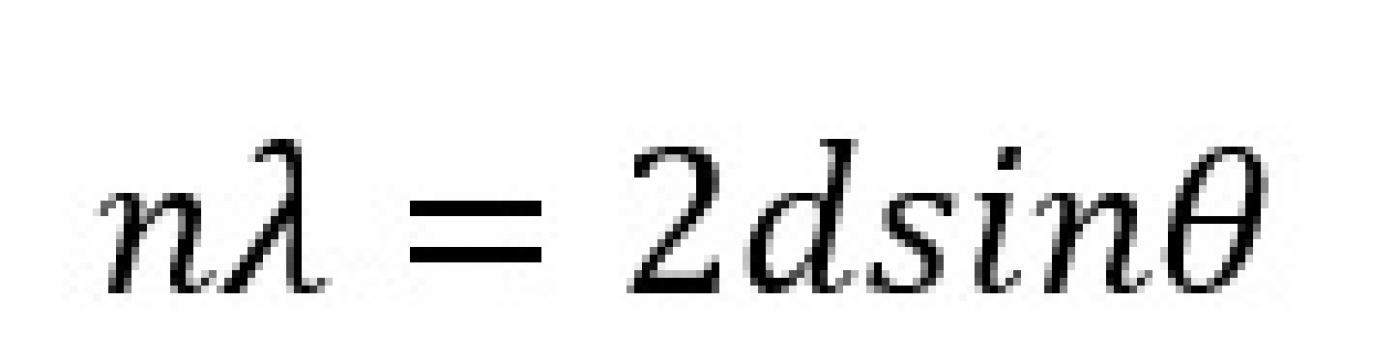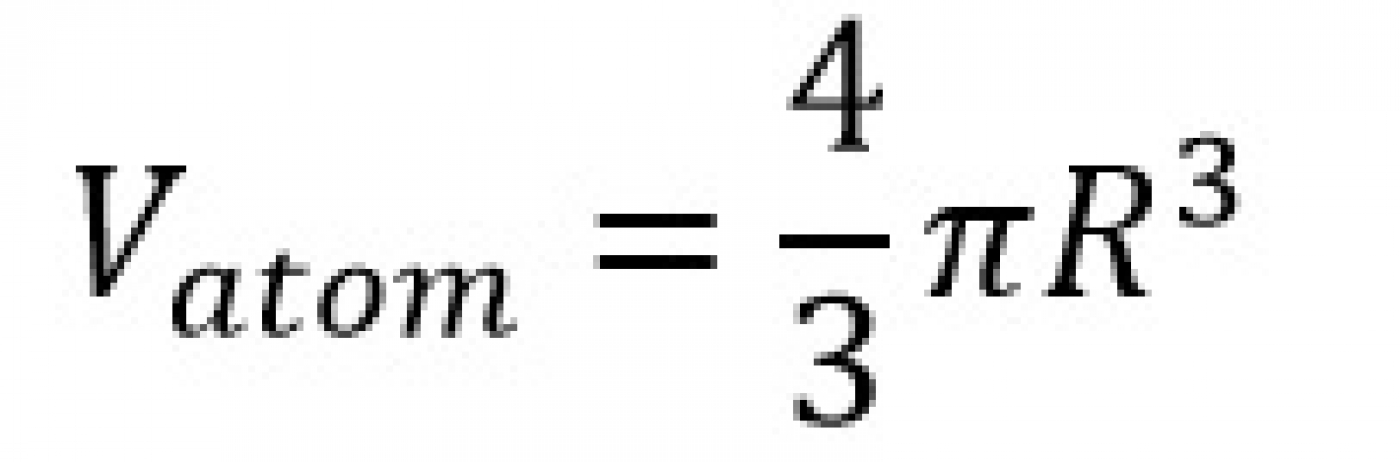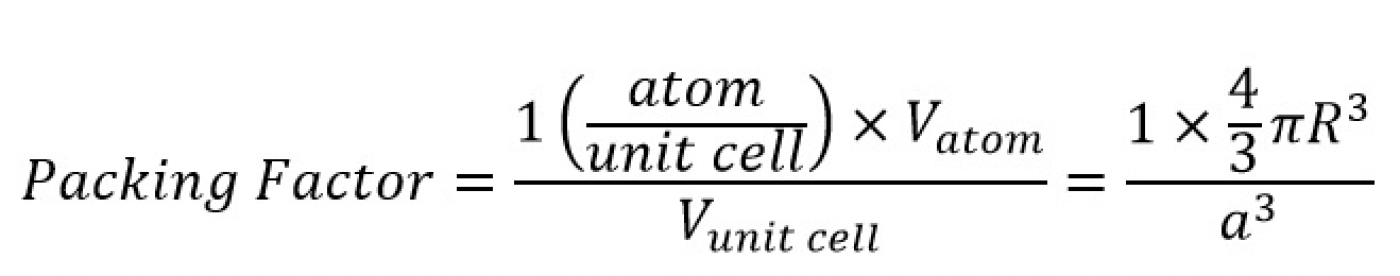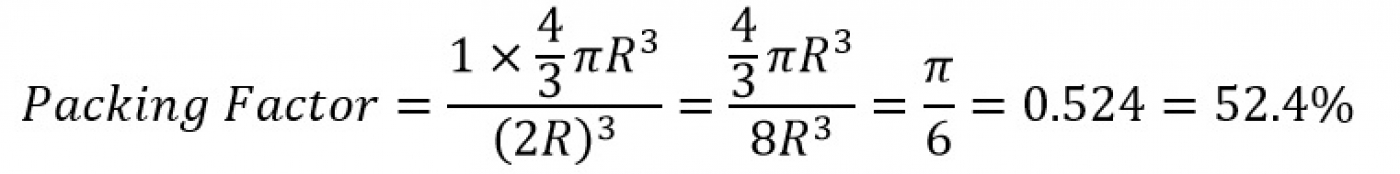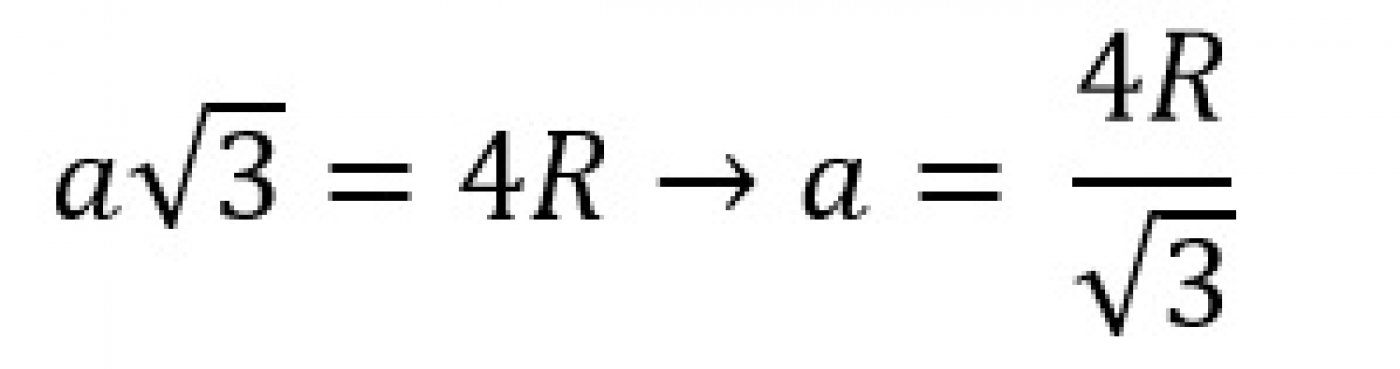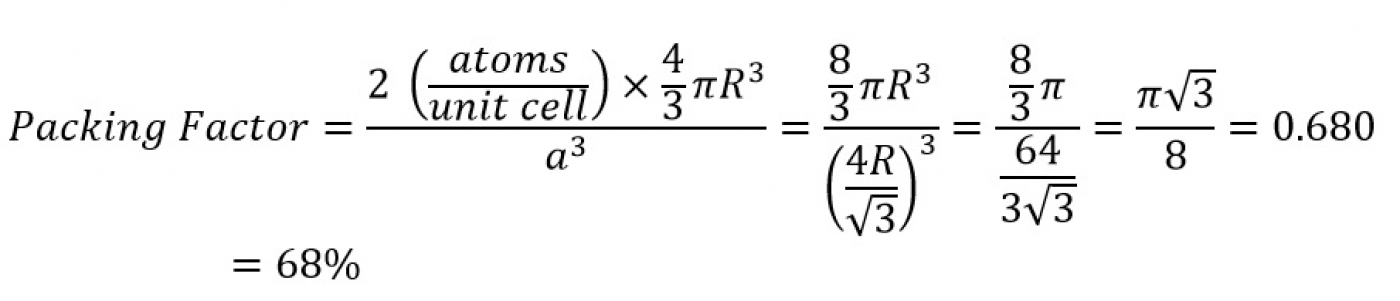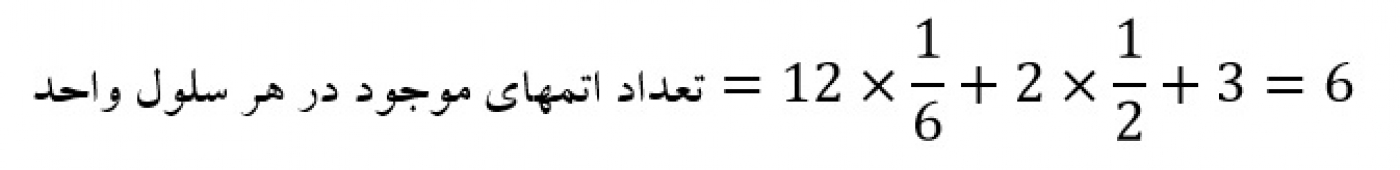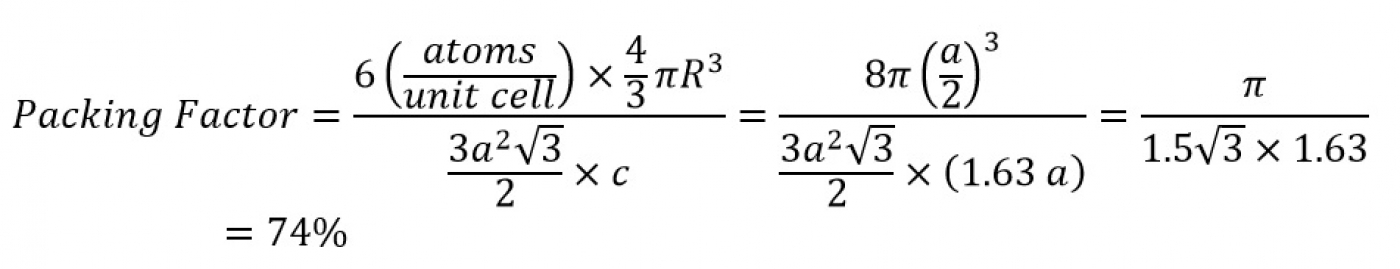12- انواع ساختارهای بلوری
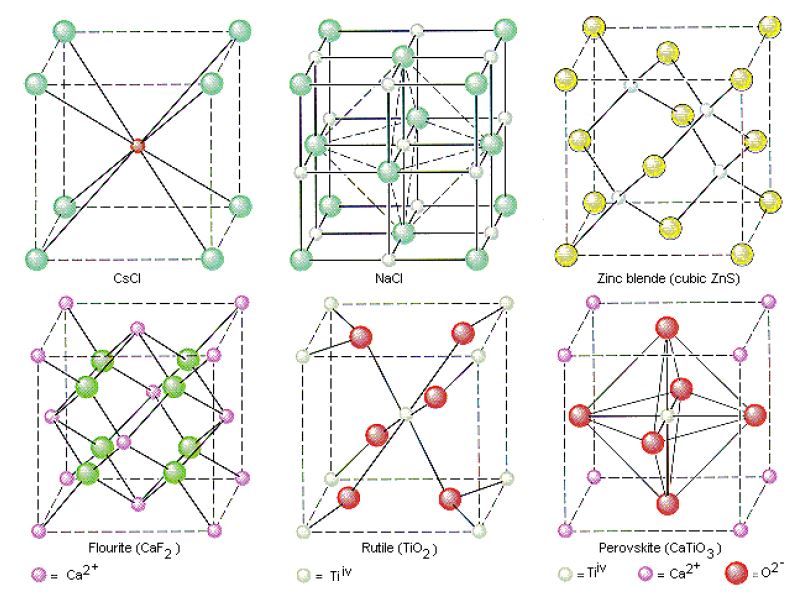
ساختار بلوری به ساختار و جهتگیری اتمها، یونها، یا مولکولهای داخل بلور جامد یا مایع گفته میشود. ساختار مرتب بلورها از طبیعت متقارن اجزاء تشکیلدهنده آن نشأت میگیرد. این ساختار بلوری را میتوان مجموعهای از واحدهای کوچک در نظر گرفت که تا بینهایت در سه بعد تکرار میشوند. این اجزای واحد کوچکترین واحد حجمی هستند که همه اطلاعات ساختار و تقارن برای تشکیل ساختار ماکروسکوپی بلور را در خود دارد. هر یک از این واحدها، سلول واحد یک شبکه بلوری نامیده میشوند. طول لبه سلول منفرد و زاویه لبه آن، پارامترهای بلور هستند که باعث به وجود آمدن شبکههای بلوری متفاوتی میشوند. در این مقاله به دستهبندیهای سلولهای واحد و معرفی هر یک از آنها پرداخته میشود.
این مقاله شامل سرفصلهای زیر است:
1- مقدمه
2- شبکههای کریستالی
1-2- پارامتر شبکه (Lattice Parameter)
2-2- فاکتور فشردگی اتمها (Packing Factor)
3-2- عدد همسایگی (Coordination Number)
4-2- تسلسل چیدن (Stacking Sequence)
3- شبکههای کریستالی مکعبی
1-3- ساختار مکعبی ساده Simple Cubic یا SC
2-3- ساختار مکعبی مرکز پُر Body Centered Cubic یا BCC
3-3- ساختار مکعبی با مراکز وجوه پُر Face Centered Cubic یا FCC
4-3- شبکه کریستالی هگزاگونال فشرده (Hexagonal Closed Packed یا HCP)
5-3- شبکههای کریستالی دیگر
1-5-3. ساختار کلرید سدیم (NaCl)
2-5-3. ساختار الماس
1- مقدمه

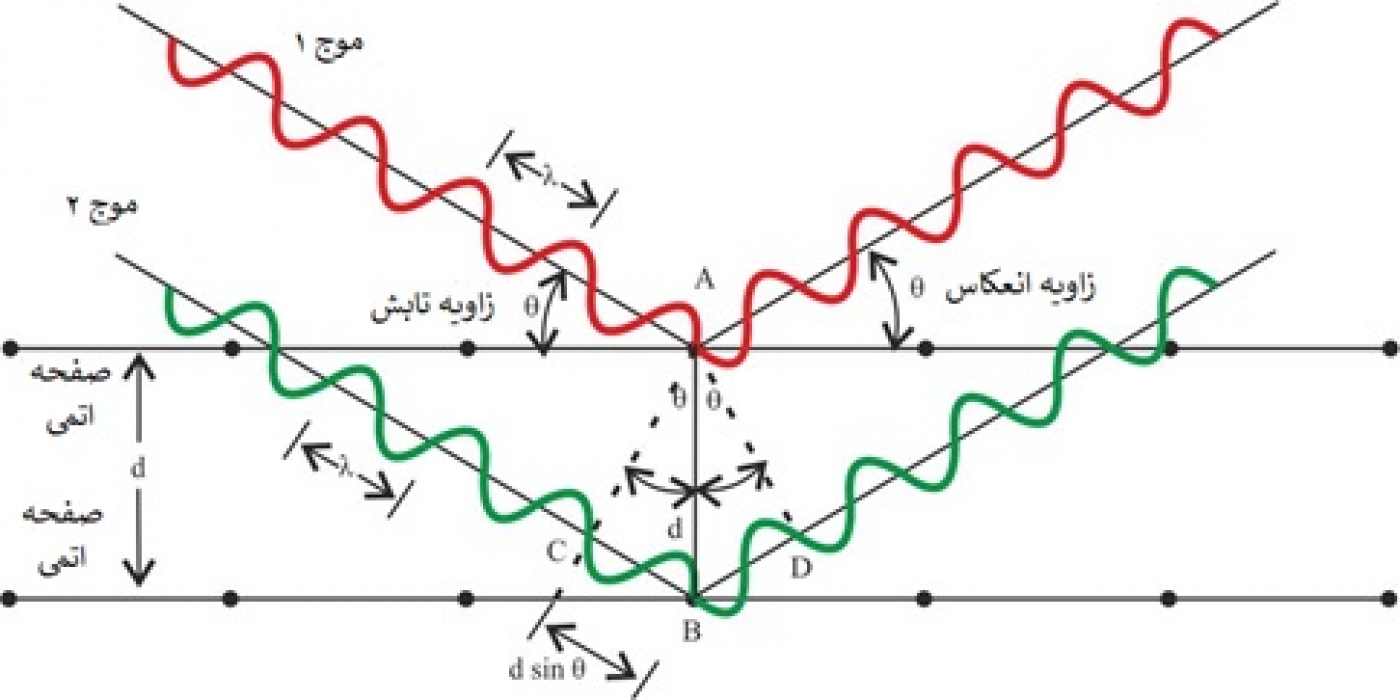
هنگامی که پرتو ایکس به نمونه بلوری با صفحات اتمی منظم برخورد میکند، بخشی از آن مانند نور در برخورد با سطح اجسام، بازتاب میشود. با توجه به انرژی بالا، بخشی از آن داخل نمونه نفوذ میکند و در داخل نمونه با صفحات اتمی پایینتر برخورد میکند و از آنجا بازتاب میشود. بنابراین دو دسته پرتو ایکس پس از برخورد به نمونه، از آن خارج میشوند: بخشی از روی سطح و بخشی از داخل نمونه. طبق قانون برهمنهی امواج، این دو دسته موج با هم تداخل میکنند و این تداخل ممکن است سازنده یا مخرب باشد.
زاویه پرتو فرودی که در شکل 2 با θ نشان داده شده است، مهمترین عامل در تعیین سازنده یا مخرب بودن این تداخل است. در شکل 2 مسافتی که این دو دسته پرتو طی میکنند تا از نمونه خارج شوند، نشان داده شده است. همانطور که از شکل هم مشخص است اختلاف مسیر بین این دو دسته پرتو 2dsinθ است که d فاصله بین صفحات اتمی است. طبق فیزیک امواج، شرط تداخل سازنده این است که اختلاف مسیر طی شده برابر با مضرب صحیحی از طول موج باشد. بنابراین رابطه زیر به دست میآید که به آن رابطه براگ گفته میشود و مبنای شناسایی مشخصات بلورها با استفاده از پرتو ایکس است.
که در آن n عددی صحیح و λ طول موج پرتو ایکس تابیده شده است. زاویه فرودی (θ) قابل تنظیم است. با توجه به مشخص بودن طول موج پرتو ایکس (λ)، به راحتی فاصله بین صفحات اتمی به دست میآید.
در کریستالوگرافی تنها خواص هندسی کریستال مورد توجه قرار میگیرد، بنابراین محل هر اتم یا مولکول، با یک نقطه هندسی در محل تعادلی آن اتم یا مولکول نشان داده میشود. شبکه کریستالی دسته نامحدودی از نقاط در فضا است که در مکانهای مشخص به شکل تناوبی تکرار میشوند. با قرار گرفتن اتم یا گروههایی از اتمها یا مولکولها در نقاط شبکه کریستالی، یک ساختار کریستالی بهدست میآید. به هر اتم، گروه اتمی یا مولکولی که در نقاط دیگر تکرار میشود، پایه (Basis) اطلاق میشود. شبکه (Lattice) نیز دستهای از نقاط در فضا است که به صورت تناوبی تکرار میشوند. سادهترین واحد کریستال همانطور که بیان شد، سلول واحد نامیده میشود. فضا با تکرار سلولهای واحد در سهبعد پر میشود و شبکه را پدید میآورد.
2- شبکههای کریستالی
شبکههای کریستالی به دو دسته معروف شبکههای براوه و شبکههای غیربراوه تقسیم میشوند. در شبکههای براوه همه اتمها از یک نوع بوده و همه نقاط شبکه معادل هم هستند. اما در شبکههای غیربراوه چند نوع اتم در شبکه وجود دارد و برخی مکانهای شبکه با هم متمایزند. در واقع شبکههای غیربراوه تلفیق دو یا چند شبکه براوه هستند.
یک شبکه فضایی مجموعهای از نقاط با فواصل برابر است که هر نقطه از شبکه را میتوان با یک بردار مشخص کرد. در این رابطه n1، n2 و n3 عددهای صحیح و a، b و c بردارهای یکه در سه جهت هستند. شکل 3 بردار نقطه P را در یک سلول واحد نشان میدهد. این بردار را میتوان با رابطه زیر نشان داد:
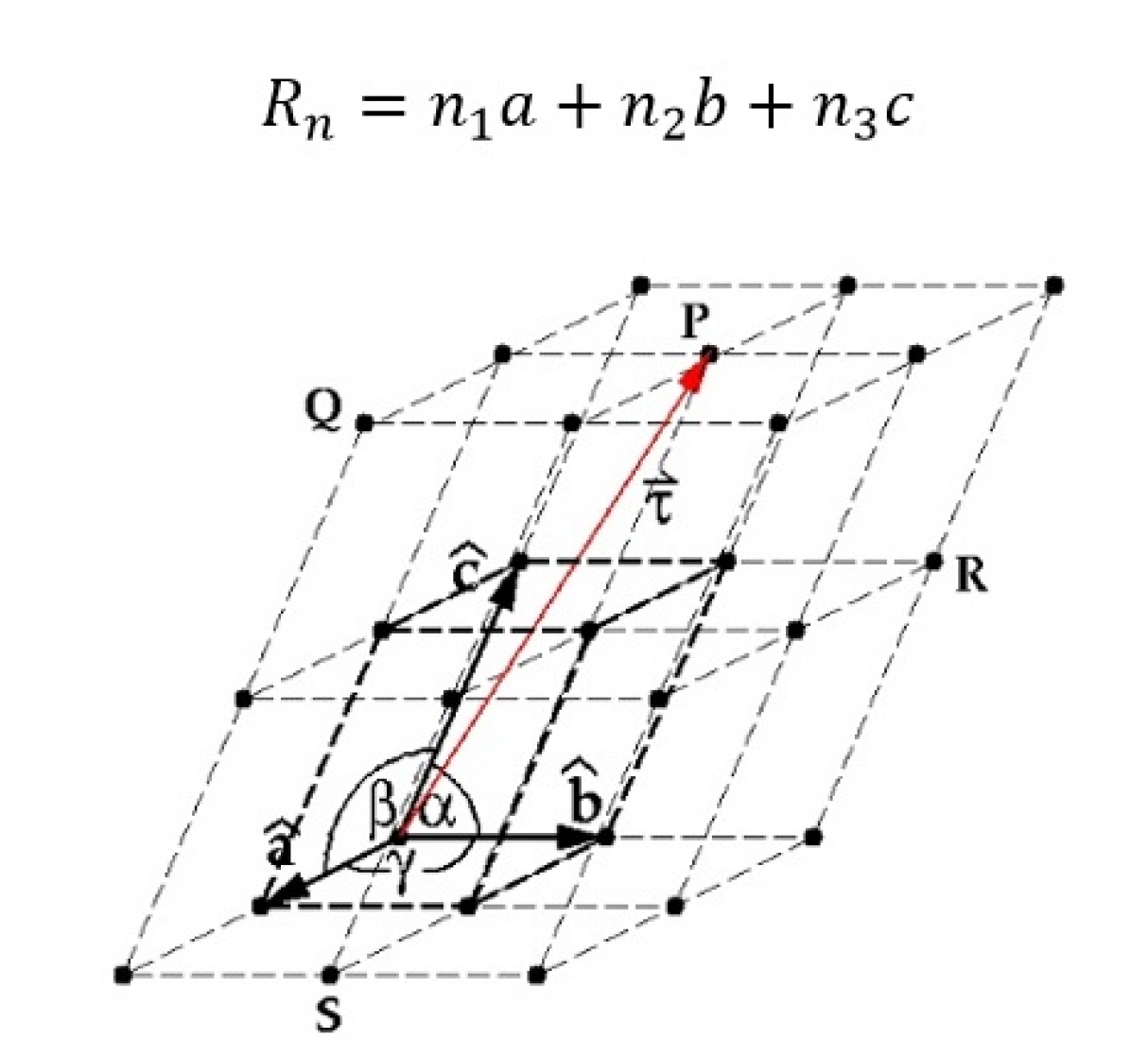
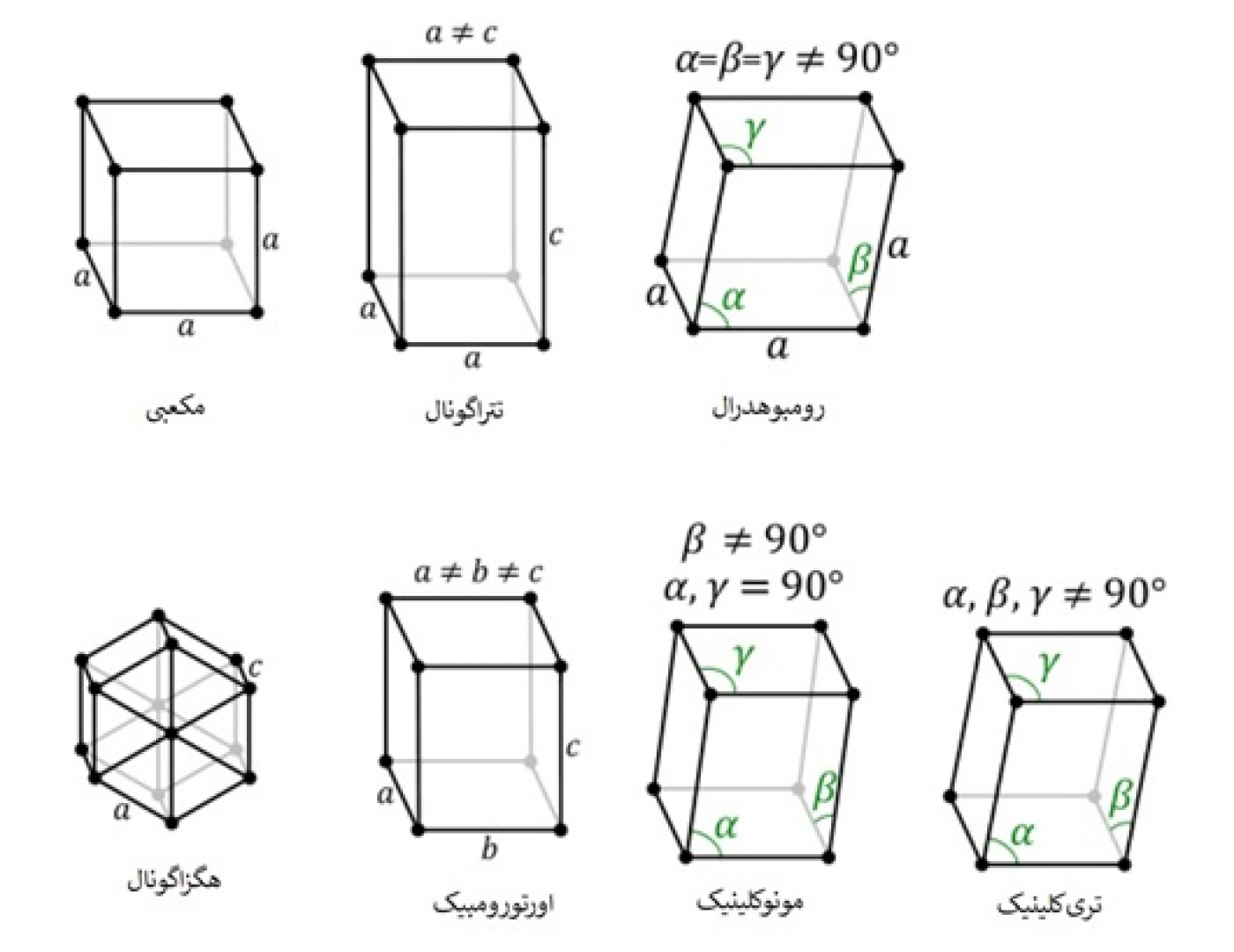
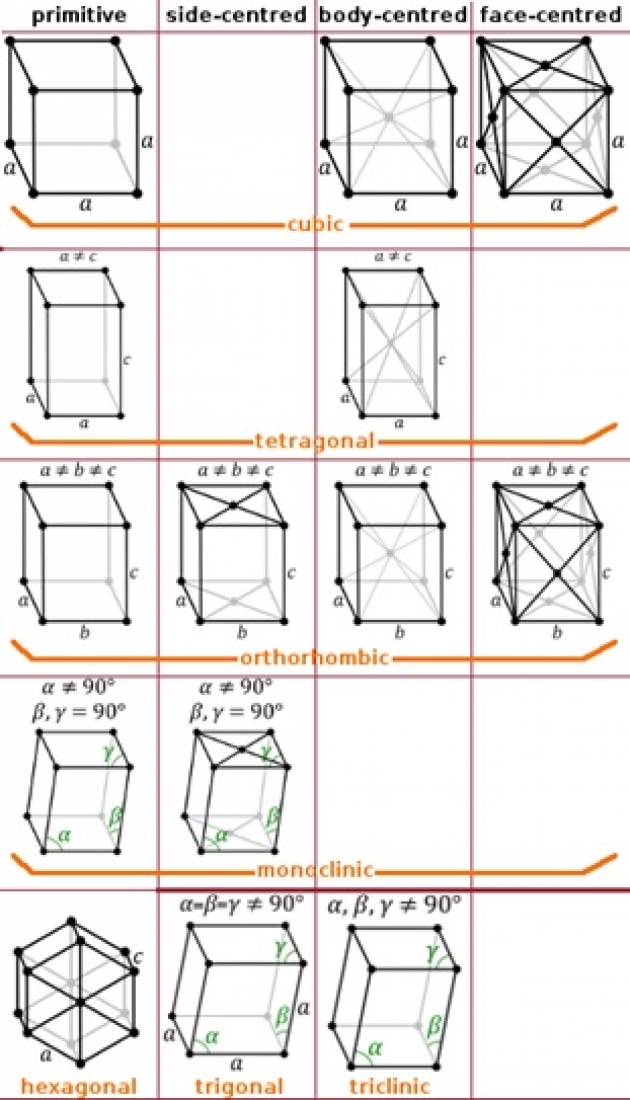
مطالعات کریستالوگرافی نشان داده است که همه بلورها را میتوان در هفت ساختار پایه (شکل هندسی) طبقهبندی کرد (شکل4). مشخصات هر شبکه همراه با نام آنها در شکل آورده شده است. این شبکهها شامل شبکههای مکعبی، ششگوشه، مکعب مستطیلی، رومبوهدرال، اورتورومبیک، مونوکلینیک و تریکلینیک هستند. با جایگذاری اتمها در این هفت ساختار پایه، میتوان به چهارده شبکه دست یافت که به شبکههای چهاردهگانه براوه معروفند که در شکل 5 نشان داده شدهاند. بهدلیل سادگی و اهمیت بالاتر شبکه مکعبی و ششگوشه (هگزاگونال)، در ادامه بیشتر به بحث در مورد این شبکهها میپردازیم.
پیش از بررسی شبکههای براوه نیاز به تعریف چند پارامتر در کریستالوگرافی است.
1-2- پارامتر شبکه (Lattice Parameter)
اطلاعاتی از سلول واحد است که به واسطه آنها بتوان اندازه، ابعاد و شکل سلول واحد را مشخص کرد. به عبارت دیگر، هندسه سلولهای واحد با استفاده از طول سه ضلع (a,b,c) و زوایای بین آنها به طور کامل تعریف میشود. اندازه اضلاع شبکه بر حسب انگستروم یا نانومتر بیان میشود و زاویه بین یالها بر حسب درجه بیان میشود. شکل 4 تصویر سلولهای واحد شبکه کریستالی را همراه با ثابتهای شبکه آنها نشان میدهد.
2-2- فاکتور فشردگی اتمها (Packing Factor)
میزان پرشدن فضای شبکه توسط اتمها، یا حجم اشغال شده توسط اتمهای داخل سلول واحد را فاکتور فشردگی اتمها مینامند.
3-2- عدد همسایگی (Coordination Number)
برای هر اتم تعداد نزدیکترین اتمهای مجاور، عدد کوردینانسی را مشخص میکنند. چون شبکه براوه به صورت تناوبی تکرار میشود، همه نقاط تعداد یکسانی نقاط همسایه یا عدد کوردینانسی دارند که این خاصیتی از شبکه است.
4-2- تسلسل چیدن (Stacking Sequence)
شبکه کریستالی از رویهم قرار گرفتن تعدادی زیادی صفحات اتمی تشکیل شده است که نحوه قرار گرفتن این لایهها را روی هم، تسلسل چیدن میگویند.
3- شبکههای کریستالی مکعبی
در این بخش به طور خاص شبکه کریستالی مکعبی مورد بررسی قرار میگیرد. همانطور که در شکل 6 نشان داده شده است، ساختارهای مکعبی به سه دسته ساختارهای مکعبی ساده، ساختارهای مکعبی مرکز پُر و ساختارهای مکعبی وجوه مراکز پُر، تقسیم میشوند.
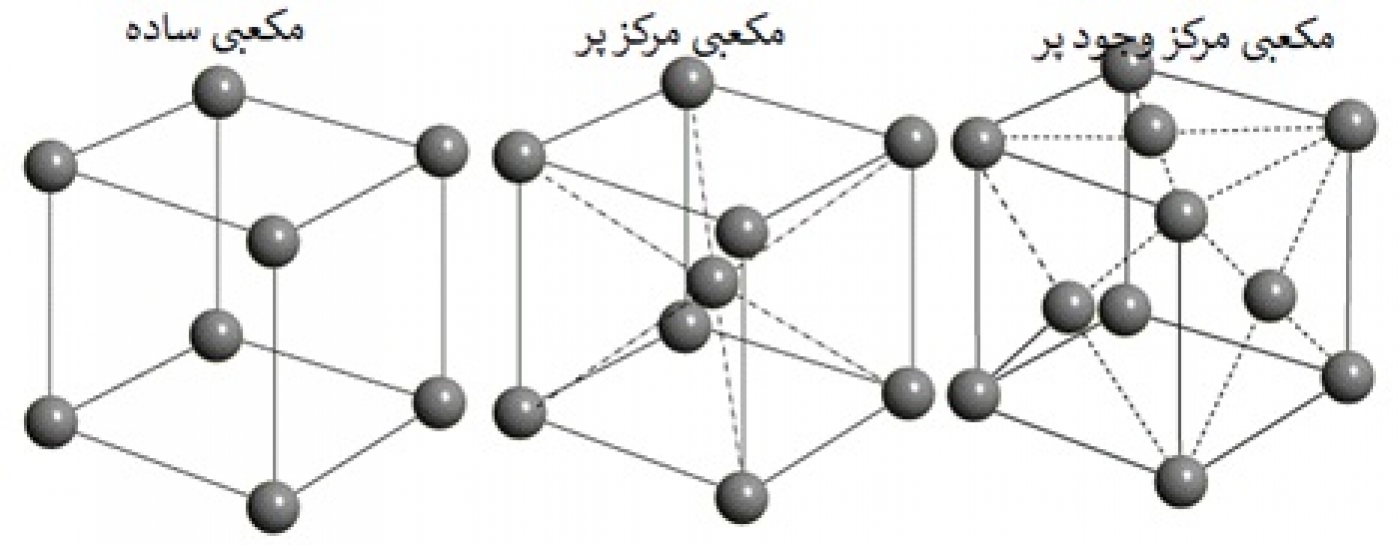
1-3- ساختار مکعبی ساده Simple Cubic یا SC
همانطورکه در شکل 7 نشان داده شده است، در این ساختار، اتمها تنها در گوشهها قرار دارند و در امتداد ضلع سلول واحد بر یکدیگر مماس هستند. از طرفی هر اتم که در گوشه مکعب قرار دارد، متعلق به هشت واحد شبکه است که در شکل 8 به طور کامل نشان داده شده است. با توجه به این شکل میتوان گفت عدد همسایگی این ساختار شش است.

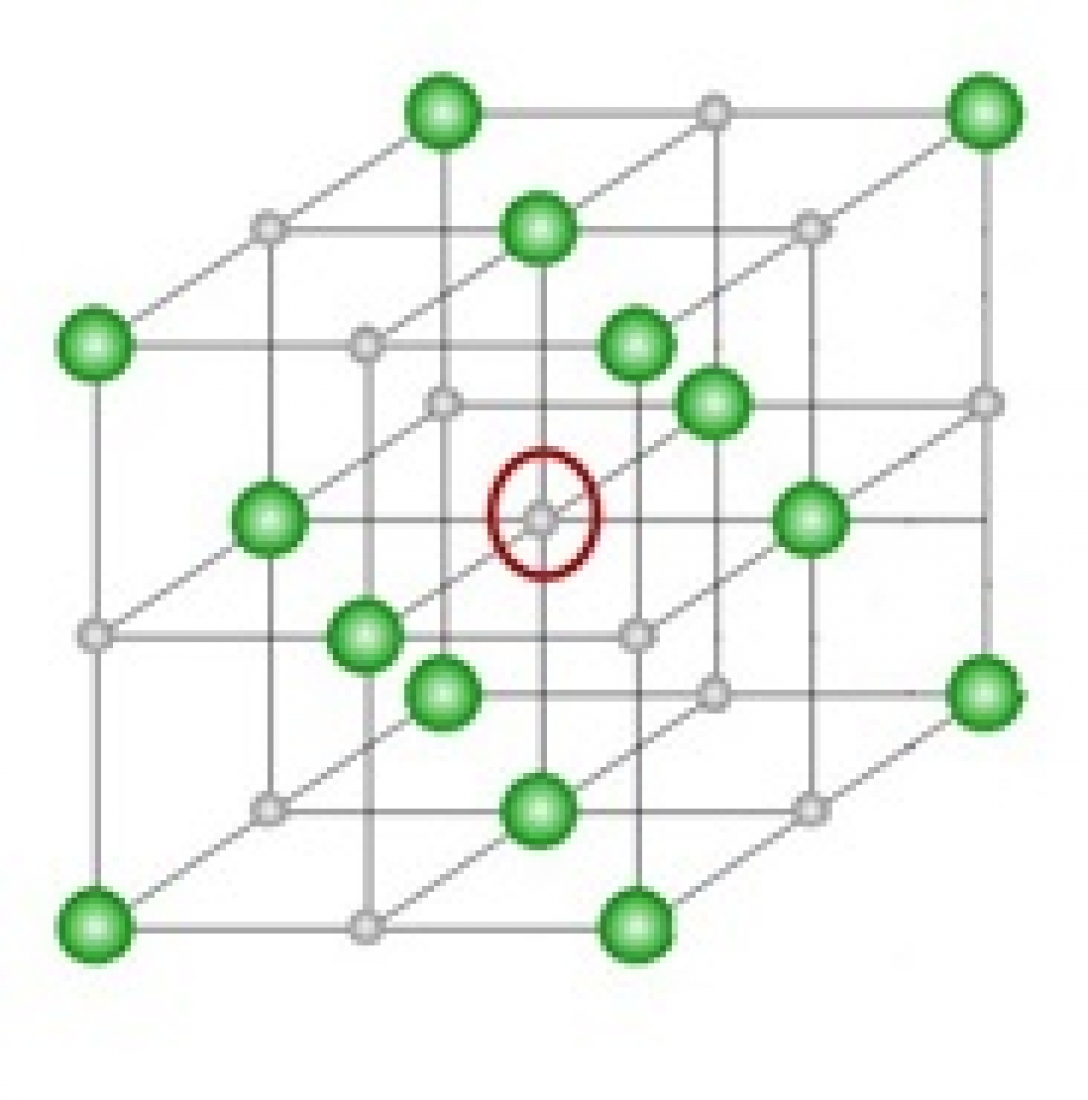
برای محاسبه تعداد اتمهای موجود در هر سلول واحد میتوان گفت با توجه به اینکه هر اتم که در گوشههای مکعب قرار گرفته باشد، بین 8 سلول واحد مشترک است، میتوان گفت 1/8 آن متعلق به هر سلول واحد است و چون هرمکعب 8 گوشه دارد، در مجموع در هر سلول واحد ساختار مکعبی ساده یک اتم وجود دارد:

که در آن R شعاع اتمی و a ضلع سلول واحد است.
حال برای محاسبه فاکتور فشردگی اتمی این ساختار باید حجم اشغال شده توسط اتمهای موجود در سلول واحد به حجم کل سلول واحد تقسیم شود. با فرض این که اتمها کرههایی توپر هستند میتوان نوشت:
گفته شد که در هر سلول واحد ساختار مکعبی ساده، یک اتم حضور دارد. بنابراین با توجه به فرمول فشردگی اتمی میتوان نوشت:
با استفاده از رابطه بین طول مکعب و شعاع اتم داریم:
2-3- ساختار مکعبی مرکزپُر Body Centered Cubic یا BCC
در این ساختار اتمها در گوشهها و مرکز مکعب قرار دارند، یعنی اتمها در راستای قطر مکعب بر یکدیگرمماس هستند و عدد همسایگی در این ساختار هشت است (شکل 9). در هر واحد شبکه نیز دو اتم (یک اتم در مرکز مکعب و یک اتم در گوشهها) موجود است. محاسبات مربوط به این ساختار در ادامه مطرح شده است.
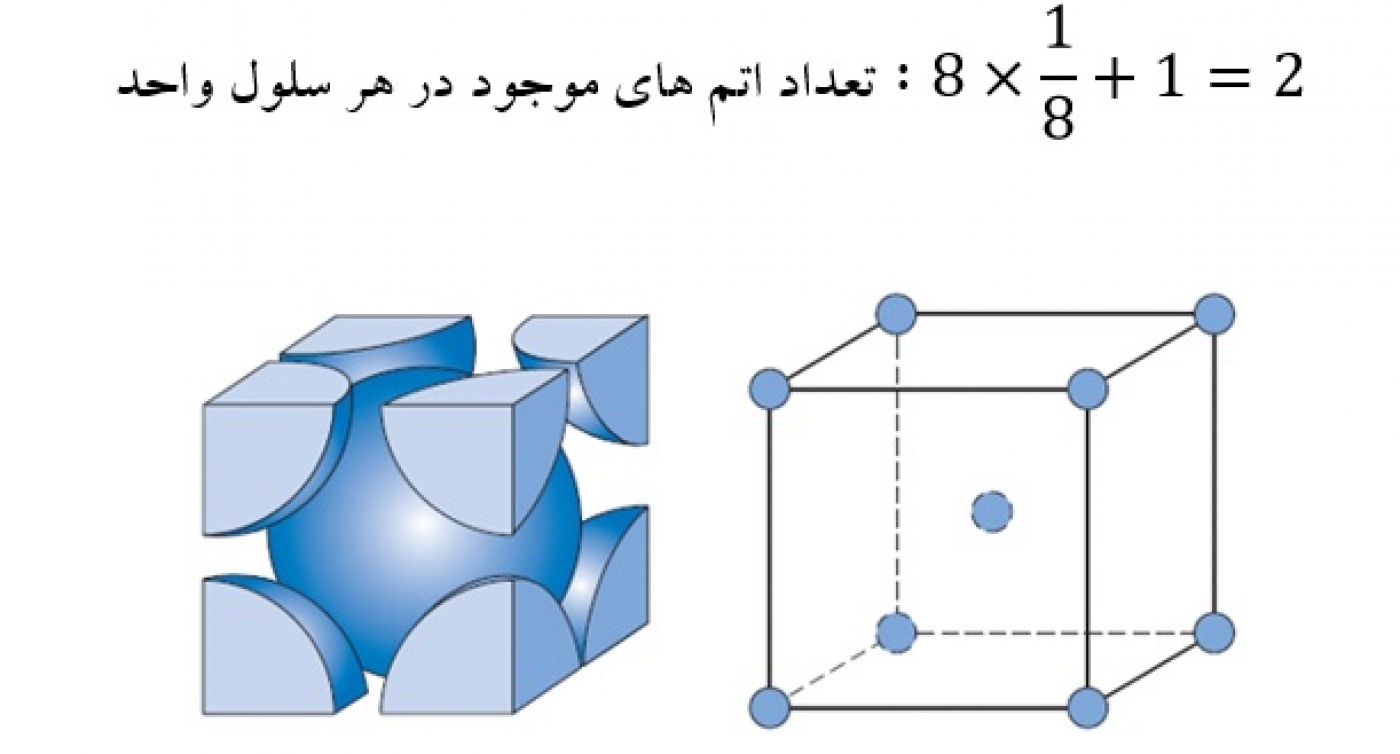
قطر مکعب از رابطه محاسبه میشود. بنابراین میتوان نوشت:
در اینجا نیز برای محاسبه فاکتور فشردگی اتمی میتوان نوشت:
بسیاری از فلزات شامل فلزات قلیایی مانند سدیم و بسیاری از عناصر واسطه مانند آهن در دمای محیط، در ساختار BCC متبلور میشوند.
3-3- ساختار مکعبی با مراکز وجوه پُر Face Centered Cubic یا FCC
در این ساختار اتمها در گوشهها و مراکز وجوه مکعب قرار دارند (شکل 10). به این ترتیب اتمهایی که در مراکز وجوه قرار دارند بین دو سلول واحد مشترک هستند. همچنین عدد همسایگی این ساختار دوازده است و اتمها در راستای قطر وجه بر یکدیگر مماس هستند. بسیاری از فلزات معمول مانند مس، نیکل و سرب در ساختار FCC شکل میگیرند.
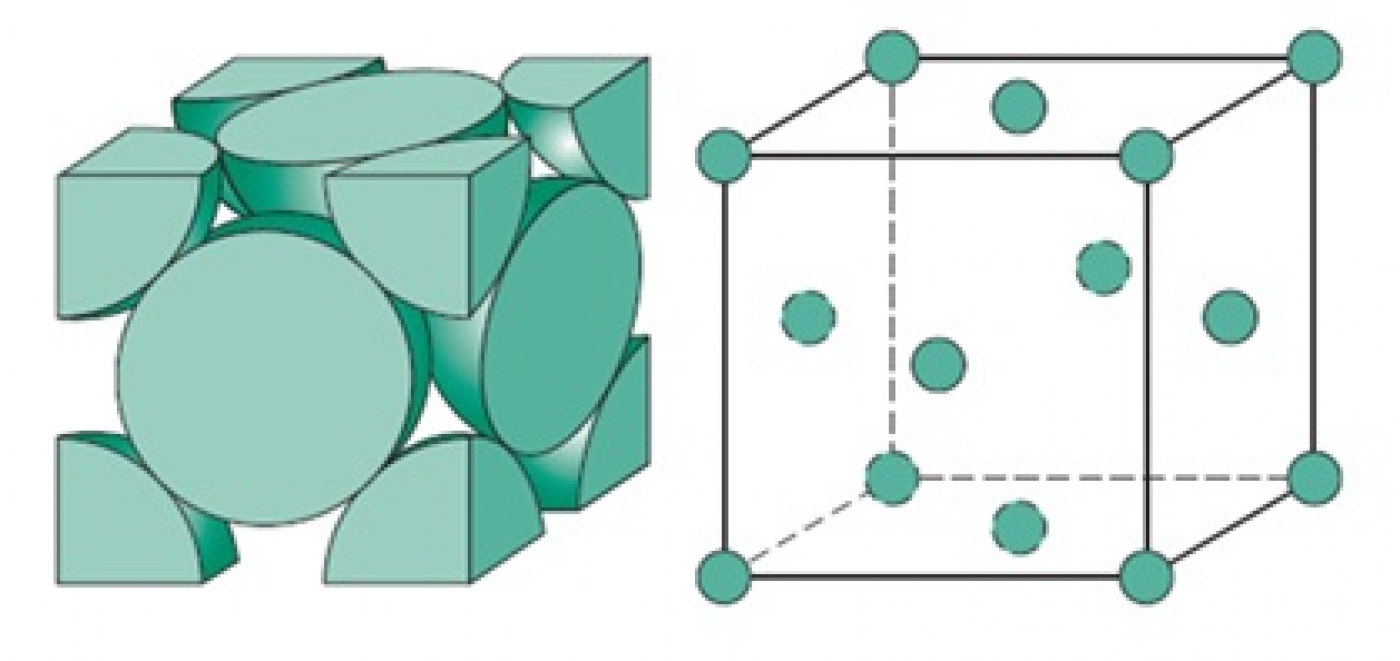
محاسبات مربوط به این ساختار در ادامه آورده شده است.
4-3- شبکه کریستالی هگزاگونال فشرده (Hexagonal Closed Packed یا HCP)
ساختار این شبکه کریستالی با ساختارهای قبلی متفاوت است. این ساختار منشوری با قاعده ششضلعی دارد که اتمها در شش گوشه دو قاعده قرار میگیرند. همچنین سه اتم دیگر در داخل منشور قرار میگیرند. برای تجسم مکان دقیق این سه اتم کافی است قاعده ششضلعی، به شش مثلث متساویالاضلاع تقسیم شود. این اتمها دقیقاً در صفحه میانی منشور و به صورت یک درمیان در مرکز این مثلثها قرار میگیرند (شکل 11). عدد همسایگی در این ساختار دوازده است. تعدادی از فلزات معمول مانند منیزیم و تیتانیم در ساختار HCP شکل میگیرند.
اتمهایی که در گوشههای این منشور قرار دارند با شش سلول واحد دیگر مشترک هستند. از طرفی اتمهایی که در مرکز قاعدهها قرار میگیرند بین دو سلول واحد مشترک هستند. بنابراین میتوان نوشت:
در این ساختار اتمها روی مثلثهای متساویالاضلاع بر یکدیگر مماس هستند. به عبارت دیگر میتوان نوشت:
a=2R
حجم منشور شش وجهی از رابطه 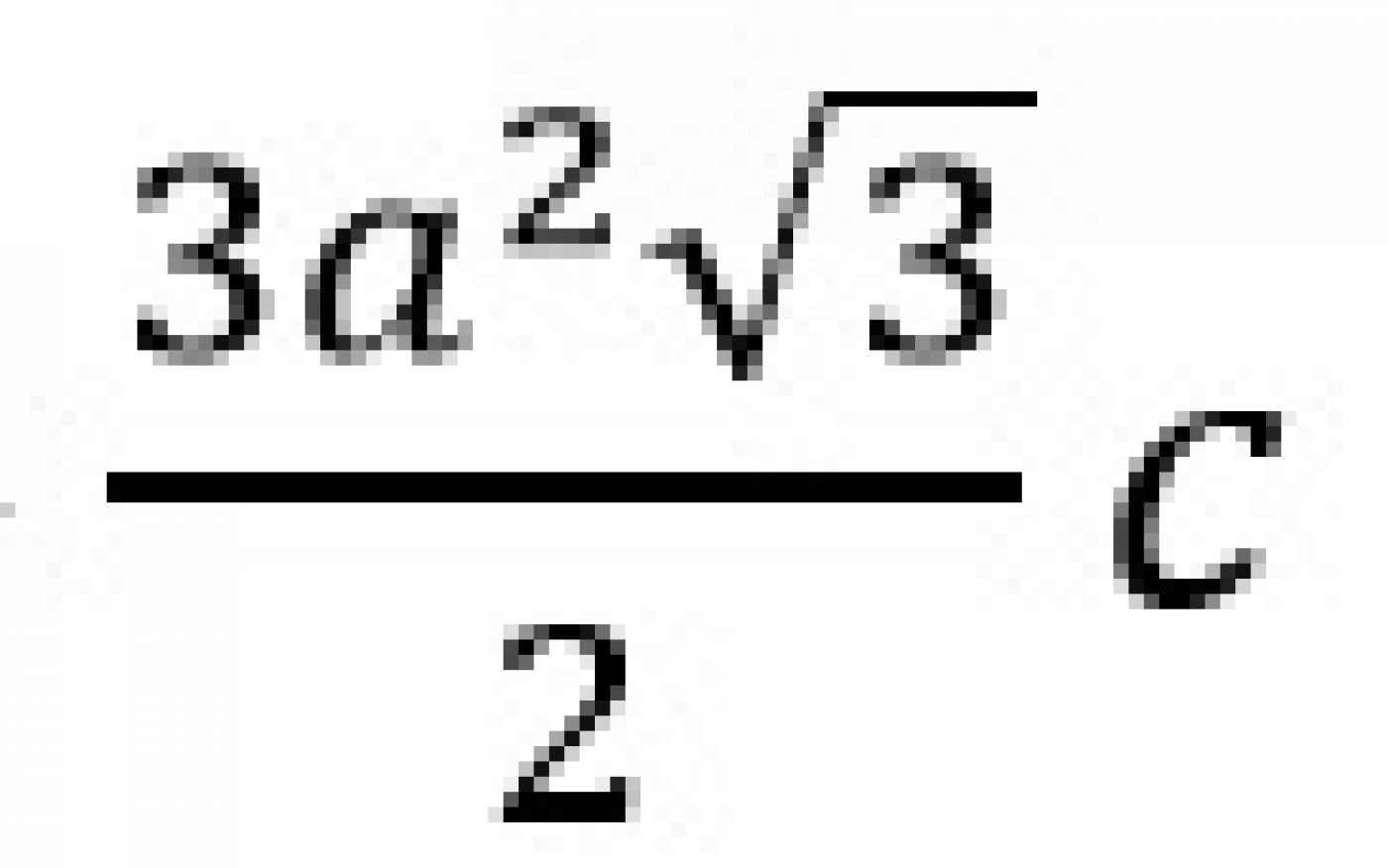
سه اتمی که داخل منشور قرار دارند در وسط ارتفاع منشور جای میگیرند. بنابراین میتوان گفت سه اتم از قاعده و یکی از اتمهای میانی، با هم یک چهاروجهی میسازند که اضلاعی به طول a و ارتفاعی برابر c/2 دارند. از طرفی برای محاسبه ارتفاع هرم، با توجه به شکل 12 میتوان نوشت:
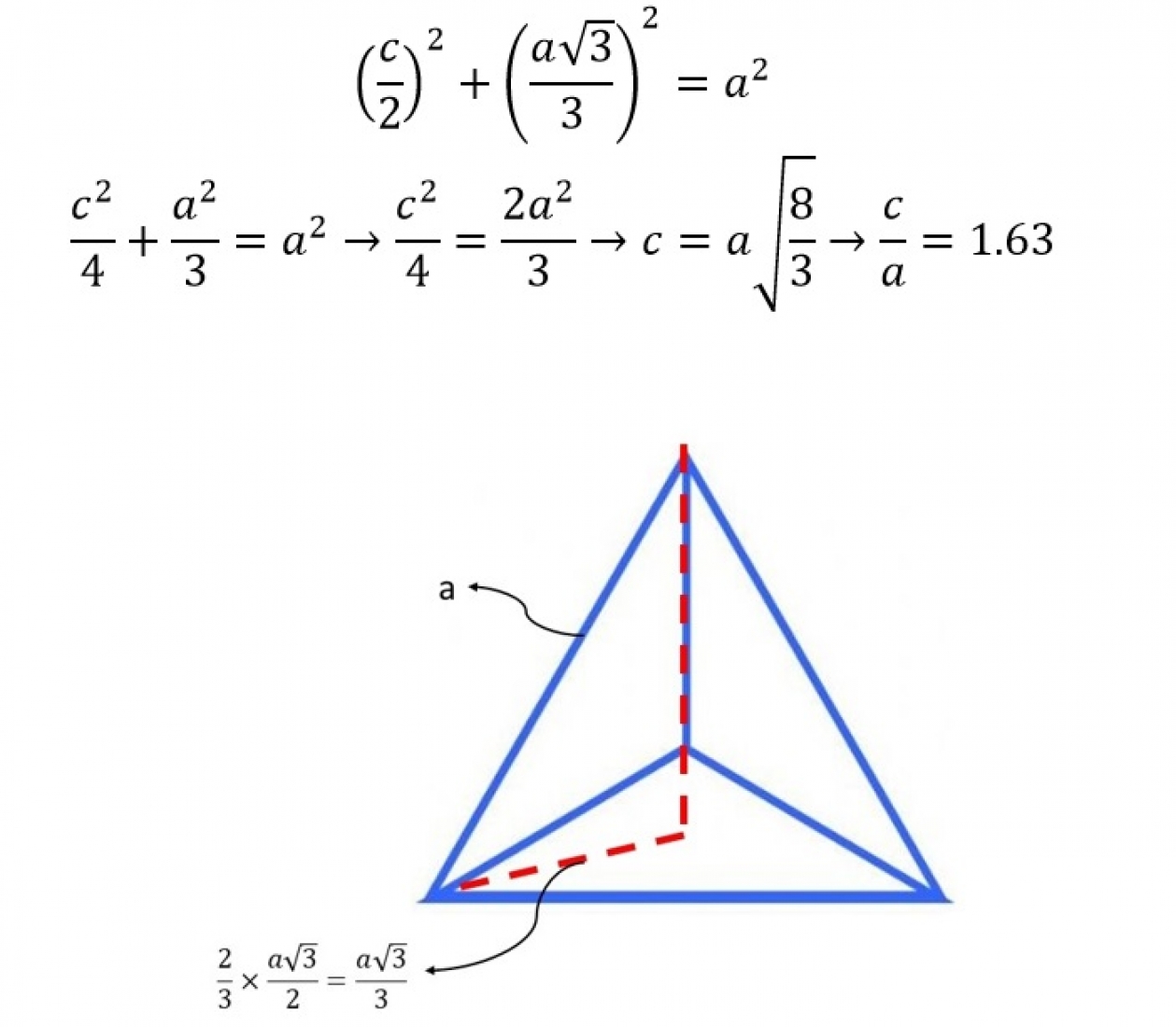
حال برای محاسبه فاکتور فشردگی اتمی میتوان نوشت:
5-3- شبکههای کریستالی دیگر
شبکههای کریستالی بحث شده تا به اکنون، سادهترین شبکههای کریستالی سهبعدی قابل بحث بودند اما ساختارهای کریستالی پیچیدهتری نیز وجود دارند که گاهی از ترکیب ساختارهای ساده ایجاد میشوند. در این قسمت تعدادی از ساختارهای کریستالی ترکیبات و مواد کووالانسی معرفی میشوند.
1-5-3. ساختار کلرید سدیم (NaCl)
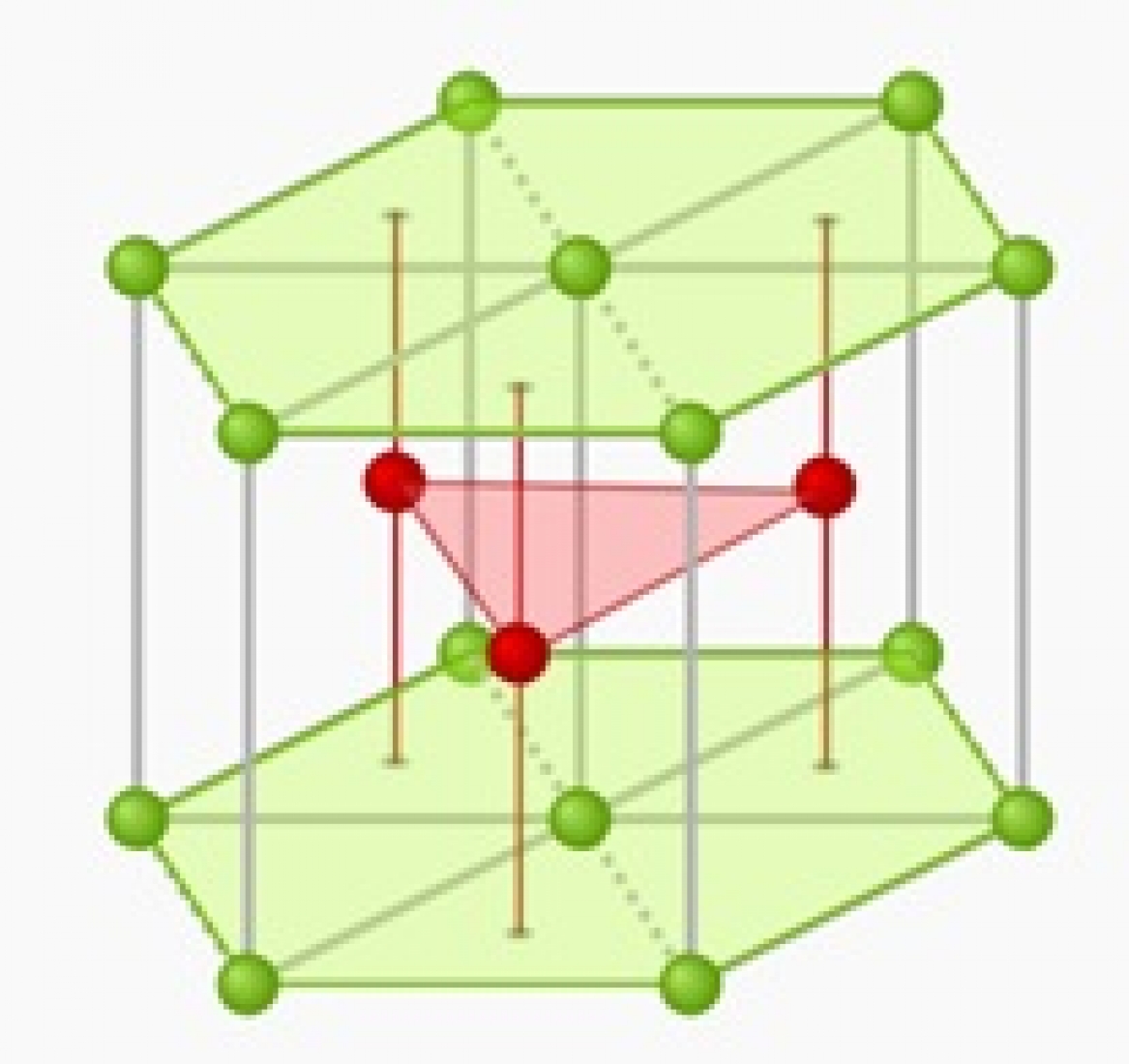
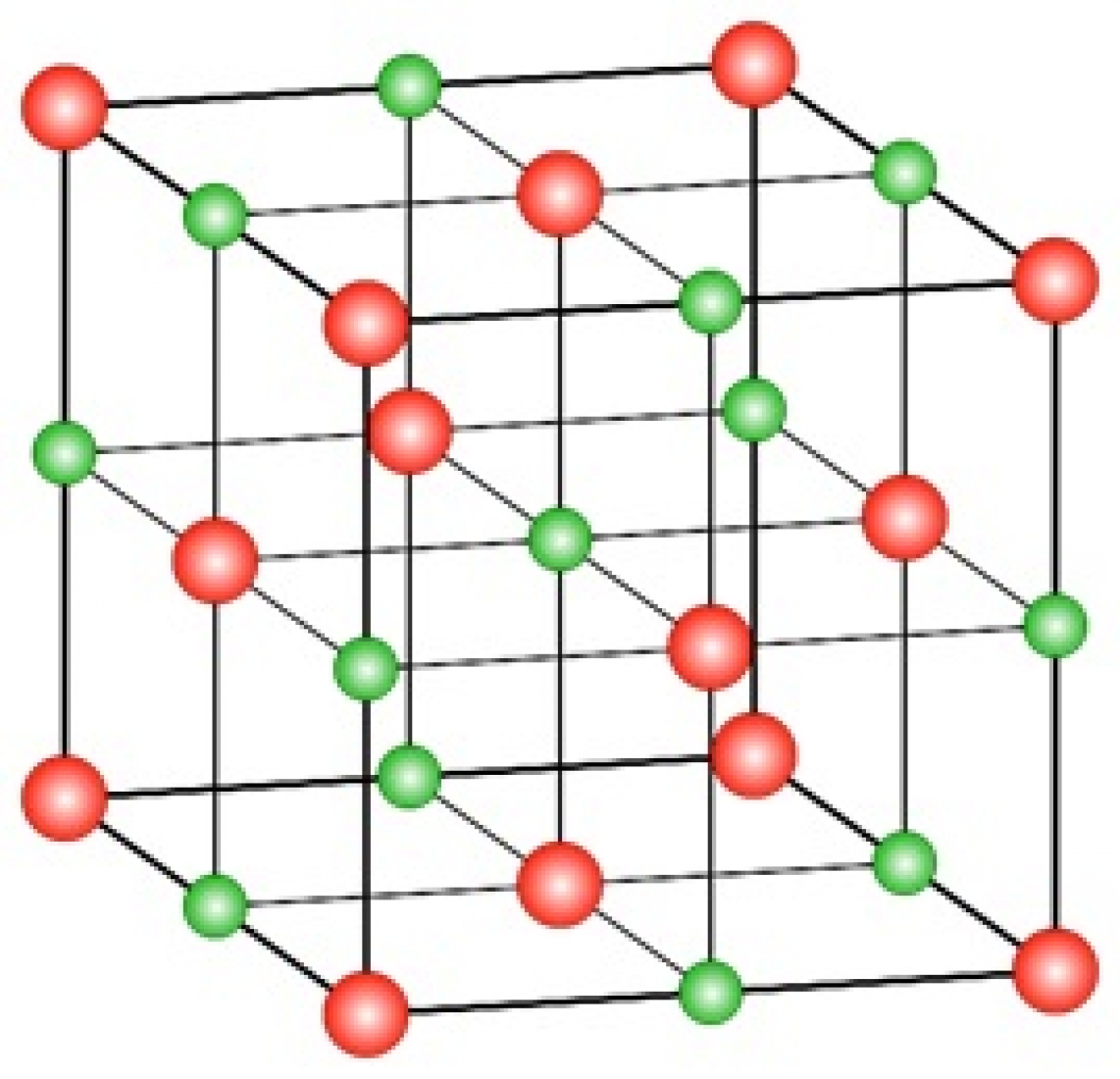
کلرید سدیم، فلورید لیتیم (LiF) و تعدادی دیگر از ترکیبات یونی، در یک شبکه کریستالی مکعبی به نام ساختار کلرید سدیم متبلور میشوند. در اینجا سلول واحد اندکی متفاوت است. ساختار کلرید سدیم شامل تعداد برابری یون سدیم و کلر است که در نقاط یکی درمیان یک شبکه کریستالی قرار گرفتهاند؛ بنابراین هر یون با شش یون، از نوع دیگر همسایه است. این ساختار کریستالی در شکل 13 نشان داده شده است. صرفنظر از اتمهای سدیم یا کلر میتوان گفت که ساختار اتمهای باقیمانده FCC است. بنابراین ساختار کلرید سدیم ترکیبی از دو ساختار FCC است. در شکل 13 گویهای قرمز نماینده یونهای کلر و گویهای سبز نماینده یونهای سدیم هستند.
2-5-3. ساختار الماس
ساختار الماس شامل دو شبکه با وجوه مرکز پر است که به داخل همدیگر نفوذ کردهاند. 8 اتم در ساختار الماس وجود دارد و هر اتم کربن در این ساختار با چهار اتم دیگر پیوند برقرار کرده است. سیلیسیم و ژرمانیم نیز با همین ساختار بلوری میشوند. شکل 14 ساختار الماس را نشان میدهد.
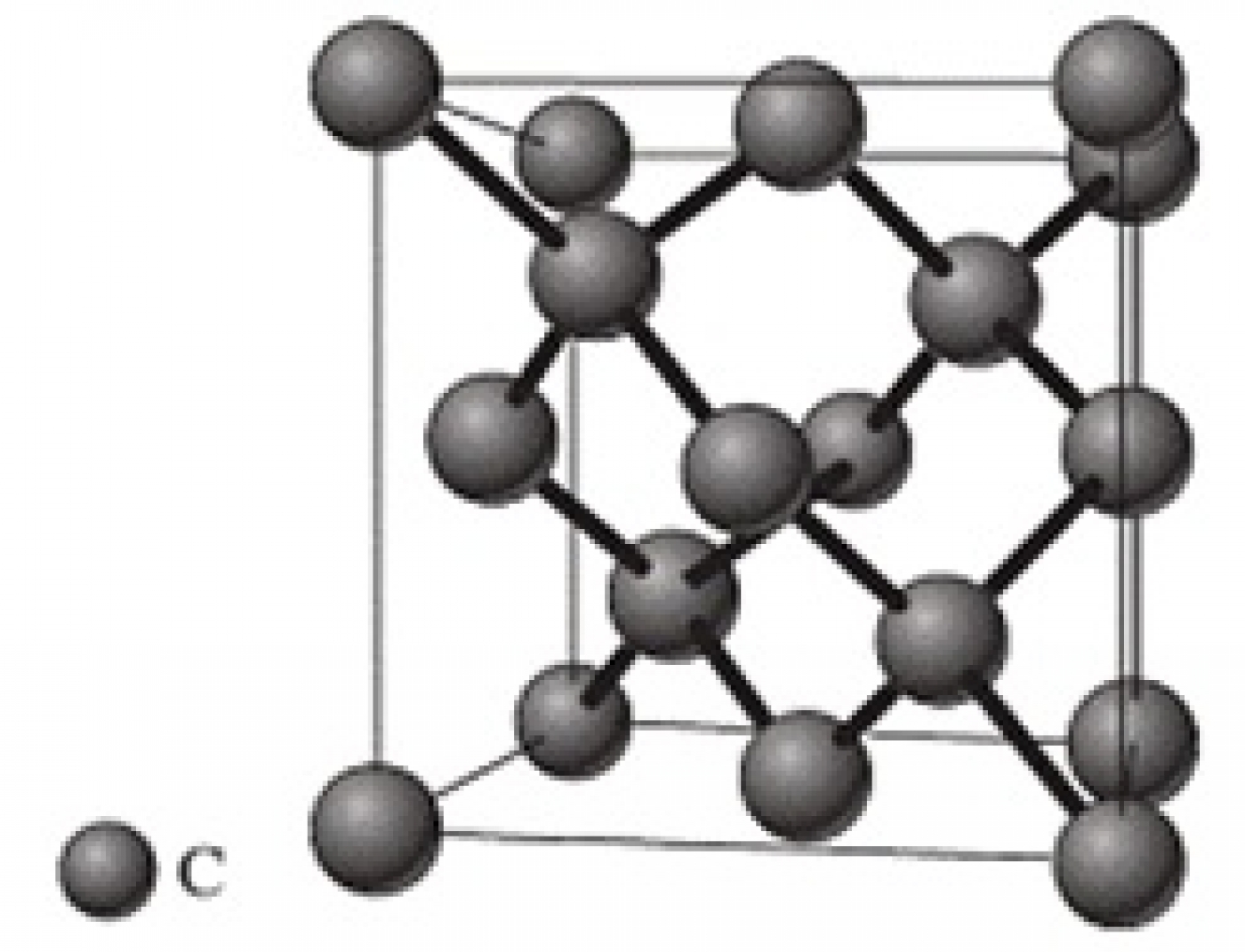
ساختارهای دیگری نیز وجود دارند که به دلیل پیچیدگی، بررسی آنها از حوصله این بحث خارج است.
منابـــع و مراجــــع