آموزش پیشرفتهآموزش نانو
روشهای کروماتوگرافی گازی بهمنظور تعیین باقیمانده سموم در مواد غذایی

روشهای کروماتوگرافی گازی بهطور گسترده برای آنالیز مواد غذایی به کار میرود. از این روش برای شناسایی کیفی و کمی ترکیبات موجود در مواد غذایی، مواد طبیعی، افزودنیها، آلایندهها مانند آفتکشها، آلودگیهای محیطی، سموم طبیعی، داروهای دامپزشکی و مواد بستبندی استفاده میشود. در این مقاله، روش تعیین باقیمانده سموم در مواد غذایی با دستگاه کروماتوگرافی گازی/طیفسنج جرمی از مرحله آمادهسازی نمونه تا گزارش نهایی و شرح مختصر دستگاه مورد بحث قرار گرفته است.
این مقاله شامل سرفصلهای زیر است:
1- مقدمه
2- آمادهسازی نمونه: استخراج و تصفیهی نمونه
۱-2- اصول آمادهسازی نمونهی مواد غذایی بهمنظور آنالیز ی سموم:
۱-۱-2- استخراج نمونه:
۱-۱-۱-2- استخراج مایع – مایع
2-1-1-2- روش حلال کاهش یافته
3-1-1-2- میکرو استخراج تک قطره
4-1-1-2- روشهای بر پایه جاذب
3- روشهای اندازهگیری کمّی
1-3- ستونهای کروماتوگرافی گازی
1-1-3- ستونهای پر شده
۲-۱-3- ستون مویینه
3-1-3- ستون مویینه سیلیکای جوش خورده
4-1-3- انتخاب ستون مویینه:
5-1-3- طول ستون، قطر داخلی و ضخامت
۲-3- انتخاب آشکارساز برای اندازهگیری سموم با کروماتوگرافی گازی
1-2-3- آشکارساز ربایش الکترون
۲-۲-3- آشکارساز نورسنج شعلهای
3-۲-3- آشکارساز یونیزاسیون شعله قلیایی:
4-۲-3- آشکارساز گرما یونی نیتروژن – فسفر
5-۲-3- آشکارساز طیفسنج جرمی
1-5-2-3- جفت شدن کروماتوگرافی گازی با طیفسنج جرمی
1-1-5-2-3- روش پایش
2-1-5-2-3- روش مانیتورینگ یون انتخابی
4- آنالیزهای تاییدی
1-4- تایید با استفاده از ستونهای با قطبیتهای مختلف
2-4- تایید به روش مشتقسازی
5- شبکه آزمایشگاهی فناوری راهبردی
6- نتیجهگیری
این مقاله شامل سرفصلهای زیر است:
1- مقدمه
2- آمادهسازی نمونه: استخراج و تصفیهی نمونه
۱-2- اصول آمادهسازی نمونهی مواد غذایی بهمنظور آنالیز ی سموم:
۱-۱-2- استخراج نمونه:
۱-۱-۱-2- استخراج مایع – مایع
2-1-1-2- روش حلال کاهش یافته
3-1-1-2- میکرو استخراج تک قطره
4-1-1-2- روشهای بر پایه جاذب
3- روشهای اندازهگیری کمّی
1-3- ستونهای کروماتوگرافی گازی
1-1-3- ستونهای پر شده
۲-۱-3- ستون مویینه
3-1-3- ستون مویینه سیلیکای جوش خورده
4-1-3- انتخاب ستون مویینه:
5-1-3- طول ستون، قطر داخلی و ضخامت
۲-3- انتخاب آشکارساز برای اندازهگیری سموم با کروماتوگرافی گازی
1-2-3- آشکارساز ربایش الکترون
۲-۲-3- آشکارساز نورسنج شعلهای
3-۲-3- آشکارساز یونیزاسیون شعله قلیایی:
4-۲-3- آشکارساز گرما یونی نیتروژن – فسفر
5-۲-3- آشکارساز طیفسنج جرمی
1-5-2-3- جفت شدن کروماتوگرافی گازی با طیفسنج جرمی
1-1-5-2-3- روش پایش
2-1-5-2-3- روش مانیتورینگ یون انتخابی
4- آنالیزهای تاییدی
1-4- تایید با استفاده از ستونهای با قطبیتهای مختلف
2-4- تایید به روش مشتقسازی
5- شبکه آزمایشگاهی فناوری راهبردی
6- نتیجهگیری
1- مقدمه
آنالیز سموم در مقیاس خیلی کم در نمونههای محیطی و غذایی از مسائل اساسی برای یک شیمیدان تجزیه است. انتخاب یک روش استخراج و آنالیز دقیق و صحیح، موضوع مهمی است که میتواند در نتیجه نهایی بسیار تاثیرگذار باشد. اگر چه روشهای قدیمی همچنان در آزمایشگاههای زیادی استفاده میشود، اما از آنجا که در بیشتر این روشها نیاز به استفاده از حجم زیادی از حلال، صرف زمان و کار زیاد است، در سالهای اخیر به سرعت در حال جایگزین شدن با روشهای سادهتر و موثرتر هستند. انواع روشهای کم کردن حلال برای نمونههای مایع و روشهایی نظیر استخراج سوکسله، استخراج با حلال شتاب یافته، استخراج با حلال فوق بحرانی و استخراج با استفاده از ماکروویو از اولین روشهایی هستند که مورد استفاده قرار گرفتند [۱].
روشهای متعددی در مقالات مطرح شده که به تغلیظ و آمادهسازی نمونه مربوط میشود. این روشها عبارتند از: استخراج مایع – مایع، استخراج فاز جامد و میکرو استخراج فاز جامد، استخراج با سیال فوق بحرانی، استخراج به همراه بیرون اندازی نمک و غیره. روشهای استخراج مایع – مایع و بیروناندازی با نمک بهطور معمول نیاز به حجم زیادی حلال آلی دارند که سمی و گران قیمت هستند، ضمن آنکه در نهایت حجم زیادی پسماند حلالهای آلی باید دور ریختهشود. در کنار این روشها، روشهای دیگری نیز به کار میرود که هر یک مزایا و معایب خود را دارند. روشهای استخراج با فاز جامد در بافتهای مختلف برای ترکیبات خاص کاربرد دارند. روشهای مستقیم استخراج با فاز جامد برای آنالیز آب و همچنین روشهای غیرمستقیم برای داروها در سیالات بیولوژیکی استفاده میشود. روش فاز جامد گرچه روش بسیار قابل اعتمادی است و نیاز به حجم اندکی حلال دارد، اما فرآیند استخراج شامل مراحل متعدد آمادهسازی اولیه ستون، عبور نمونه، شستشو با حلال و حذف عوامل مزاحم و در نهایت خارج ساختن آنالیتهای جذب شدهاست. روشهای دیگر میکرو استخراج و ویژگیهای برخی از آنها در ادامه بررسی میشود [2].
2- آمادهسازی نمونه: استخراج و تصفیهی نمونه
استخراج روشی است که بهمنظور جداسازی آنالیت از بافت نمونه با استفاده از حلال مناسب مورد استفاده قرار میگیرد. استخراج باید بهگونهای انجام شود که در انتهای کار محلولی با بالاترین غلظت از آنالیت همراه با کمترین میزان آلودگی به عوامل تداخلکننده، بهدست آید.
۱-2- اصول آمادهسازی نمونهی مواد غذایی بهمنظور آنالیز ی سموم
در آنالیز نمونههای مواد غذایی با دو نوع بافت مواجه هستیم. یکی بافتهای به نسبت ساده مانند آب، آب میوه و مشروبات الکلی و دیگر نوشیدنیها و دیگری، بافتهای پیچیدهتر با منشاء گیاهی و حیوانی. بافتهای غذایی، ترکیبات بسیار زیادی دارند که میتوانند در طی مراحل مختلف شناسایی و تعیین آنالیت تداخل ایجاد کنند بنابراین لازم است قبل از تزریق به دستگاه با انواع روشهای فیزیکی و شیمیایی جداسازی شوند. بهطور معمول، تجزیه و تحلیل و غربالگری برای تعداد زیادی از آفتکشها و آلایندهها در نمونههای غذایی شامل حداقل سه گام اساسی است: جداسازی، استخراج و تصفیه.
فرایند جداسازی روشی است که ترکیبی از ماده شیمیایی را به دو یا چند مخلوط متمایز تبدیل میکند که هر کدام ممکن است خود یک مخلوط جدید باشند و حداقل یکی از آنها از یک یا چند جزء از بافت نمونه غنی شدهاست.
استخراج یک فرایند جداسازی است که از جداسازی یک ماده از بافت نمونه تشکیل شدهاست. در فرایند استخراج در حالت ایدهآل تنها یک جزء (آنالیت) از بافت نمونه جدا میشود. اما در شرایط آزمایشگاهی برای نمونههای حقیقی محصول فرایند استخراج مخلوط از چند یا چندین جزء با ساختارهای نسبتا مشابه است (ترکیبات هماستخراج).
تصفیه، مرحله بعد از استخراج است. در این مرحله تلاش میشود تا ترکیبات هماستخراج از محصول مرحله استخراج جدا شوند و محلول نهایی دارای بیشترین غلظت از آنالیت مورد نظر و کمترین غلظت از ترکیبات مزاحم باشد [3].
بهطور معمول، نمونههای مواد غذایی به چهار دسته طبقهبندی میشوند:
۱- مواد غذایی با رطوبت بالا و چربی پایین (میوهها و سبزیجات)، ۲- مواد غذایی با رطوبت بالا و چربی بالا (گوشت و شیر)، ۳- مواد غذایی با رطوبت پایین و چربی پایین (آرد)، ۴- مواد غذایی با رطوبت پایین و چربی بالا (کره، روغنها و غیره).
هر یک از گروههای ذکر شده در این طبقهبندی شرایط مخصوص به خود را در فرآیندهای جداسازی، استخراج و تصفیه دارند که لازم است در هنگام انتخاب راهکار مناسب برای آمادهسازی نمونه در نظر گرفته شود.
فرایند جداسازی روشی است که ترکیبی از ماده شیمیایی را به دو یا چند مخلوط متمایز تبدیل میکند که هر کدام ممکن است خود یک مخلوط جدید باشند و حداقل یکی از آنها از یک یا چند جزء از بافت نمونه غنی شدهاست.
استخراج یک فرایند جداسازی است که از جداسازی یک ماده از بافت نمونه تشکیل شدهاست. در فرایند استخراج در حالت ایدهآل تنها یک جزء (آنالیت) از بافت نمونه جدا میشود. اما در شرایط آزمایشگاهی برای نمونههای حقیقی محصول فرایند استخراج مخلوط از چند یا چندین جزء با ساختارهای نسبتا مشابه است (ترکیبات هماستخراج).
تصفیه، مرحله بعد از استخراج است. در این مرحله تلاش میشود تا ترکیبات هماستخراج از محصول مرحله استخراج جدا شوند و محلول نهایی دارای بیشترین غلظت از آنالیت مورد نظر و کمترین غلظت از ترکیبات مزاحم باشد [3].
بهطور معمول، نمونههای مواد غذایی به چهار دسته طبقهبندی میشوند:
۱- مواد غذایی با رطوبت بالا و چربی پایین (میوهها و سبزیجات)، ۲- مواد غذایی با رطوبت بالا و چربی بالا (گوشت و شیر)، ۳- مواد غذایی با رطوبت پایین و چربی پایین (آرد)، ۴- مواد غذایی با رطوبت پایین و چربی بالا (کره، روغنها و غیره).
هر یک از گروههای ذکر شده در این طبقهبندی شرایط مخصوص به خود را در فرآیندهای جداسازی، استخراج و تصفیه دارند که لازم است در هنگام انتخاب راهکار مناسب برای آمادهسازی نمونه در نظر گرفته شود.
۱-۱-2- استخراج نمونه
روش اولیهی آمادهسازی میوهها و سبزیجات برای آنالیز باقیماندهی سموم، همگنسازی نمونه در آسیاب با سرعت بالا و سپس اضافه کردن یک حلال غیر قطبی که بهطور معمول هگزان یا بنزن است. سپس استونیتریل بهعنوان حلال استخراج کننده برای باقیمانده سموم ارگانوفسفره و ارگانوکلره استفاده میشود. این روش توسط میلز، انلی و گیتر در سال ۱۹۶۳ توسعه یافته است و اغلب بهعنوان روش OG یا میلز معروف است. این روش برای آنالیز باقیماندهی سموم در مواد گیاهی در طول 20 سال گذشته مورد استفاده قرار گرفته و بهعنوان روشی رسمی در بسیاری از کشورها به تصویب رسیدهاست. در نمونههایی با رطوبت پایینتر، به یک نسبت ثابت آب و استونیتریل به نمونه اضافه میشود [۱].
انتخاب روش مناسب آنالیز به طبیعت و بافت نمونه بستگی دارد. علاوهبر روش میلز و دیگر روشهای استخراج قدیمیتر، در سالهای اخیر، روشهای استخراج جدیدتری نیز معرفی شدهاست که از آن میان میتوان به موارد زیر اشاره کرد: میکرو استخراج تک قطره، میکرو استخراج مایع غشای فیبر توخالی استخراج فاز جامد میکرو استخراج فاز جامد، استخراج جذبی با میله چرخنده و میکرو استخراج فیبر توخالی پوشش داده شده با پلیمر [2].
انتخاب روش مناسب آنالیز به طبیعت و بافت نمونه بستگی دارد. علاوهبر روش میلز و دیگر روشهای استخراج قدیمیتر، در سالهای اخیر، روشهای استخراج جدیدتری نیز معرفی شدهاست که از آن میان میتوان به موارد زیر اشاره کرد: میکرو استخراج تک قطره، میکرو استخراج مایع غشای فیبر توخالی استخراج فاز جامد میکرو استخراج فاز جامد، استخراج جذبی با میله چرخنده و میکرو استخراج فیبر توخالی پوشش داده شده با پلیمر [2].
۱-۱-۱-2- استخراج مایع – مایع
استخراج مایع – مایع روشی کارآمد و آسان بهمنظور استخراج برای بافتهای مایع است. در این روش حلال غیر قابل امتزاج، مانند هگزان، بنزن و اتیل استات برای استخراج سموم غیر قطبی و دیکلرومتان، کلروفرم-متانول، دیاتیلاتر یا حلالهای قطبی دیگر بهطور کلی برای سموم قطبی استفاده میشود. این روش اصولا برای استخراج سموم غیر فرار و نیمه فرار استفاده میشود. در این روش، نمونهی آب با حجم مناسبی از حلال آلی هم زده میشود و مهاجرت ترکیبات آلی از فاز آبی به فاز آلی اتفاق میافتد. بیشتر سدیمکلرید یا نمک مناسب دیگری برای جلوگیری از ایجاد کف در زمان استخراج و افزایش کارایی فرایند به مخلوط اضافه میشود. سرانجام، حلال آلی محتوی آنالیت تحت فشار کاهش یافته تغلیظ میشود. روش استخراج مایع – مایع، روشهای مختلفی مانند استخراج مایع ناپیوسته، استخراج پیوسته و استخراج مایع – مایع مستقیم را شامل میشود [2].
2-1-1-2- روش حلال کاهش یافته
روش حلال کاهش یافته برای بیشتر ترکیبات آلی و سموم استفاده میشود. میکرو استخراج تک قطره، میکرو استخراج جریان یافته، HMF-LPME وHFM حفاظت شده از انواع روشهای حلال کاهش یافته است که برای آنالیز سموم استفاده میشود.
روشهای استخراج مینیاتوری تمام معایب روشهای استخراج مایع – مایع را برطرف کرده است. این روشها به نسبت ارزان هستند و به مقدار کمی حلال نیاز دارند. ویژگی بارز این روشها، امکان تزریق تمام حلال آلی استخراج شده، است که این امر باعث بهبود حد تشخیص میشود.
روشهای استخراج مینیاتوری تمام معایب روشهای استخراج مایع – مایع را برطرف کرده است. این روشها به نسبت ارزان هستند و به مقدار کمی حلال نیاز دارند. ویژگی بارز این روشها، امکان تزریق تمام حلال آلی استخراج شده، است که این امر باعث بهبود حد تشخیص میشود.
3-1-1-2- میکرو استخراج تک قطره
میکرو استخراج تک قطره، روش استخراج سادهای است که در آن یک قطره بهعنوان فاز استخراجی عمل میکند. حجم قطره به طور معمول 0.5 تا 2.5 میکرولیتر است. این روش، در حقیقت کوچک شدهی روش معمولی استخراج مایع – مایع است. آنالیت هدف با یک تک قطره نامحلول در آب (آلی) که از نوک میکرو سرنگ به درون نمونه غوطهور شدهاست، از بافت نمونه استخراج میشود. پس از مدت زمانی معین از آغاز استخراج، میکرو قطره مجدد به درون سرنگ کشیده شده و برای آنالیز به دستگاه آنالیزکننده تزریق میشود. از مزایای این روش میتوان به استخراج و تغلیظ همزمان و حجم بسیار اندک حلال اشاره کرد. مهمترین مشکل در این روش، عدم پایداری قطره در سر سرنگ است که به کنترل شرایط (دما، سرعت هم زدن و غیره) و کمی مهارت نیاز دارد. این روش برای تعیین مواد در مقیاس بسیار اندک مناسب است [2].
4-1-1-2- روشهای بر پایه جاذب
از جمله روشهای جدیدتر برای استخراج سموم، روش گیر انداختن آنالیت روی جاذب جامد، مانند استخراج فاز جامد، میکرو استخراج فاز جامد و استخراج جذبی با میله چرخنده و میکرو استخراج فیبر توخالی پوشش داده شده با پلیمر است.
در این روشها آنالیت با استفاده از یک جاذب که روی یک بستر مناسب تثبیت شدهاست، جذب شده و از بافت نمونه جدا میشود و در آخر بعد از حذف گونههای مزاحم، با یک حلال مناسب شسته میشود. انتخاب جاذب مناسب بهگونهای که بیشترین کارایی در جذب نمونه و حداقل جذب را برای گونههای مزاحم داشتهباشد از عوامل بسیار تاثیرگذار در استخراج است. بسیاری از جاذبهای SPE، SPME و SBSE بهصورت تجاری در انواع سرنگ، کارتریج و دیسک، قابل دسترس هستند [2].
در این روشها آنالیت با استفاده از یک جاذب که روی یک بستر مناسب تثبیت شدهاست، جذب شده و از بافت نمونه جدا میشود و در آخر بعد از حذف گونههای مزاحم، با یک حلال مناسب شسته میشود. انتخاب جاذب مناسب بهگونهای که بیشترین کارایی در جذب نمونه و حداقل جذب را برای گونههای مزاحم داشتهباشد از عوامل بسیار تاثیرگذار در استخراج است. بسیاری از جاذبهای SPE، SPME و SBSE بهصورت تجاری در انواع سرنگ، کارتریج و دیسک، قابل دسترس هستند [2].
3- روشهای اندازهگیری کمّی
پس از استخراج و تغلیظ، محلول استخراج شده به دستگاه کروماتوگرافی گازی تزریق میشود تا مقادیر آن در مقایسه با یک استاندارد تعیین مقدار شود. دستگاه کروماتوگرافی گازی دارای بخشهای مختلفی است که در ادامه به اختصار شرح دادهمیشود.
1-3- ستونهای کروماتوگرافی گازی
در دستگاههای کروماتوگرافی گازی از دو نوع ستون استفاده میشود: ستونهای پر شده و ستونهای مویین. اگر چه کارهای قابل ملاحظهای در گذشته با ستونهای پر شده صورت گرفته است، ولی بهعلت کاهش راندمان کروماتوگرافی و سختی اتصال آنها به سیستمهای جرمی، کاربردشان به شدت محدود شدهاست.
1-1-3- ستونهای پر شده
یکی از شرایط مهم برای انتخاب ستون بهمنظور آنالیز باقیماندهی سموم، مقاومت حرارتی فاز ساکن است. بسیاری از فازهای ساکن، پلیمرهای سیلیکونی با استخلافهای متفاوت هستند. مجموعهای از انواع فازهای ساکن در جدول (1) نشان داده شدهاست. هنگامی که از ستونهای پر شده استفاده میشود بهتر است از جنس شیشه با طول 5.1 تا 3 متر و قطر داخلی 3 تا 6 میلیمتر باشد. اگر چه این ستونها برای جداسازی معرفهایی مانند بیفنیلهای چند کلره مناسب نیستند.
جدول ۱: فاز ساکنهای معمول استفاده شده در آنالیز باقیمانده سموم
| نام شیمیایی | نام فاز | استفاده معادل |
| 100 درصد متیل سیلیکون | OV-1 | OV-101, SE-30,SP2100, DC200, DC-11, SF-96, SE-52 |
| 95 درصد متیل سیلیکون، ٪۵ فنیل | OV-73 | |
| 94 درصد متیل سیلیکون، ۵ درصد فنیل، ۱ درصد وینیل | SE-54 | |
| 90 درصد متیل سیلیکون، ۱۰ درصد فنیل | OV-3 | |
| 80 درصد متیل سیلیکون، ۲۰ درصد فنیل | OV-7 | |
| 65 درصد متیل سیلیکون، ۳۵ درصد فنیل | OV-11 | |
| 50 درصد متیل سیلیکون، ۵۰ درصد فنیل | OV-17 | SP-2250 |
| 50 درصد متیل سیلیکون، ۵۰ درصد تریفلوروپروپیل | OV-210 | QF-1, SP-2401 |
| 75 درصد متیل سیلیکون، ۲۵ درصد سیانواتیل | OV-225 | XE-60 |
| 86 درصد متیل سیلیکون، ۱۴ درصد سیانوپروپیل فنیل | OV-1701 |
۲-۱-3- ستون مویینه
ستونهای مویین به دلیل مسیر باز جریان، ستونهای لوله باز نیز نامیده میشوند. ستون مویین مزیتهای زیادی نسبت به ستونهای پر شده دارد. برای مثال، ستونهای مویینه دارای قدرت تفکیک بالاتر، زمان آنالیز کوتاهتر، تخریب کمتر و آلوده شدن کمتر ستون است. بسیاری از ترکیبات که در ستون پر شده با هم تداخل دارند را میتوان بهراحتی روی ستون مویینه کارآمدتر، از هم جدا کرد [4].
3-1-3- ستون مویینه سیلیکای جوش خورده
در مراحل اولیهی استفاده از این روش، اولین ستونهای مویین به کار رفته از جنس مواد پلاستیکی (نایلون و تایگون) و فلز (آلومینیوم، نیکل، مس، طلا، و فولاد ضد زنگ ) ساخته شدهبودند. ستونهای پلاستیکی دارای محدودیت دماییاند. ستونهای مویینه سخت و انعطافپذیر که از جنس فولاد ضد زنگ هستند بهطور وسیع و گسترده در آنالیز مواد نفتی مورد استفاده قرار گرفتند. سطح فعال فلزی ستونهای مویینه سبب شد که آنالیز ترکیبات قطبی و گونههای حساس کاتالیستی با این گونه ستونها مطلوب نباشد. با گذشت زمان، با مطالعه و درک شیمی سطح شیشه، مویینههای ساخته شده از شیشههای بور سیلیکات و سودالیم محبوبیت زیادی پیدا کردند و جایگزین مویینههای فلزی شدند. جداسازی روی ستونهای مویینهی شیشهای نسبت به مویینهی فلزی بسیار بهتر است. یکی از معایب این ستونها، شکنندگی آنها است. مهمترین پیشرفت در زمینه ستونهای مویینه مربوط به سال ۱۹۷۹ بود که شرکت هولت-پاکارد اولین ستون مویینه از جنس سیلیکای جوش خورده را ارائه نمود. ستونهای ساخته شده از سیلیکای جوشخورده دارای ویژگی انعطافپذیری فولاد ضد زنگ بوده و از بیاثری سطح داخلی شیشه نیز برخوردار است. بدین ترتیب، سیلیکای جوش خورده بهعنوان ماده انتخابی در تولید ستونهای مویین به سرعت جایگزین شیشه شد. ورود ستونهای مویینه از جنس سیلیکای جوشخورده، تاثیر چشمگیری بر کروماتوگرافی گازی داشته است [4].
4-1-3- انتخاب ستون مویینه
همه ستونهای مویین که در بیشتر کارهای تحقیقاتی بهمنظور اندازهگیری باقیماندهی سموم استفاده شدند شامل سیلیکون با استخلافهای مختلف هستند. تعدادی از ستونهای عمومی استفاده شده در جدول (۲) نشان داده شدهاست [۱].
جدول ۲:انواع ستون موئینه
| کارخانه سازنده | ۱۰۰ درصد متیل | ۵ درصد فنیل | 20 درصد فنیل | ۳۵ درصد فنیل | ۵۰ درصد فنیل | ۱۴ درصد سیانوپروپیل |
| ohio valley | OV-l, OV-101 | OV-73 | OV-7 | OV-II | OV-17 | OV-1701 |
| alltech | RSL-IOO, RSL-150 | RSL-200 | RSL-300 | RSL-1701 | ||
| chrompac | CPSIL5CB | CPSILRCB | CPSIL 19CB | |||
| H.P | HP-I, ULTRA-I | HP-2, ULTRA-2 | HP-17 | |||
| J&W | DB-I | DB-5 | DB-60B” | DB-17 | DB-170l | |
| Nordion | OV-I | SE-54 | OV-17 | OV-1701 | ||
| Quadrex | 007-1 | 007-2 | 007-7 | 007-11 | 007-17 | 007-1701 |
| Rcstek | Rtx-1 | Rtx-5 | Rtx-20 | Rtx-35 | Rtx-17 | Rtx-1701 |
| SGE | BP-1 | BP-5 | ||||
| Supelco | SPB-1 | SPB-5 | SPB-20 | SPB-35 | SPB-2250, SP-2100 | |
| Other names | SE-30, SE-33 | SE-54, SE-52 |
5-1-3- طول ستون، قطر داخلی و ضخامت
ستونهای سیلیسی در اندازههای مختلفی عرضه میشوند. بهطور معمول قطر داخلی ستون 0.2، 0.25 و 0.32 میلیمتر و ضخامت پوشش داخلی 0.25 میکرومتر بوده و همچنین طول این ستونها بهصورت معمول 15، 30 و 60 متر است. ثابت شدهاست که ستونهای سیلیکای جوش خورده که دارای قطر داخلی 0.2 میلیمتر تا 0.35 میلیمتر و طول بین 10 تا 60 متر باشند به دلیل قابلیت جداسازی، طول عمر و خواص مکانیکی مطلوب، ستونهای مناسبی برای تعیین سموم و آفتکشها هستند [۱].
۲-3- انتخاب آشکارساز برای اندازهگیری سموم با کروماتوگرافی گازی
آنالیز باقیماندهی سموم بر حساسیت و انتخابپذیری آشکارساز کروماتوگرافی گازی متکی است. باقیماندهی سموم در مواد غذایی بسیار اندک است. اگر چه در فرایند آمادهسازی مقدار ترکیبات هماستخراج تا حد زیادی کاهش مییابد اما با این وجود همچنان مقادیری از ترکیبات آلی از بافت نمونه در محلول نهایی وجود دارد.
چهار آشکارساز متداول بهمنظور آنالیز باقیمانده سموم شامل: ربایش الکترون، نورسنج شعلهای، یونیزاسیون شعلهای قلیایی، گرمایونی نیتروژن – فسفر (NPD) است [۱].
وقتی آفتکشها شامل عناصر شیمیایی مختلف باشند از آشکارسازی که به هر یک از عناصر پاسخ بهتری بدهد، استفاده میشود. شناساگر ربایش الکترون که توسط لاولاک (1960) و لاولاک و لیپسکی در سال 1961 معرفی شد، اولین آشکارساز انتخابی با حساسیت بالا برای ترکیبات هالوژنه است. در اواسط سال 1960 با اختراع آشکارساز یونیزاسیون شعلهای قلیایی و آشکارساز نورسنج شعلهای امکان تشخیص انتخابی سموم ارگانوفسفره و ترکیبات حاوی نیتروژن با حساسیت بالا فراهم شد. ترکیبی از قدرت جداسازی GC با آشکارسازهای حساس انتخابی، این روش را به ابزاری مهم برای آنالیز باقیماندهی آفتکشها تبدیل میکند [4].
ﺗﺸﺨﻴﺺ و ﺗﻌﻴﻴﻦ ﻣﻘﺪار ﺳﻤﻮم ﻣﺘﻌﺪد ﺑﺎ اﻧﻮاع روشهاي ﻛﺮوﻣـــﺎﺗﻮﮔﺮاﻓﻲ ﮔـــﺎزی با آشکارسازهای ECD، NPD، FPD، اﺳﭙﻜﺘﺮوﻣﺘﺮي ﺟﺮﻣﻲ ﺳﺎده ﻳﺎ ﻣﺘﻮاﻟﻲ ﺑﺎ آﺷﻜﺎرﺳﺎزﻫﺎي ﻳـﻮﻧﺶ اﻟﻜﺘﺮونی و ﺷـﻴﻤﻴﺎﻳﻲ، روش پیگیری گزینش متوالی (GC/MS/MS) انجام شدهاست.
چهار آشکارساز متداول بهمنظور آنالیز باقیمانده سموم شامل: ربایش الکترون، نورسنج شعلهای، یونیزاسیون شعلهای قلیایی، گرمایونی نیتروژن – فسفر (NPD) است [۱].
وقتی آفتکشها شامل عناصر شیمیایی مختلف باشند از آشکارسازی که به هر یک از عناصر پاسخ بهتری بدهد، استفاده میشود. شناساگر ربایش الکترون که توسط لاولاک (1960) و لاولاک و لیپسکی در سال 1961 معرفی شد، اولین آشکارساز انتخابی با حساسیت بالا برای ترکیبات هالوژنه است. در اواسط سال 1960 با اختراع آشکارساز یونیزاسیون شعلهای قلیایی و آشکارساز نورسنج شعلهای امکان تشخیص انتخابی سموم ارگانوفسفره و ترکیبات حاوی نیتروژن با حساسیت بالا فراهم شد. ترکیبی از قدرت جداسازی GC با آشکارسازهای حساس انتخابی، این روش را به ابزاری مهم برای آنالیز باقیماندهی آفتکشها تبدیل میکند [4].
ﺗﺸﺨﻴﺺ و ﺗﻌﻴﻴﻦ ﻣﻘﺪار ﺳﻤﻮم ﻣﺘﻌﺪد ﺑﺎ اﻧﻮاع روشهاي ﻛﺮوﻣـــﺎﺗﻮﮔﺮاﻓﻲ ﮔـــﺎزی با آشکارسازهای ECD، NPD، FPD، اﺳﭙﻜﺘﺮوﻣﺘﺮي ﺟﺮﻣﻲ ﺳﺎده ﻳﺎ ﻣﺘﻮاﻟﻲ ﺑﺎ آﺷﻜﺎرﺳﺎزﻫﺎي ﻳـﻮﻧﺶ اﻟﻜﺘﺮونی و ﺷـﻴﻤﻴﺎﻳﻲ، روش پیگیری گزینش متوالی (GC/MS/MS) انجام شدهاست.
1-2-3- آشکارساز ربایش الکترون
امروزه یکی از مشهورترین و شاید دومین آشکارساز در کروماتوگرافی گازی بعد از آشکارساز یونیزاسیون شعله، آشکارساز ربایش الکترون است. این آشکارساز از یک منبع رادیواکتیو با انتشار ذرهی بتا بهعنوان منبع الکترون برای انجام یونیزاسیون بهره میبرد. برخورد الکترونها به جریان گاز حامل، جریان ثابتی را بهوجود میآورد که حضور ترکیبی با قابلیت جذب الکترون (ترکیبات هالوژندار) باعث کاهش آن و ظهور یک پیک منفی میشود [۱].
۲-۲-3- آشکارساز نورسنج شعلهای
حساسترین آشکارساز برای ترکیبات فسفردار و گوگرددار، آشکارساز نورسنج شعلهای است. FPD براساس لومینسانس شیمیایی تولید شده از عنصر خاص وقتی که در شعله هیدروژن میسوزد، است. اگر چه آشکارساز نورسنج شعلهای میتواند به ترکیباتی که دارای هالوژن، نیتروژن، قلع، کروم، سلنیوم، تلور و بور هستند نیز با تغییر شرایط شعله، قدرت پاسخگویی داشته باشد، ولی بهصورت عمده برای مشاهده گونههای آلی گوگرددار و فسفردار که بهطور معمول این آشکارساز برای آنها انتخابی هستند، استفاده میشود [۱].
3-۲-3- آشکارساز یونیزاسیون شعله قلیایی
در سال ۱۹۶۴، کارمن و گایفرید نشان دادند که با اضافه کردن نمک سدیم به آشکارساز FID انتخابپذیری این آشکارساز به ترکیبات فسفردار و هالوژندار افزایش پیدا میکند. این آشکارساز برای مولکولهای دارای نیتروژن و فسفر اختصاصی اما انتخابگری آن ضعیف است [۱].
4-۲-3- آشکارساز گرما یونی نیتروژن – فسفر
آشکارساز ترمویونی به آشکارساز نیتروژن – فسفر نیز مشهور است. اساس کار این آشکار ساز به این صورت است که آند فلزی، یونهای مثبت را وقتی در یک گاز گرم میشوند، منتشر میکند. بهصورت معمول این نوع آشکارساز انتخابی بوده و برای ترکیباتی که دارای نیتروژن و فسفر هستند به کار میروند. این ترکیبات شامل مواد دارویی، سموم و آلایندههای زیست محیطی هستند [۱].
5-۲-3- آشکارساز طیفسنج جرمی
1-5-2-3- جفت شدن کروماتوگرافی گازی با طیفسنج جرمی
دستگاههای GC-MS به دلیل انتخابپذیری بالای ذاتی و حساسیت بسیار خوب، از ابزارهای قدرتمند موجود برای آنالیز باقیمانده آفتکشها بهشمار میروند.
وقتی مولکولی با الکترونی که دارای انرژی خاص است بمباران شود الگوی شکست آن نشاندهندهی ساختار مولکولی منحصر به فرد آن مولکول در یک طیف جرمی است که بیشتر بهعنوان اثر انگشت از این ماده در نظر گرفته میشود.
وقتی مولکولی با الکترونی که دارای انرژی خاص است بمباران شود الگوی شکست آن نشاندهندهی ساختار مولکولی منحصر به فرد آن مولکول در یک طیف جرمی است که بیشتر بهعنوان اثر انگشت از این ماده در نظر گرفته میشود.
1-1-5-2-3- روش پایش
طیفسنج جرمی بهعنوان آشکارساز، قادر به انجام آنالیز روی نمونهها با دو روش است. در روش اسکن، آنالیز نمونه در تمام دامنه جرمی انتخاب شده، انجام میگیرد. طیف پس زمینه را میتوان از طیف نمونه کم و طیف اصلاح را میتوان برای مقایسه مستقیم با طیف جرمی در یک کتابخانه مورد استفاده قرار داد [۱].
2-1-5-2-3- روش مانیتورینگ یون انتخابی
در مواردی که غلظت سموم خیلی کم، در محدوده پیکوگرم بر حسب میزان تزریق باشد، از روش مانیتورینگ یون انتخابی استفاده میشود که در آن جریان یونی جهت جرم انتخابی اعمال میشود. بهمنظور تایید لازم است که حداقل سه یون اندازهگیری شود. روش مانیتورینگ یون انتخابی برای تایید نتایج به دست آمده با دیگر آشکارسازهای انتخابی مناسب است [۱].
4- آنالیزهای تاییدی
1-4- تایید با استفاده از ستونهای با قطبیتهای مختلف
آنالیز تاییدی با استفاده از یک ستون با قطبیت متفاوت با ستون قبلی با روش مشابه انجام میشود. زمان بازداری یکسان از ترکیب شاهد و ترکیب ناشناخته در دو ستون مویینه با قطبیت متفاوت به منزلهی شاهدی قوی از یکسان بودن ترکیبات است [۱].
2-4- تایید به روش مشتقسازی
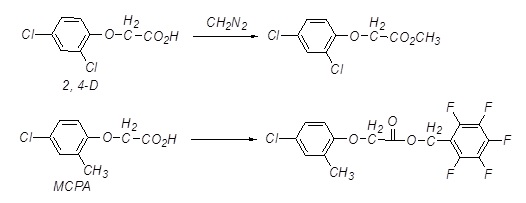
مشتقسازی شیمیایی و آنالیز آن با دستگاه کروماتوگرافی گازی/ طیفسنج جرمی غالبا با بهبود پیکها همراه بودهاست. همچنین پایداری حرارتی و فراریت بیشتر ترکیبات مشتقسازی شده، میتواند باعث افزایش حساسیت و کاهش حد تشخیص شود. مشهورترین شکل مشتقسازی، جابهجایی اتمهای هیدروژن فعال در مولکول (-OH, –COOH, -NH2, NHR, -SH) با گروه تریمتیلسیلیل است. همچنین واکنش دیآزومتانها با اسیدهای کربوکسیلیک منجر به تشکیل متیلاسترهای مربوطه شده و یا با فنلها، متیلاسترهای آروماتیک را بوجود میآورند. در این روش علاوه بر اینکه مشتق فرارتری بدست میآید، میتواند روشی برای اثبات وجود ترکیبات باشد. به مثالی از مشتقسازی چند نمونه سم برای نشان دادن روش مشتقسازی در شکل (۱) اشاره شدهاست [۱].
5- شبکه آزمایشگاهی فناوری راهبردی
این مقاله از مجموعه مقالات فصل نامه شبکه آزمایشگاهی فناوریهای راهبردی سال 2017، شماره 19 برگرفته شده است. برای دسترسی به مراکز خدمات دهنده GC بر روی لینک زیر کلیک کنید [5].
| نام دستگاه |
| کروماتوگراف گازی |
6- نتیجهگیری
آفتکشها بهطور گسترده در تولید مواد غذایی استفاده میشوند. در آنالیز مواد غذایی برای اندازهگیری و شناسایی طیف وسیعی از سموم بهخصوص سمومی که به مقدار خیلی کم در مواد غذایی وجود دارند، نیاز به روشهای جداسازی است که در این مقاله به بررسی روشهای آمادهسازی نمونه شامل جداسازی، استخراج و تصفیه پرداختیم. پس از استخراج و پیش تغلیظ لازم است محلول استخراج شده به دستگاه کروماتوگرافی گازی تزریق شود تا مقادیر آن در مقایسه با یک استاندارد تعیین مقدار شود. دستگاه کروماتوگرافی گازی مورد استفاده دارای بخشهای مختلفی است که بهطور مختصر ویژگیهایی که باید بخشهای مختلف دستگاه به منظور آنالیز باقیمانده سموم داشته باشد در این مقاله شرح داده شدهاست.
منابـــع و مراجــــع
۱ – Gordon M.H, Principlesapplications of gas chromatography in food analysis. Book Ellis Horwood Series in Food ScienceTechnology, 1990.
۲ – Pawliszyn J, Handbook of Solid Phase Microextraction. University of Waterloo Waterloo, Ontario Canada, 2012.
۳ – Wilson, Ian D.; Adlard, Edward R.; Cooke, Michael; et al., eds. Encyclopedia of separation science. San Diego: Academic Press, 2000.
۴ – ۱۳۹۵ ،رویکرد جدید در کروماتوگرافی گازی،.کامران عشقی و پرویز سلیمانی دینانی
۵ – فصل نامه شبکه آزمایشگاهی فناوریهای راهبردی سال 2017 و شماره 19





