اصول و کلیات سنتز نانوذرات با استفاده از روش پلی اُل
این مقاله شامل سرفصلهای زیر است:
1- مقدمه
2- خصوصیات و مزایای سنتز نانوذرات با استفاده از پلیاُلها
3- سنتز نانوذرات با استفاده از فرایند پلیاُل
4- نتیجهگیری
1- مقدمه
سنتز به روش پلیاُل یکی از روشهای سنتز نانوذرات است که مبتنی بر فاز مایع بوده و با استفاده از الکلهای چندظرفیتی (الکلهایی که بیش از یک بنیان الکلی دارند) با نقطه جوش بالا انجام میگیرد. خانواده پلیاُل با ترکیب اتیلنگلیکول (به عنوان سادهترین عضو) شروع شده و به دو دسته اصلی تشکیل میشوند:
الف) پلیاُلهایی که با تکرار واحدهای اتیلنگلیکول ایجاد میشوند، مانند دیاتیلنگلیکول (DEG)، تری اتیلنگلیکول (TrEG)، تترااتیلنگلیکول (TEG) و به همین ترتیب تا پلیاتیلنگلیکول (PEG) که در ساختار خود بیش از 2000 واحد اتیلنگلیکول دارد.
ب) پلیاُلهایی که با افزایش طول زنجیره کربنی (نسبت به اتیلنگلیکول) ایجاد میشوند، مانند پروپاندیاُل، بوتاندیاُل و غیره. ترکیباتی مانند گلیسرول (Gly) و ترکیباتی با چند بنیان الکلی نیز در این گروه جای میگیرند.
از میان خانواده بزرگ پلیاُلها، اتیلنگلیکول، دیاتیلنگلیکول، گلیسرول و بوتاندیاُل بیشترین کاربرد را برای سنتز نانوذرات مختلف دارند. ساختار شیمیایی چند نمونه از پلیاُلهای متداول در شکل 1 نشان داده شده است.
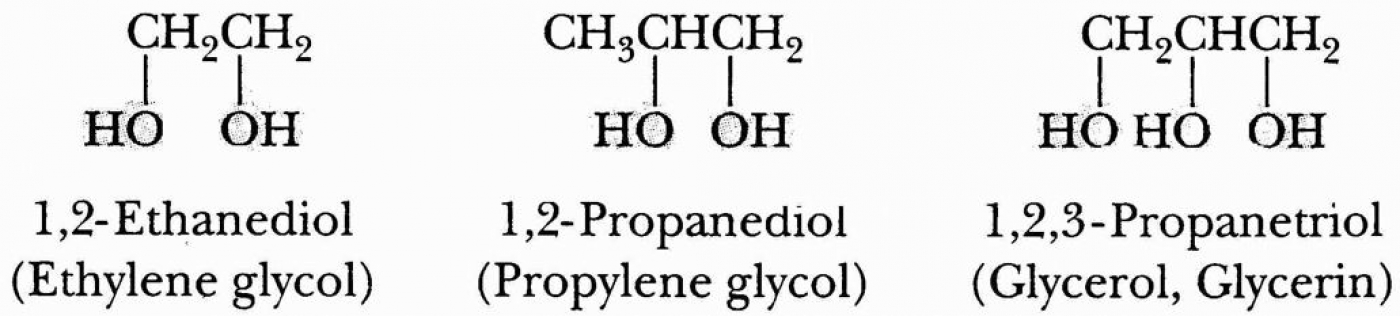
پلیاُلها علاوه بر سنتز نانوذرات، کاربردهای دیگری از قبیل استفاده به عنوان حلال، کاربرد به عنوان عامل آبزدا [Dewatering Agent]، خنککننده و انتقالدهنده حرارت، نرمکننده [Plasticiser]، افزودنیهای غذایی، صنایع دارویی، ماده اولیه تولید پلیمر و غیره نیز دارد. پلیاُلها موادی غیرسمی، زیستتخریبپذیر و زیستسازگار هستند. برخی از آنها دارای تأییدیه سازمان غذا و داروی آمریکا [US Food and Drug Administration; FDA] بوده و برخی از آنها نیز به عنوان حلال سبز شناخته میشوند.
در سال 1989 یک دانشمند فرانسوی به نام فیوِت برای اولین بار از پلیاُلها برای سنتز ذرات کوچک استفاده کرد و از آن پس عبارات ”فرایند پلیاُل“ یا ”سنتز پلیاُل“ مرسوم شد. این فرآیند با سنتز ذرات فلزی مانند کبالت، نیکل، مس و پلاتین آغاز شد و به دیگر فلزات، ترکیبات بینفلزی و آلیاژهایی مانند CoxCu1-x، FeNi و FeCoNi تعمیم یافت. در سالهای ابتدایی، اندازه ذرات فلزی سنتزشده در حدود 0/5 تا 5 میکرومتر بود و از نظر یکنواختی، اندازه و شکل کیفیت بسیار بالایی داشت و در عین حال میزان کلوخهایشدن آنها نیز بسیار کم بود. تمامی این موارد در کنار هم باعث توسعه روزافزون این روش سنتزی شد، به طوری که این روش به یک روش مقبول و پرکاربرد در سنتز نانوذرات مختلف تبدیل شد. طی دو دهه اخیر، تحقیقات فراوانی در این حوزه صورت گرفته است و تعداد مقالات چاپشده در حوزه سنتز پلیاُل از کمتر از 100 مقاله در سال 2000 به بیش از 1000 مقاله در سال 2014 رسیده است.

عامل دما دارای تأثیر بسیار مهمی در فرایند سنتز و تعیین مشخصات محصولات حاصل از روش پلیاُل است؛ زیرا سرعت واکنش معمولا ًپایین بوده و نیاز به اعمال شرایط ویژهای دارد. میتوان تأثیر دما را از سه دیدگاه مختلف مورد بررسی قرار داد: (1) تأثیر دما بر پتانسیل کاهش اتیلنگلیکول، (2) تأثیر دما بر شکستن پیوندهای شیمیایی و تشکیل پیوندهای جدید و (3) تأثیر دما بر پدیده نفوذ. این فاکتورها سبب ایجاد تنوع در نحوه تأمین حرارت مورد نیاز واکنش شده و نتایج منحصربهفردی به وجود میآورد. میتوان انرژی مورد نیاز برای گرمکردن محلول طی روش پلیاُل را توسط حرارتدهی معمولی، تابش لیزر، امواج آلتراسونیک و امواج مایکروویو تأمین کرد. اخیراً استفاده از امواج مایکروویو به منظور حرارتدهی محلول در روش پلیاُل بسیار مورد توجه قرار گرفته است. این روشها اغلب به روشهای فعالسازی دما بالا معروف هستند. روش پلیاُل در گذشته تنها به صورت حرارتدهی معمولی و امروزه بیشتر به صورت حرارتدهی توسط امواج مایکروویو مورد استفاده قرار میگیرد. فرآیند احیا توسط تابش مایکروویو نسبت به روشهای معمولی با سرعت بیشتر و طی انتقال حرارت تحت مکانیزم رسانش و جابجایی انجام شده و با تبدیل انرژی تابشی به گرمایی سبب گرمشدن ماده میشود. موادی مانند آب، الکلها و گلیکولها دارای ضریب اتلاف دیالکتریک و توان احیاکنندگی بسیار مناسبی هستند. تابش مایکروویو به این محلولها در حضور سورفکتانتها (مواد فعال سطحی) سبب سنتز نانوذرات فلزات مختلفی مانند، Ru, Ni, Au, Pt, Ag, Pt و ترکیبات فلزی مانند HgS، CdS، و MoSe شده است. نانوذرات فلزی تشکیلشده درون محلول نیز امواج مایکروویو را به صورت مناسبی جذب کرده و سبب گرمشدن سریع محیط میشوند. در این حالت نشان داده شده است که استفاده از مایکروویو برای حرارتدهی محلول سبب سنتز نانوذراتی با توزیع و اندازه مناسبتر شده و تأثیر بسیار مطلوبی روی زمان و بازده سنتز میگذارد. مقایسه سنتز نانوذرات نیکل با دو روش حرارتدهی معمولی و تابش مایکروویو نشان میدهد که فرایند سنتز با حرارتدهی معمولی در دمای C°195 پس از 5 تا 17 ساعت کامل میشود، درحالی که حرارتدهی توسط امواج مایکروویو به مدت 45 دقیقه برای تکمیل فرایند کافی است.
2- خصوصیات و مزایای سنتز نانوذرات با استفاده از پلیاُلها
به طور کلی پلیاُلها از مزایای زیادی در سنتز نانوذرات برخوردارند. اولین مزیت پلیاُلهای موجود، تنوع و گستردگی زیاد آنهاست که باعث افزایش چشمگیر انعطافپذیری و تطبیقپذیری سنتزهای پلیاُل شده است. با افزایش وزن مولکولی و تعداد گروههای هیدروکسیل (-OH) پلیاُلها، نقطه جوش، قطبیت و ویسکوزیته آنها افزایش مییابد.
مهمترین مشخصه پلیاُلها آن است که از جنبههای مختلف به عنوان حلالهای همارز با آب شناخته میشوند، اما نقطه جوش بالاتری نسبت به آن دارند. پلیاُلها در انحلال ترکیبات مختلف مشابه آب عمل میکنند و به این ترتیب، میتوان از مواد اولیه ساده و ارزانقیمت (مانند هالیدها، نیتراتها و سولفاتها) در فرایندهای سنتز مختلف استفاده کرد. علاوه بر این، محصولات واکنش عموماً حلالیت پایینی در پلیاُلها (به دلیل قطبیت پایینتر آنها نسبت به آب) داشته و بهراحتی تهنشین خواهند شد. از آنجایی که قطبیت پلیاُلها بسیار کمتر از آب است، لذا ترکیبات و نمکهای با قطبیت بالا، حلالیت کمتری در آنها دارند و بهراحتی رسوب میکنند. پلیاُلها عوامل کیلیتکننده با قطبیت پایینتری نسبت به آب هستند، اما این خاصیت کیلیتکنندگی در مجموع باعث افزایش حلالیت آنها شده است، به طوری که از لحاظ حلالیت با آب قابل مقایسه هستند. در علم شیمی، عموماً ترکیباتی که با فلزات تشکیل کمپلکس میدهند، تحت عنوان لیگاند شناخته میشوند و به دستهای از لیگاندها که توانایی تشکیل کمپلکس و برهمکنش با یک فلز خاص را از طریق دو یا چند قسمت خود داشته باشند، کیلیتکننده “Chelator” یا “Chelating agent” گفته میشود. خاصیت کیلیتکنندگی پلیاُلها نقش بسیار کلیدی مهمی در کنترل فرایندهای جوانهزنی، رشد و کلوخهایشدن نانوذرات دارد؛ زیرا پلیاُلها به سطح ذرات (بهویژه ذرات اکسیدی) چسبیده و به عنوان پایدارکننده کلوییدی عمل میکنند.
مزیت دیگر استفاده از پلیاُلها، نقطه جوش بالای آنها است و لذا میتوان سنتز نانوذرات را در دماهای C° 320-200 و بدون نیاز به فشارهای بالا یا استفاده از اتوکلاو انجام داد. استفاده از دمای بالا در سنتز نانوذرات، امکان تولید مستقیم نانوذرات بلورین در فاز مایع را ممکن میسازد و لذا نیازی به انجام فرایندهای بعدی برای افزایش بلورینگی، که باعث رشد و کلوخهایشدن آنها میشود، نیست. بلورینگی بالای نانوذرات یکی از مسائل مهم در تبیین خواص ساختاری آنها است؛ زیرا کارایی مطلوب کاتالیزورها، ترکیبات فلوئورسان، نیمهرساناها، ابررساناها و بسیاری دیگر از ترکیبات عاملدارشده، مستلزم بلورینگی بسیار بالای آنهاست.
از یک سو، استفاده از دماهای بالا برای سنتز نانوذرات با بلورینگی مناسب ضروری بوده، اما از سوی دیگر باعث کلوخهایشدن و رشد نانوذرات میشود. در اینجا، خواص کئوردیناسیونی پلیاُلها موجب عاملدارکردن سطح و پایدارکنندگی کلوییدی میشود که یکی از مزایای سنتز با استفاده از پلیاُلها به شمار میآید. منظور از پیوند کئوردیناسیونی این است که بین ذرات فلزی و پلیاُل برهمکنشها یا پیوندهایی ایجاد میشود که باعث پایداری بالای فلز میشود. به عبارت دیگر، پلیاُل با تشکیل پیوندهای کئوردیناسیونی، نه تنها به عنوان کاهنده بلکه به عنوان عامل پایدارکننده نیز ایفای نقش میکند. علاوه بر نقطه جوش پلیاُلها، تجزیه حرارتی (Thermal Decomposition) آنها نیز در تعیین حداکثر دمای مورد استفاده در فرآیند سنتز مورد توجه قرار میگیرد. پدیدههایی از قبیل آبزدایی، اکسیداسیون، کربوکسیلزدایی و همچنین پلیمریزاسیون منجر به تجزیه حرارتی پلیاُلها میشوند که معمولاً در دماهای حدود C° 50 پایینتر از نقطه جوش پلیاُل تسریع میشوند. خلوص مواد اولیه نیز فرایند تجزیه حرارتی را تحت تأثیر قرار میدهد. بنابراین، دمای مناسب برای سنتز نانوذراتی با بلورینگی و پایداری مناسب بایستی با توجه به نوع نانوذرات، پلیاُل و مواد اولیه مورد استفاده انتخاب شود. از ویژگیهای دیگر پلیاُلها میتوان به مواردی زیر اشاره کرد:
(الف) خواص احیاکنندگی پلیاُلها که سنتز مستقیم نانوذرات فلزی را ممکن میسازد؛ (ب) حذف راحت پلیاُلها از سطح نانوذرات پس از اتمام سنتز که باعث خلوص بالاتر محصول میشود و (ج) توانایی تولید انبوه و قابلیت استفاده در فرایندهای سنتز با جریان پیوسته [Continuous-Flow].
3- سنتز نانوذرات با استفاده از فرایند پلیاُل
انتشار روزافزون مقالات علمی در حوزه سنتز نانوذرات با استفاده از روش پلیاُل نشان از رشد چشمگیر و فزاینده کاربرد این روش در سنتز نانوذرات مختلف دارد. میتوان دلیل این امر را ویژگیهای منحصربهفرد و مزایای این روش نسبت به سایر روشها دانست. نانوذرات سنتزشده با این روش در سه دسته اصلی قرار میگیرند:
1. سنتز نانوذرات فلزی به روش پلیاُل.
2. سنتز نانوذرات اکسید فلزی به روش پلیاُل.
3. سنتز کالکوژنیدهای فلزی نانومتری و نانوذرات غیرفلزی به روش پلیاُل.
نانوذرات فلزی اولین ترکیبات نانومتری هستند که به روش پلیاُل سنتز شدهاند. سنتز نانوذرات فلزی به روش پلیاُل شامل دو مرحله اصلی است. در مرحله اول، یک نمک معدنی از ترکیب موردنظر در پلیاُل (به عنوان حلال) حل میشود. با وجود آنکه نمکهایی مانند استات کبالت، نیکل یا مس آبدار در اتیلنگلیکول کاملاً محلول هستند، اما در برخی موارد، ماده اولیه به مقدار کمی در پلیاُل حل میشود. در این موارد، یک ترکیب حد واسط بین ماده اولیه و محصول نهایی به وجود میآید که در واقع نیروی محرکه ادامه واکنش است. در اکثر موارد، حلالیت ماده اولیه به اندازهای است که منجر به تشکیل این ترکیب حد واسط شود. البته تشکیل ترکیب حد واسط بین ماده اولیه و محصول نهایی عمومیت زیادی ندارد و تنها در برخی از موارد مشاهده شده است. در مرحله دوم، محلول واکنش را در معرض حرارت (منابع حرارتی متداول یا امواج مایکروویو) قرار میدهند. با افزایش حرارت تا رسیدن به نقطه جوش پلیاُل، ترکیب مورد استفاده به عنوان ماده اولیه احیا شده (البته در مواردی که قدرت احیاکنندگی پلیاُل کافی نباشد، بایستی یک عامل احیاکننده نیز افزوده شود) و به صورت عنصری در میآید. در طی این مرحله، اندازه ذرات عناصر فلزی نیز در اثر فرایندهای جوانهزنی و رشد افزایش مییابد. از آنجایی که این روش یک روش سنتز پایینبهبالا است، بنابراین میزان رشد ذرات را میتوان با کنترل پارامترهایی مانند دما، زمان، غلظت مواد اولیه، ویسکوزیته، نوع پلیاُل و غیره کنترل کرده و نانوذراتی با اندازه دلخواه تولید کرد. هر چه دمای محلول در این روش بالاتر باشد، نرخ جوانهزنی بالاتر و نانوذرات با اندازه یکنواختتری ایجاد میشود. همچنین، افزایش زمان واکنش موجب افزایش اندازه ذرات میشود. از اینرو، با کنترل عوامل فوق میتوان امکان دستیابی به نانوذرات فلزی با اندازه دلخواه را فراهم کرد.
پلیاُل یکی از روشهای مناسب سنتز نانوذرات اکسید فلزی است. در این روش، نمکهای ساده فلزی مانند هیتراتها، هالیدها و استاتهای فلزی به عنوان ماده اولیه مورد استفاده قرار میگیرد. حلال پلیاُل بلافاصله جوانه ذرات تشکیلشده را از نظر اندازه و توزیع اندازه کنترل میکند. حذف پلیاُل از سطح ذرات به صورت نسبتاً سادهای انجام میشود، به این ترتیب که ابتدا با آب مورد شستشو قرار میگیرد، سپس در معرض عوامل کوئوردیناسیوندهنده قویتر مانند آمینها و کربوکسیلات قرار گرفته و نهایتاً در دمای C° 320-200 عملیات حرارتی میشود. علاوه بر دما، مدت زمان واکنش، غلظت و نوع افزودنی، میتوان با غلظت آب در دسترس نیز واکنش را کنترل کرد. وجود آب برای تشکیل اکسیدها بسیار ضروری است، به طوری که برای غلظت پایین آب از چگالش درونی پلیاُلهای تنها، برای غلظت متوسط آب از هیدراتها به عنوان ماده اولیه استفاده میشود. به طور کلی، با بزرگترشدن اندازه ذره غلظت بالایی از ماده اولیه و آب مورد نیاز است. تزریق داغ آب داغ و ماده اولیه سبب کوچکترشدن ذرات میشود. معمولاً اندازه ذره کمینه با حلالیت ترکیب محصول موردنظر در پلیاُل کنترل میشود. برای ذرات بسیار کوچک، کمپلکسهای کوئوردیناسیونی از کاتیون فلزی و پلیاُل دارای پایداری بیشتری نسبت به اکسیدهای نامحلول هستند. معمولاً، سنتز پلیاُل منجر به ایجاد سوسپانسیونهای کلوئیدی پایدار حاوی نانوذرات نسبتاً کلوخهنشده با اندازه 1 تا 200 نانومتری میشود. مواردی از مشخصات نانوذرات اکسید فلزی سنتزشده به روش پلیاُل در جدول 1 آورده شده است.
جدول 1- مثالهایی از نانوذرات اکسید فلزی سنتزشده به روش پلیاُل
| پلیاُل مورد استفاده | شکل ذرات | اندازه ذرات(nm) | اکسید فلز |
| EG,PEG | کروی | 5-25 | TiO2 |
| TrEG | کروی | 3/5 | CeO2 |
| Gly | کروی | 60 | WO3 |
| DEG | کروی | 2-20 | Fe3O4 |
| TrEG | زنجیرهای | 25-38(قطر) | |
| پنتال دیاُل | مکعبی | 90(طول ضلع) | CuO |
| EG | کره تو خالی | 50-240 | CuO2 |
| DEG | کروی | 5-20 | |
| EG | مکعبی | 150-400 | |
| EG | کروی | 2/5-6/5 | Al2O3 |
امروزه انواع مختلفی از نانوذرات اکسیدی دوتایی و سهتایی با ترکیب شیمیایی گوناگون، شکل، عناصر آلاینده و اندازه ذرات مختلف با روش پلیاُل قابل سنتز هستند. در مقایسه با سنتز نانوذرات فلزی به روش پلیاُل، اطلاعات دقیقی از نحوه کنترل شکل ذرات اکسیدی حاصل از روش پلیاُل وجود ندارد. کنترل مورفولوژی ذرات اکسیدی نیازمند بررسی اثر خاصیت اسیدی یا بازی سطوح نانوذرات روی کوئوردیناسیون چسبندگی سطح پلیاُلها و تأثیر متقابل آن روی جوانهزنی ذرات است. همچنین، علاوه بر پلیاُلها، استفاده از عوامل فعال ویژه برای کنترل دقیق شکل نانوذرات اکسیدی مورد نیاز است.
سنتز پلیاُل اکسیدهای فلزی به واسطه خواص احیاکنندگی پلیاُلها محدود شده و موجب تشکیل ذرات فلزی میشود. برای سیستمهای مشخص، امکان تهیه ذرات فلزی و همینطور اکسید فلزی تنها با تنظیم دمای واکنش وجود دارد. در حالت کلی، سنتز نانوذرات اکسید فلزی در دمای پایینتر (C° 180-100) و نانوذرات فلزی در دمای بالاتر (C° 250-180) انجام میشود.
علاوه بر نانواکسیدهای فلزی، سنتز کالکوژنیدهای فلزی نانومتری و نانوذرات غیرفلزی به روش پلیاُل به طور گستردهای صورت میگیرد. در این حالت، سولفیدهای فلزی مورد توجه قرار گرفتهاند. در سالهای اخیر، سنتز کالکوژنیدهای فلزی برای کاربردهای ویژه از قبیل سلولهای خورشیدی، فوتوکاتالیستها، ترموالکتریکها و باتریهای لیتیومی مورد استفاده قرار گرفته است.
4- نتیجهگیری
امروزه روش پلیاُل یکی از روشهای پرکاربرد در سنتز نانوذرات بوده و نانوذرات تولیدی با این روش از کیفیت بسیار بالایی از نظر ساختار، اندازه، شکل و غیره برخوردار هستند. تاکنون ترکیبات مختلفی با این روش سنتز شدهاند که عمدتاً شامل ترکیبات فلزی، اکسید فلزی و کالکوژنیدهای فلزی میشوند. اندازه ذرات تولیدی از یک نانومتر تا چندین میکرومتر متغیر است. اصلیترین دلایل توسعه روزافزون این روش عبارتند از: نقطه جوش بالا، زیستتخریبپذیری و زیستسازگاری بالا، گستردگی و انعطافپذیری بالای پلیاُلها، پایدارکنندگی نانوذرات، حذف آسان پلیاُلها بعد از اتمام واکنش، توانایی انطباق با شرایط گرمایش با امواج مایکروویو و برابری میزان انحلال ترکیبات مختلف در پلیاُلها با میزان انحلال همان ترکیبات در آب.