کاربردهای نانوالیاف در زیست پزشکی

این مقاله شامل سرفصلهای زیر است:
1- مقدمه
2- داربستهای نانولیفی
3- مواد مورد استفاده در ساخت داربستهای نانولیفی
1-3- بیوپلیمرهای طبیعی
2-3- بیوپلیمرهای مصنوعی
3-3- بیوسرامیکها
4-3- هیدروژلها
4- انواع داربستهای نانولیفی
1-4- رگهای خونی نانولیفی
2-4- داربست نانولیفی برای ترمیم بافتهای عصبی
3-4- داربست نانولیفی در ترمیم بافت استخوان
4-4- داربست نانولیفی برای ترمیم بافت غضروف
5- کاربردهای آرایشی بهداشتی نانوالیاف
نتیجهگیری
1- مقدمه
در دو دهه اخیر، دانش زیستپزشکی از رشد چشمگیری برخوردار بوده است. شاید دلیل این رشد را بتوان در سیر تاریخی تکامل علم پزشکی جستجو کرد. در عصر حاضر، پیوند اعضا از یک فرد به فرد دیگر، فراوانترین نوع جراحی ترمیمی محسوب میشود. اما این روش در کنار موفقیتهای گسترده در حوزههای درمانی میتواند منجر به مشکلاتی مانند پس زدن پیوند توسط فرد پذیرنده عضو، عفونت در سطح تماس با بافت گیرنده، و ایجاد ناهنجاریهای بیولوژیکی ناشی از پیوند شود. لذا مهندسی بافت به عنوان راه حلی مناسب برای رفع این مشکلات و مسائل ناشی از پیوند بافت توسعه یافته است.
در این روش، بافت زنده و فعال مورد نظر، با استفاده از سلولهای زنده ساخته میشود. این داربستها میتوانند طبیعی، سنتزی و یا ترکیبی از هر دو باشند. سلولهای مورد استفاده میتوانند پس از پیوند داربست به بخش آسیب دیده، به طور مستقیم به داخل آنها مهاجرت کنند یا قبل از پیوند و در محیط آزمایشگاهی در درون داربست قرار گیرند و پیوند انجام شود. در مهندسی بافت، پس از حذف بافت آسیب دیده، سلولهای مورد نیاز برای ترمیم، در داخل یک ساختار از پیش ساخته شده و مناسب برای رشد و نمو سلولها، در محل مورد نظر قرار داده میشوند. در بافتهای نرم بدن، داربست تخریب و بافت جدید جایگزین آن میشود، اما در بافتهای سخت میتوان از موادی استفاده کرد که تخریبپذیر نباشند [1]. علم زیستپزشکی در حال حاضر نیاز به استفاده از داربستهای سه بعدی نانوساختار دارد. از اینرو، نانوالیاف حاصل از فرآیند الکتروریسی بهدلیل ساختار سه بعدی، اندازه کوچکتر از میکرون، سطح ویژه بالا، ساختار متخلخل، انعطافپذیری و خواص مکانیکی مطلوب توانستهاند به عنوان یک ماده منحصربهفرد در کاربردهای زیستپزشکی مطرح شوند. در ادامه، به معرفی برخی از مهمترین مواد مورد استفاده برای ساخت نانوالیاف پرداخته خواهد شد.
2- داربستهای نانولیفی
اکثر بافتهای بدن موجودات زنده را ساختارهای نانولیفی از جنس پروتئینها تشکیل میدهند. برای مثال استخوان، عاج، دندان، غضروف و پوست از جمله این بافتها هستند. یکی از مسائل مهم در زیستپزشکی، ایجاد چارچوب سه بعدی مناسب و سازگار برای رشد سلولها به منظور ترمیم و جایگزینی بافتها است. در سالهای اخیر، توجه زیادی به ساخت چنین الگوهایی بهوسیله نانوالیاف الکتروریسی شده از جنس پلیمرهای زیستسازگار (biopolymers) شده است. چنین چارچوبهایی در زیستپزشکی به عنوان داربست نانولیفی شناخته میشوند.
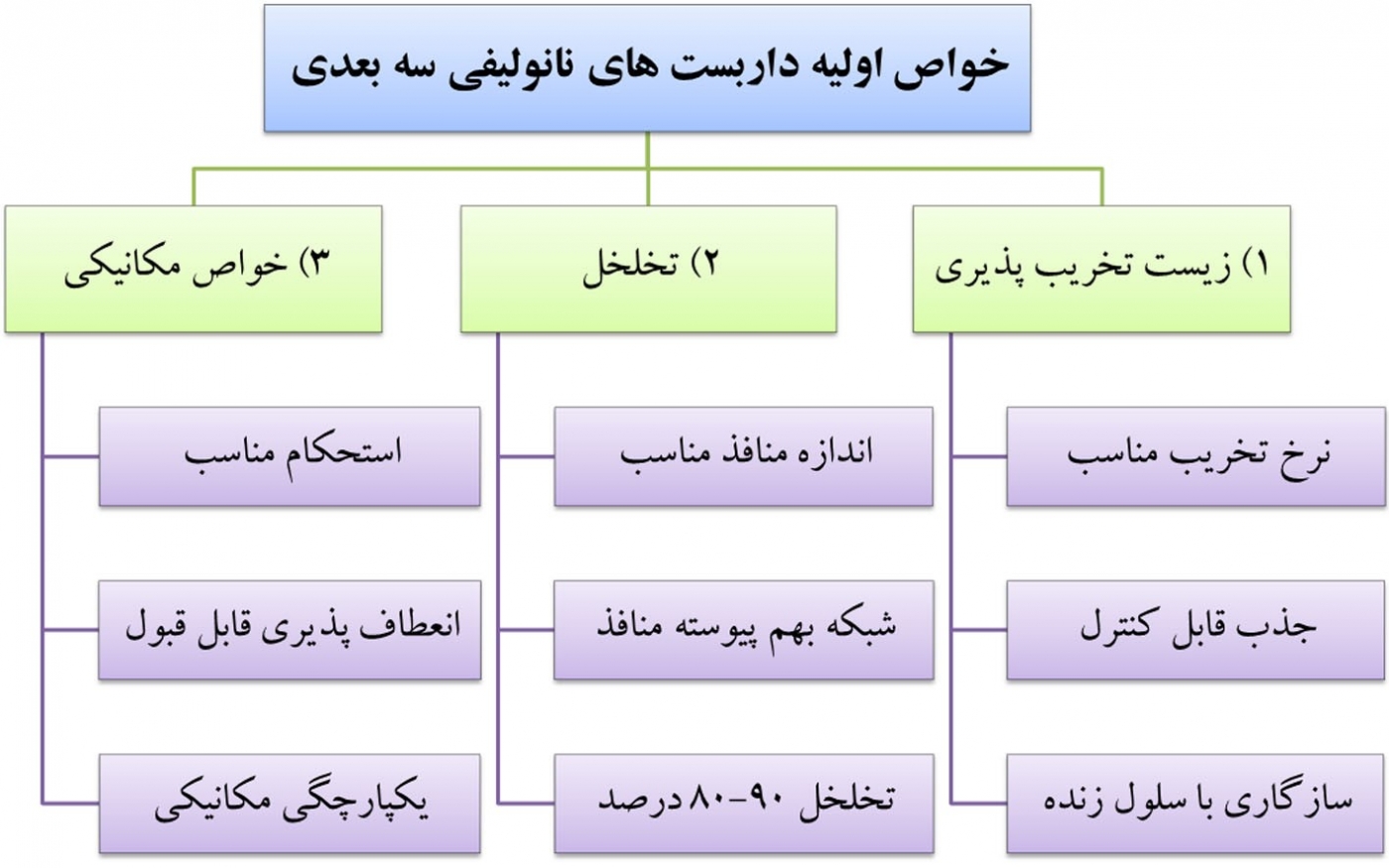
داربستهای نانولیفی باید علاوه بر فراهمسازی یک محیط سه بعدی برای اتصال و تکثیر سلولها، زمینه رشد و تبدیل آنها به یک بافت پیچیده را فراهم کنند. داربستهای نانولیفی باید دارای یک سری خواص اولیه باشند که در شکل 1 فهرست شدهاند. در واقع، یک داربست نانولیفی باید قابلیت سازگاری با سلولهای زنده را داشته باشد تا سلولها بتوانند جذب آن شده و تکثیر شوند. داربستهای نانولیفی باید از تخلخل مناسبی برخوردار باشند تا سلولها بتوانند فعالیتهای زیستی مناسبی از خود نشان دهند. داربستهای نانولیفی جانشین مناسبی برای ماتریسهای خارج سلولی طبیعی در بدن هستند [2].
معمولاً پس از ساخت بستر مناسب و ایجاد سطوح فعال برای اتصال، رشد و تکثیر سلولها، تعدادی سلول بر روی بستر قرار داده میشود. این بستر پس از انجام آزمایشات زیستسازگاری، در مجاورت بافت آسیب دیده در داخل بدن کشت داده میشود. در نهایت، بافت آسیب دیده پس از رشد و تکثیر سلولها و ایجاد ماتریس خارج سلولی در محل و ایجاد پیوند با بافتهای مجاور بستر، با گذشت زمان ترمیم میشود. مطالعات انجام شده بر روی رشد سلولها در بسترهای لیفی نشان میدهند که لایه نانولیفی علاوه بر فراهمسازی شرایط فیزیکی مناسب برای تکثیر سلولی، موجب بهبود و ارتقای بافتهای کناری در بدن میشود و دلیل آن، مشخصات توپولوژیکی خود بستر است. لایه نانولیفی با داشتن نسبت سطح به حجم و درصد تخلخل بسیار بالا، رشد سلولها را تسریع میکند و موجب بهبود و تقویت رشد بافت میشود [3].
3- مواد مورد استفاده در ساخت داربستهای نانولیفی
مواد زیستسازگاری که برای تهیه داربستهای نانولیفی مورد استفاده قرار میگیرند، به 4 دسته کلی زیر تقسیم میشوند: (الف) بیوپلیمرهای طبیعی، (ب) بیوپلیمرهای مصنوعی، (ج) سرامیکها، و (د) هیدروژلها. در ادامه به معرفی هر کدام از این مواد پرداخته میشود.
1-3- بیوپلیمرهای طبیعی
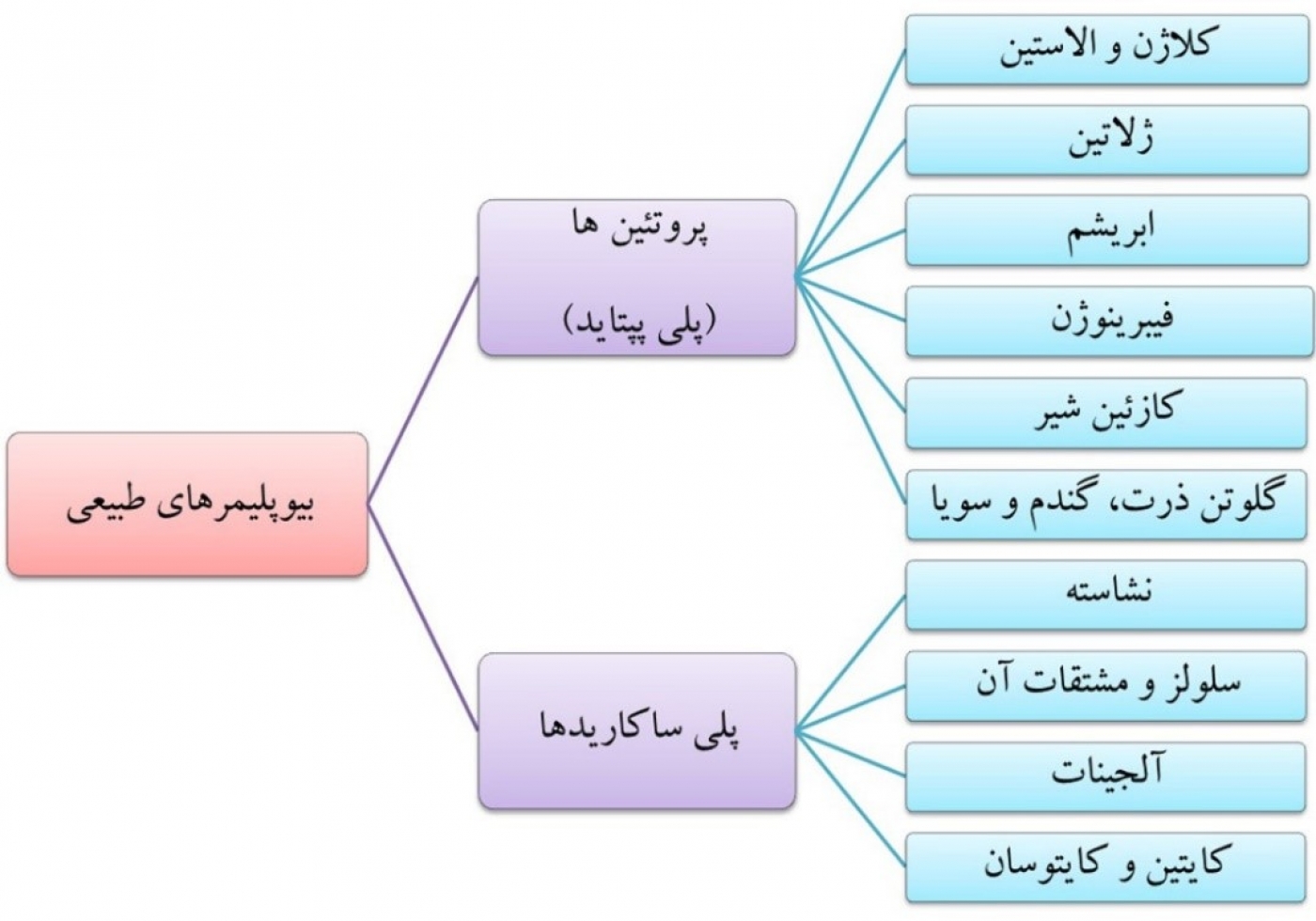
بیوپلیمرهای طبیعی (natural biopolymers) به دو دسته کلی پلیساکاریدها (حاوی مقادیر بسیار بالای گروههای هیدروکسیل) و پروتئینها (با گروههای آمیدی) تقسیم میشوند. شکل 2 دستهبندی کاملی از بیوپلیمرهای طبیعی را نشان میدهد. تاکنون بسیاری از بیوپلیمرهای طبیعی مانند ژلاتین، آلجینات، سلولز و نشاسته، به صورت موفقیتآمیز الکتروریسی شدهاند.
بیوپلیمرهای طبیعی توانایی بالایی در تحمل بارهای مکانیکی (load bearing) دارند و به دلیل اهمیت عملکردشان در انتقال نیرو و حفظ تعادل حیاتی در یک اورگانیسم، از اهمیت بسیاری برخوردار هستند. این دسته از پلیمرها زیستسازگاری را افزایش میدهند و بسیار شبیه به ماکرومولکولهای موجود در بدن انسان هستند. عیب اصلی این مواد، خواص مکانیکی نامطلوب آنها است. با این وجود، تنها برخی از بیوپلیمرهای طبیعی شامل کلاژن، الاستین، فیبرینوژن، ابریشم، کیتین و کیتوسان، قابلیت استفاده به عنوان داربستهای نانولیفی با خواص مکانیکی مطلوب را دارند. محدودیتهای موجود در تهیه و خواص مکانیکی نامناسب بیوپلیمرهای طبیعی، پژوهشگران را به سمت استفاده از بیوپلیمرهای مصنوعی هدایت کرده است [4و5].
2-3- بیوپلیمرهای مصنوعی
ساختار شیمیایی منظم و یکنواخت پلیمرهای مصنوعی، یکی از مزایای این مواد در ساخت داربستهای نانولیفی به شمار میرود. از آنجاییکه اغلب پلیمرهای مصنوعی زیستتخریبپذیر نیستند، استفاده از پلیمرهای مصنوعی در داربستهای نانولیفی با محدودیتهایی مواجه است. پلیمرهای مصنوعی مورد استفاده در داربستهای نانولیفی باید دارای سه شرط اصلی زیر باشند: (1) غیرسمی، (2) خواص مکانیکی بالا، و (3) تخریبپذیری قابل کنترل. در بین بیوپلیمرهای مصنوعی فقط بیوپلی استرها این ویژگیها را دارند.
هنگامیکه از پلیمرهای مصنوعی در داربستهای نانولیفی استفاده میشود، دمای تبدیل شیشهای شدن (Tg) و دمای ذوب (Tm) پلیمر بسیار حائز اهمیت است. اگر دمای تبدیل شیشهای شدن پلیمر نزدیک دمای بدن (37C˚) باشد، پلیمر تخریب میشود. درصورتیکه دمای تبدیل شیشهای شدن پلیمر بسیار بالاتر از این دما باشد، پلیمر تخریب نمیشود. از دیدگاه عملیاتی، اگر دمای ذوب پلیمر نزدیک دمای بدن باشد، بهدلیل نداشتن ثبات و یکپارچگی مکانیکی قابل استفاده نیست. بنابراین داربستهای زیستتخریبپذیر الکتروریسی شده عمدتاً بر پایه پلیمرهای پلیکاپرولاکتون (PCL)، پلیلاکتید (PLA)، پلی(گلایکولیک اسید) (PGA) یا کوپلیمرهای تهیه شده از آنها هستند [5و6].
3-3- بیوسرامیکها
بیوسرامیکها مواد غیرآلی حاوی کربن و سیلیکون هستند و عموماً به شکل اکسیدهای سرامیکی وجود دارند. این مواد به دلیل زیستسازگاری بالا و شباهت به ترکیبات غیرآلی طبیعی در ساختار استخوان و دندان به طور گسترده استفاده میشوند. سرامیکها ذاتاً شکنندهاند و کاربرد آنها در داربست نانولیفی برای تحمل بارگذاریهای مکانیکی (Loading) محدود است، زیرا آنها تحت بارهای فشاری نسبت به بارگذاریهای کششی رفتار مکانیکی بهتری دارند [7].
4-3- هیدروژلها
هیدروژلها، پلیمرهای آبدوست با اتصالات عرضی هستند که زیستسازگاری بسیار خوبی از خود نشان میدهند. احتمال تشکیل لخته و تخریب بافت در این مواد بسیار پایین بوده و مشخصات فیزیکی آنها شبیه به بافتهای نرم است. هیدروژلها دارای نفوذپذیری بسیار بالای اکسیژن، مواد مغذی و دیگر متابولیتهای قابل حل در آب هستند [7].
4- انواع داربستهای نانولیفی
همانطورکه اشاره شد، کلیه بافتهای بدن انسان از نظر بیولوژیکی شامل ساختارهایی از نانوالیاف هستند و بر اساس مطالعات انجام شده، داربستهای نانولیفی با توجه به خواص فیزیکی و توپولوژیکی منحصر به فرد خود میتوانند شرایط لازم برای تکثیر سلولی، بهبود و تقویت رشد بافت و ترمیم بافتهای آسیب دیده بدن انسان را فراهم کنند. در این بخش، به معرفی حوزههای کاربردی نانوالیاف پلیمری الکتروریسی شده با هدف ترمیم بافتهای بدن پرداخته خواهد شد.
1-4- رگهای خونی نانولیفی
رگهای خونی (Blood Vessels) نقش بسیار مهمی در انتقال جریان خون از قلب به داخل بافتهای بدن دارند. در حال حاضر، به دلیل اینکه اندامهای مصنوعی یا بافتهایی به ظرافت رگهای مصنوعی وجود ندارند، پزشکان مجبورند از بدن بیمار، رگی را برداشته و به محل مورد نیاز پیوند بزنند. علاوه بر اینکه این عمل بسیار وقتگیر و پیچیده است، تعداد رگهای مناسب در بدن برای برقراری پیوند نیز بسیار محدود است. لذا تلاشهای گستردهای برای توسعه بافتهایی با خواص منحصر به فرد رگ در حال انجام است. رگهای خونی ساختار لولهای شکل دارند و ترکیبی از الیاف پروتئینی آرایشیافته و سلولهای یکپارچه شامل سلولهای ظریف ماهیچه (Smooth Muscle Cells) و سلولهای اندوتلیال (Endothelial Cells) و سه لایه روزنهدار مجزا از جنس الیاف کلاژن و الاستین هستند. آرایش شعاعی فیبریلهای ماتریس فوقسلولی به موازات سلولهای جهتدار ماهیچهای، استحکام لازم و قابل قبولی را به وجود میآورند. رگهای خونی به لحاظ اندازه فیزیکی، خواص مکانیکی و بیوشیمیایی بر اساس محل و وظیفه خاصی که دارند، با یکدیگر متفاوت هستند [8].
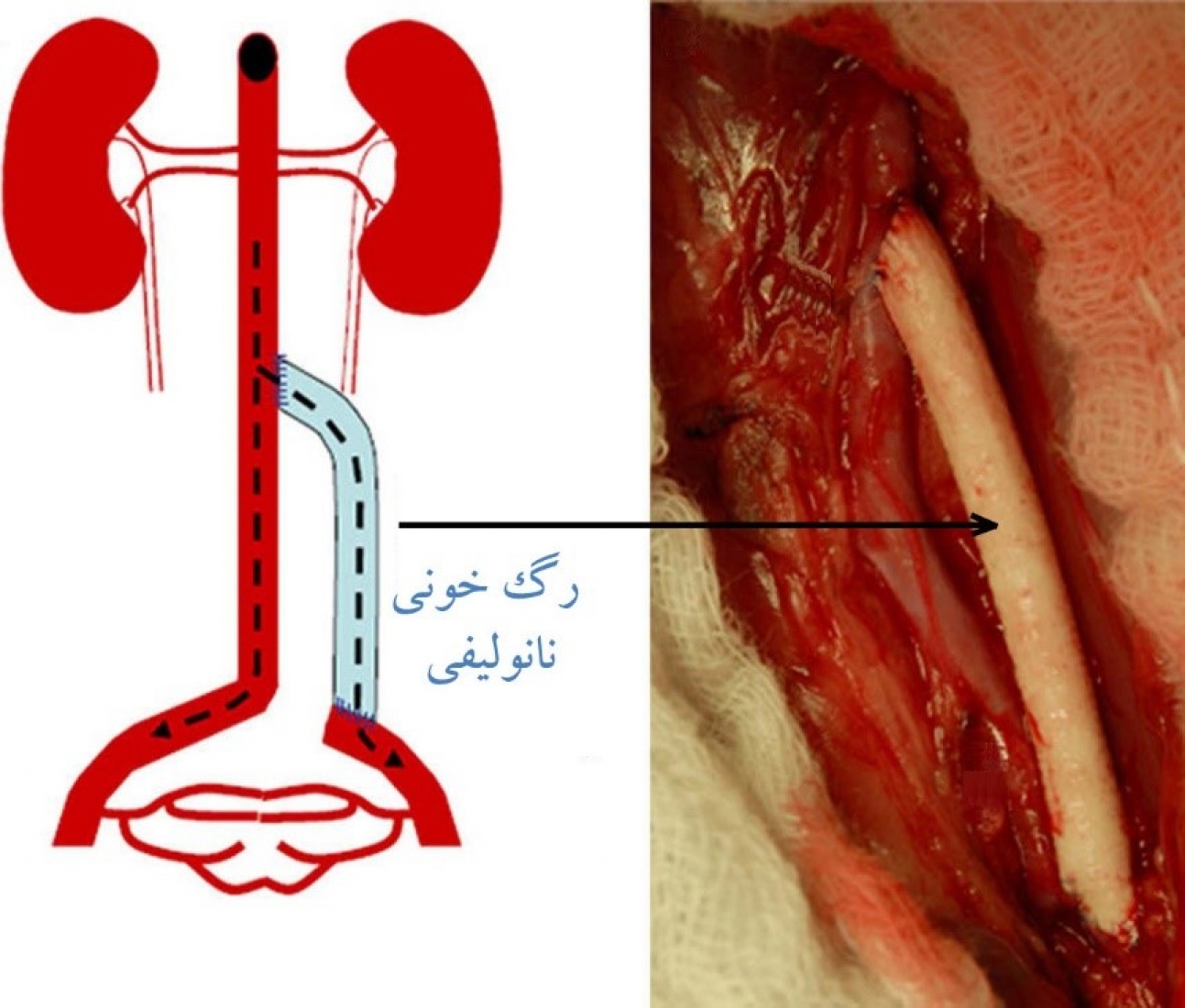
تهیه بافت رگ مصنوعی و جایگزین کردن آن با بخشهای آسیبدیده کار بسیار دشواری است؛ زیرا ممکن است سیستم ایمنی بدن، آن را به عنوان یک جسم خارجی پس بزند. در برخی از موارد نیز ممکن است لخته شدن موجب اختلال پیوند عروقی شود. لخته شدن معمولاً حاصل تکثیر سلولهای ظریف ماهیچه است و میتواند مجاری خون را مسدود کرده و در جریان خون اختلال به وجود آورد. خاستگاه لخته شدن، شکلگیری لختههای متشکل از سلولهای قرمز خون، لئوکیتها و فیبرین است که میتواند موجب آسیب دیدن دیواره رگهای خونی شود. تاکنون تحقیقات گستردهای بر روی جایگزین کردن رگهای خونی نازک (با قطر کمتر از 6 میلیمتر) و کشت سلولهای اندوتلیال روی لایههای نانوالیاف الکتروریسی شده انجام شده است. ساختمان رگهای مصنوعی میتواند از بافتهای کلاژنی یا بافتهای زیستتخریبپذیر ساخته شود. بافتهای تهیه شده از کلاژن طبیعی، خواص مکانیکی ضعیفی دارند. اکثر ماتریسهای خارج سلولی طبیعی و ساختار کلی بافتهای بدن، به ترتیب از نانوالیاف کلاژن با آرایش اتفاقی، و الیاف پلیکاپرولاکتون زیستتخریبپذیر تهیه میشوند. نانوالیاف پوشش داده شده با کلاژن، قابلیت اتصالپذیری سلولهای اندوتلیال را افزایش میدهند. از سوی دیگر، استحکام کششی بافتهای ساخته شده از نانوالیاف، با خواص مکانیکی سرخرگهای بدن انسان برابری میکند. در حال حاضر، داربست نانولیفی کلاژن/پلی کاپرولاکتون با خواص مکانیکی نزدیک به رگهای خونی و بدون ایجاد سمیت سلولی، از مرحله آزمونهای جانوری گذشته است و توانایی استفاده در آزمونهای انسانی را دارد. در شکل 3 رگ خونی نانولیفی کلاژن/پلی کاپرولاکتون پیوندی به بدن خرگوش نشان داده شده است.
2-4- داربست نانولیفی برای ترمیم بافتهای عصبی
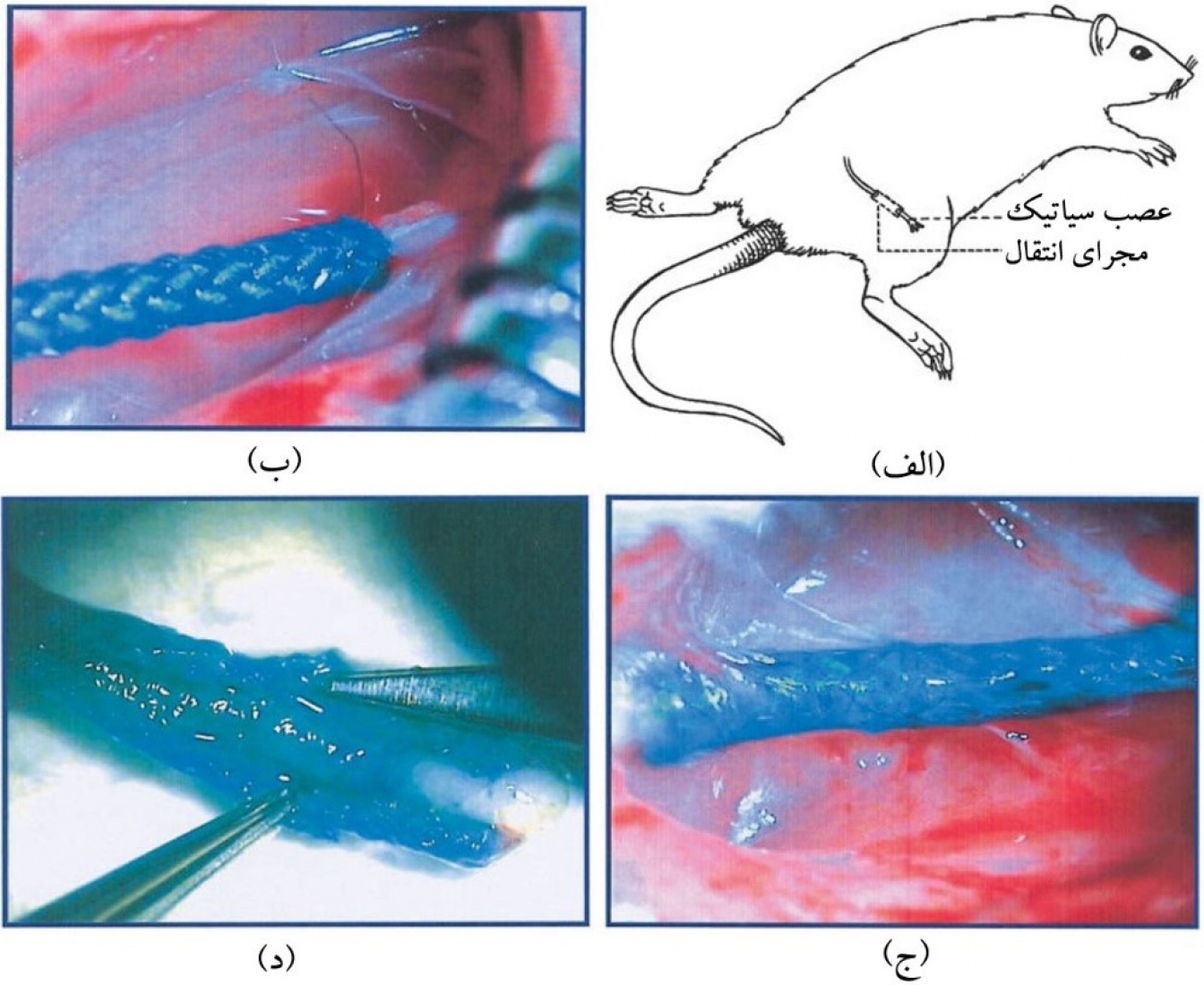
ترمیم بافت عصبی به دلیل تأثیرگذاری مستقیم در رفتار انسان بسیار حائز اهمیت است. صدمه دیدن سیستم عصبی منجر به کاهش کنترل و ناتوانی شدید بدن میشود. در صورتیکه ماتریس خارج سلولی به صورت مناسب سنتز شود، در فرآیند بازسازی و ترمیم اعصاب تأثیر بسزایی خواهد داشت. ماتریسهای خارج سلولی سیستم عصبی از کلاژنهای نوع I، II، III،IV و گلایکوپروتئینهای نانوکلاژنی و گلایکوز و گلوکز آمینو گلایکوزانها تشکیل میشوند. بنابراین یک روش مناسب برای تهیه و تولید بافت پلیمری لیفی جهت کاربرد در مهندسی بافتهای عصبی، استفاده از نانوالیاف زیست سازگار است [10]. برای نمونه، از نانوالیاف زیستتخریبپذیر پلی(لاکتید-co-گلایکولیک اسید) میتوان در عصب سیاتیک استفاده کرد. شکل 4 تصاویر این داربست نانولیفی پیوند زده شده را نشان میدهد که پس از برقراری پیوند بین کانال هدایتکننده عصبی نانولیفی با عصب سیاتیک موش، اثری از جراحت باقی نمانده است. از سوی دیگر، امروزه از داربستهای نانولیفی پلیکاپرولاکتون جهتدار و مخلوط پلیکاپرولاکتون و کلاژن، برای جایگزینی بافتهای عصبی استفاده میشود. داربستهای نانولیفی پلیکاپرولاکتون/کلاژن در مقایسه با پلیکاپرولاکتون خالص، مهاجرت سلولی و فرآیند تشکیل سلولهای عصبی را بهبود میدهد.
3-4- داربست نانولیفی در ترمیم بافت استخوان
استخوان طبیعی یک ماده کامپوزیتی است که از فاز آلی کلاژن و گلایکوپروتئینها به عنوان بستر و فاز غیرآلی هیدروکسی آپاتیت با فرمول شیمیایی Ca5(PO4)3OH به عنوان پرکننده تشکیل شده است. به بیان دقیقتر، کلاژن بیش از 90% بستر استخوان را در برگرفته است و بیش از 95% این کلاژن، از جنس فیبریلهای کلاژن نوع I به صورت نانوالیاف با قطر 50 نانومتر هستند. در واقع، استخوان نوعی غشای یکپارچه است که میتواند به عنوان مکانی مناسب برای ذخیرهسازی کلسیم و فسفات بکار رود. هدف از پژوهشهای انجام شده بر روی مواد زیستی مناسب جهت جایگزینی با استخوان، تهیه لایههای طبیعی یا سنتزی است که جایگزین غشاهای زنده بیمار میشوند. در مواد زیستی چسبندگی عامل بسیار مهمی است زیرا برای فعالیتهای سلولی مانند رشد و تکثیر ضروری است.
موادی که برای ترمیم استخوان به کار میروند معمولاً ترکیبی از پلیمرهای زیستتخریبپذیر با سرامیکهای زیستی (bioceramics) هستند. تاکنون پلیمرهای زیستتخریبپذیر مانند ابریشم، پلی کاپرولاکتون (PCL)، پلی لاکتیک اسید (PLA)، پلیگلایکولید (PGA) و پلی(لاکتیک-co-گلایکولیک اسید (PLGA) که در نخهای بخیه قابل جذب، پیچها و صفحات نگهدارنده استخوان کاربرد دارند، به عنوان جایگزینی برای بافت استخوان مورد استفاده قرار گرفتهاند. سرامیکهای زیستتخریبپذیر در جراحیهای ارتوپدی بهعنوان پرکننده در درمان شکستگی استخوان و در جراحی دندان برای پوشش قطعات فلزی جهت بهبود کاشت دندان بهکار میروند. سرامیکهای زیستی به دلیل استحکام بالای خود میتوانند استحکام جزء پلیمری را همزمان با بهبود رشد سلولهای استخوانساز تقویت کنند. «نانوالیاف پلیمری زیستتخریبپذیر کامپوزیتی شده با سرامیک زیستی» (bioceramic-reinforced biodegradable polymeric nanofibers) مانند پلیکاپرولاکتون/نانوذرات هیدروکسیآپاتیت، مناسبترین ماده کامپوزیتی برای جایگزینی استخوان پیوندی به شمار میروند [12].
4-4- داربست نانولیفی برای ترمیم بافت غضروف
غضروف (cartilage) یک بافت متراکم همبند است که تا حدی انعطافپذیر بوده و خاصیت برگشتپذیری دارد. غضروف دارای ماتریس پروتئینی درونسلولی تقویت شده و شبکههای سهبعدی از جنس فیبریلهای کلاژن و الاستین است. تخریب بافت غضروف باعث اختلالات زیادی در انسان میشود. با بهرهگیری از الکتروریسی میتوان ماتریسها و بافتهای منحصر به فردی برای غشاهای غضروفی تولید کرد. داربستهای نانولیفی برای ترمیم بافت غضروف باید چسبندگی سلولی، تکثیر، تمایز، مهاجرت، تخلخل، مقاومت کششی، فشاری و برشی بالایی داشته باشند. از اینرو، برای بازسازی غضروف، فقط از داربستهای نانولیفی متخلخل از جنس موادی مانند کیتوسان، مخلوط کیتوسان/پلی اتیلن اکسید، پلی گلایکولید (PGA)، پلیکاپرولاکتون (PCL)، پلی لاکتیک اسید (PLA)، کلاژن نوع II، اسید هالورونیک و آلجینات استفاده میشود [12].
5- کاربردهای آرایشی بهداشتی نانوالیاف
ذرات یا مایعات موجود در ماسکهای محافظتی پوست از قبیل پمادهای موضعی متداول ممکن است حین مصرف وارد نقاط حساسی از بدن مانند چشم و بینی شوند. بسیاری از این مواد به صورت اسپری مورد استفاده قرار میگیرند. برای رفع این چالش میتوان از مواد لیفی استفاده کرد. برای این منظور، از نانوالیاف پلیمری الکتروریسی شده حاوی هیدروژلها بهعنوان ماسک محافظ پوست برای درمان، ترمیم و پاکسازی پوست استفاده میشود. چنین ماسکهایی به دلیل منافذ بسیار ریز و سطح ویژه بسیار بالا، سرعت انتقال مواد به پوست و میزان مصرف آن را کنترل میکنند. همچنین به دلیل انعطافپذیری لایه نانوالیاف، این ماسکها میتوانند به راحتی بر روی بخشهای مختلف پوست قرار گیرند [1].
نتیجهگیری
در سالهای اخیر، تحقیقات بر روی کاربردهای نانوالیاف حاصل از فرآیند الکتروریسی، به دلیل ساختار خاص و منحصربه فرد این مواد روز به روز در حال افزایش است. کاربرد نانوالیاف در زیستپزشکی نیز به دلیل سطح ویژه بالا، امکان تولید ساختار سه بعدی و زیست سازگار، تخلخل بالا و خواص مکانیکی مطلوب بسیار مورد توجه قرار گرفته است. از اینرو، مقاله حاضر برخی از کاربردهای نانوالیاف در حوزه زیستپزشکی را معرفی و برخی از نمونههای کاربردی آنها برای جایگزینی با بافت استخوان، غضروف، بافتهای عصبی و عروق خونی را مورد بحث و بررسی قرار داد.