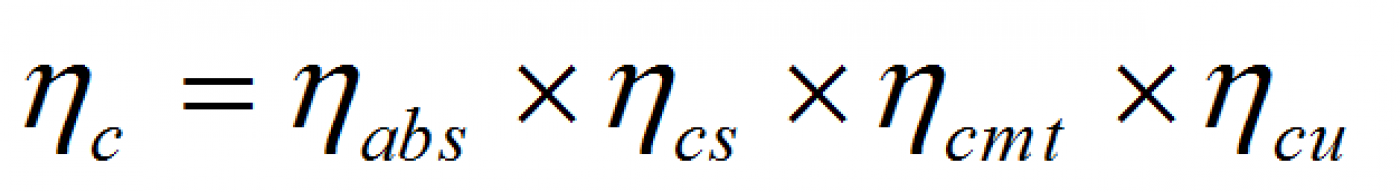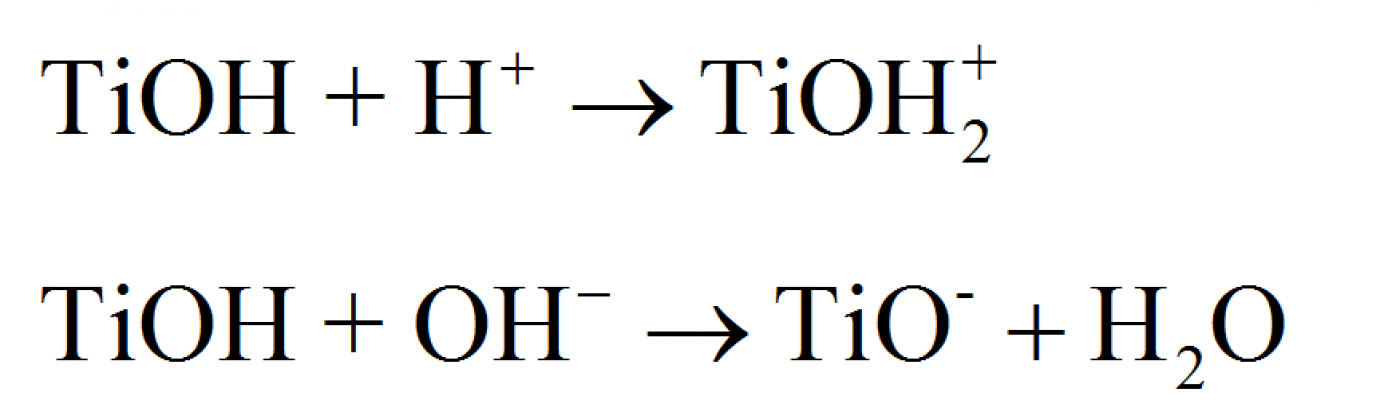کاربرد مواد فوتوکاتالیستی در تصفیه آب

این مقاله شامل سرفصلهای زیر است:
1- مقدمه
2- لازمه انجام واکنشهای فوتوکاتالیستی
1-2- لازمه انجام واکنشهای فوتوکاتالیستی از دیدگاه ترمودینامیکی
2-2- لازمه انجام واکنشهای فوتوکاتالیستی از دیدگاه سینتیکی
3- انواع مواد فوتوکاتالیست
4- عوامل مؤثر بر تخریب فوتوکاتالیستی آلایندهها در فرآیند تصفیه آب
1-4- غلظت آلاینده
2-4- غلظت ماده فوتوکاتالیست
3-4- pH محلول
4-4- اندازه و مورفولوژی ماده فوتوکاتالیست
5-4- دمای واکنش
6-4- یونهای غیرآلی
7-4- شدت نور و زمان تابشدهی منبع تابشی
8-4- اکسیژن محلول در آب
5- رآکتور فرآیندهای فوتوکاتالیستی
نتیجهگیری
1- مقدمه
فرآیند تصفیه آب را هنگامی میتوان ایدهآل و کاربردی نامید که مقرون به صرفه باشد، قابلیت حذف کامل گونههای سمی موجود در آب را داشتهباشد و حین فرآیند تصفیه، محصولات جانبی خطرناک تولید نکند. روشهای موجود برای تصفیه آب از جمله روشهای زیستی، تصفیه به کمک هوا (air stripping)، استفاده از کربن فعال گرانولی (granulated activated carbon) بهعنوان جاذب، سوزاندن (incineration) و استفاده از گاز اُزن (ozonation) معایبی دارند که کاربرد آنها را برای حذف آلایندههای سمی با محدودیت مواجه میسازند. دلیل محدودیت آنها این است که این روشها بهطور معمول گرانقیمت هستند و قابلیت تخریب تمام ترکیبات سمی را ندارند. همچنین، برخی ترکیبات مقاومت بالایی در برابر تخریب زیستی دارند. استفاده از گاز اُزن نیز تخریبی جزئی در ترکیبات سمی ایجاد میکند و همچنین محصولات جانبی سمی نیز حین فرآیند تولید میشوند. روش فوتوکاتالیستی زیرمجموعهای از فرآیندهای اکسیداسیون پیشرفته (AOPs) است که در آن آلایندههای سمی توسط تخریب نوری از بین میروند. استفاده از روش فوتوکاتالیستی در مقایسه با دیگر روشهای تصفیه آب برتریهایی دارد که از جمله آنها میتوان به مواردی چون تخریب کامل مواد شیمیایی و تبدیل آنها به گونههای شیمیایی کم ضرر CO2 و H2O، تخریب ترکیبات بسیار پایدار، عملکرد بسیار خوب در دما و فشار محیط، عدم نیاز به تزریق گاز اکسیژن، نبود آلودگی در محصول نهایی و همچنین اقتصادی و پیشرفته بودن اشاره کرد.
مواد فوتوکاتالیست بهطور عمده اکسیدهای جامد نیمهرسانا هستند که تحت تابش نور با انرژی کافی فعال میشوند. در سالهای اخیر، کاربرد مواد نیمهرسانا بهعنوان ماده فوتوکاتالیست در تخریب آلودگیهای آلی بسیار گسترش یافته است. به منظور بهبود خواص فوتوکاتالیستی، امروزه از مواد فوتوکاتالیست با اندازه ذراتی در مقیاس نانومتر استفاده میشود، زیرا خاصیت کاتالیستی ماده نه تنها به نوع ماده بلکه به اندازه ذرات آن نیز وابسته است و مواد در مقیاس نانو میتوانند رفتارهای متفاوتی در مقایسه با مواد به شکل انبوه از خود نشان دهند. افزایش خاصیت کاتالیستی ماده در مقیاس نانو را میتوان به این صورت شرح داد که با کوچک شدن ابعاد، تعداد اتمهای بیشتری در سطح قرار میگیرند و در نتیجه، نسبت سطح به حجم افزایش مییابد و بهدنبال آن خاصیت کاتالیستی ماده نیز افزایش مییابد. جهت دستیابی به خواص فوتوکاتالیستی بهینه در مقیاس نانو، اندازه بهینهای برای نانومواد وجود دارد که در صورت کمتر بودن اندازه ماده از این اندازه ایدهآل، جفتشدگی سطحی بین الکترون و حفره رخ میدهد. در این حالت، پیش از انتقال جفتهای الکترون-حفره به سطح، جفتشدگی در سطح صورت میگیرد.
در یک اتم منفرد، الکترونها سطوح انرژی گسستهای را اشغال میکنند. اما در یک بلور، سطوح انرژی بسیار نزدیک به یکدیگر هستند و نواری پیوسته از انرژی را تشکیل میدهند که هر یک از این سطوح مربوط به هر یک از اتمهای بلور است. در یک فلز (یا رسانا)، بالاترین نوار انرژی نیمهپر است و الکترونهای آن به انرژی بسیار کمی نیاز دارند تا به قسمت خالی نوار برانگیخته شوند. منشأ رسانایی الکتریکی فلزات در دمای اتاق نیز به همین دلیل است. در مواد عایق و نیمهرسانا، الکترونهای ظرفیت ماده بهطور کامل نوار را پوشش میدهند که به آن نوار ظرفیت گفته میشود. در حالی که نوار با بالاترین انرژی (نوار رسانش یا هدایت) خالی از الکترون است (حداقل در دمای صفر کلوین).
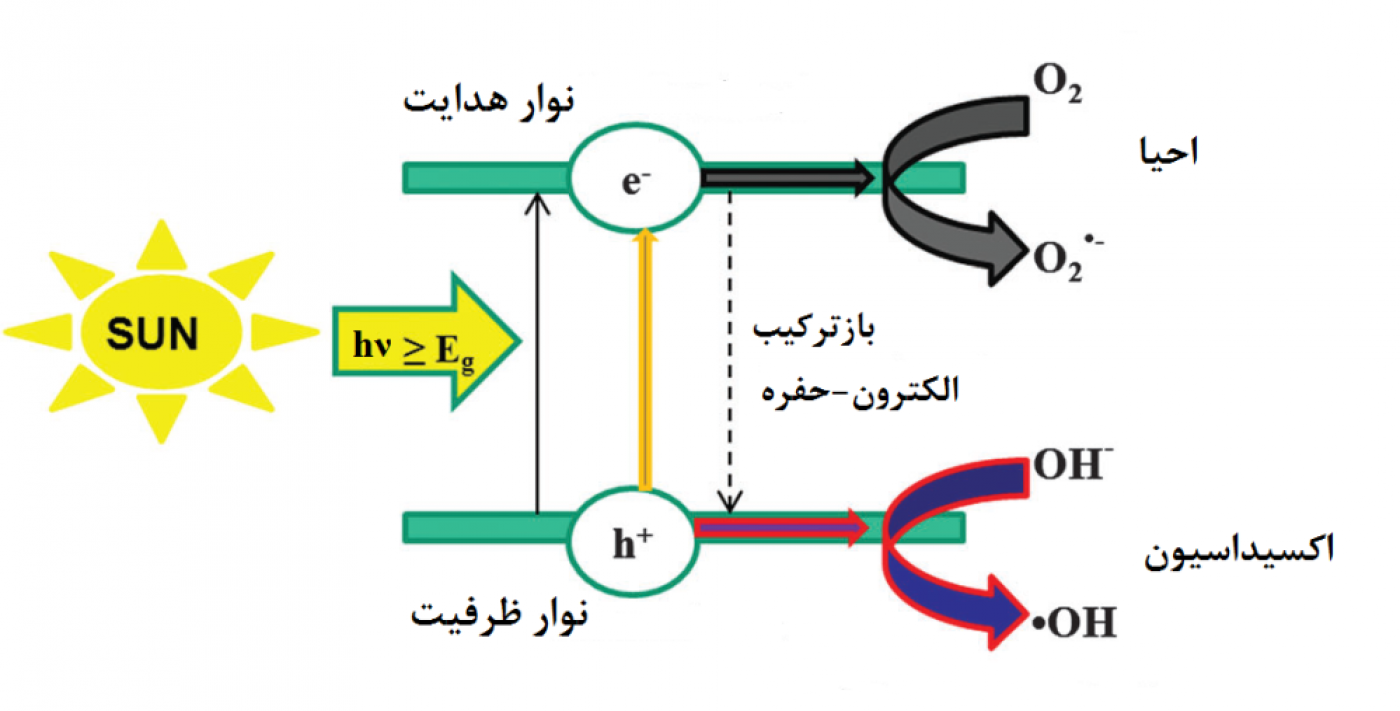
شکل 1، شمایی از سازوکار فرآیند فوتوکاتالیستی را نشان میدهد. ماده نیمهرسانا با جذب تابش موج الکترومغناطیسی با انرژی برابر یا بزرگتر از شکاف انرژی (band gap) آن برانگیخته میشود و به موجب آن الکترون از نوار ظرفیت به نوار رسانش انتقال مییابد و در نتیجه به طور همزمان یک محل خالی از الکترون (+h) در نوار ظرفیت به نام حفره ایجاد میشود. بازترکیب زوج الکترون- حفره با مسیر انتقال بار رقابت میکند. حین فرآیند بازترکیب، الکترون برانگیخته شده انرژی اضافی خود را در قالب نشر فوتونی با انرژی تقریباً برابر با شکاف انرژی نیمهرسانا آزاد میکند. این انرژی اضافی میتواند بهصورت تابش گرمایی نیز آزاد شود.
2- لازمه انجام واکنشهای فوتوکاتالیستی
1-2- لازمه انجام واکنشهای فوتوکاتالیستی از دیدگاه ترمودینامیکی
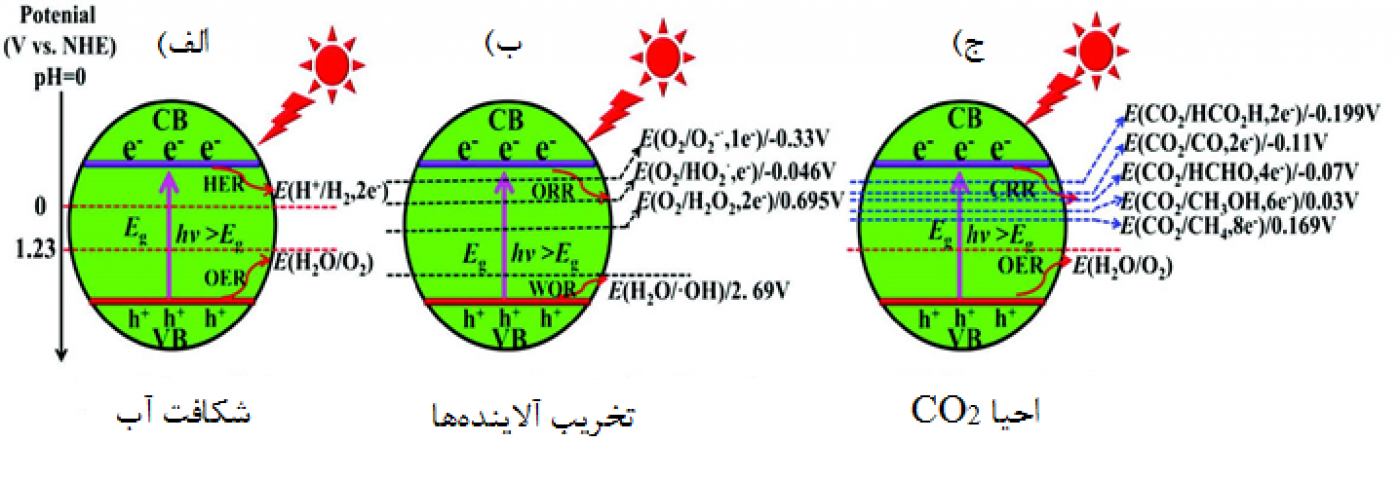
لازمه انجام سه نوع واکنش فوتوکاتالیستی مرسوم (شامل شکافت آب، تخریب آلایندهها و احیا CO2) از دیدگاه ترمودینامیکی در شکل 2 بررسی شده است. همانطوری که در شکل (2- الف) مشخص است، برای دستیابی به فرآیند شکافت آب، سطوح انرژی نوار رسانش و نوار ظرفیت نیمهرسانا بهترتیب باید منفیتر و مثبتتر از پتانسیلهای کاهش و اکسایش باشند. در شکل (2- ب)، برای تخریب آلایندهها، گونههای فعال اکسنده باید بهوسیله کاهش O2 تولید شوند. واکنش کاهش O2 یا توسط الکترونهای برانگیخته در نوار رسانش یا از طریق تشکیل رادیکالهای هیدروکسیل توسط حفرههای برانگیختهشده صورت میگیرد. باید خاطر نشان کرد که تشکیل رادیکالهای •OH حین فرآیند اکسایش حفرهها در بسیاری از نیمهرساناها با سطح انرژی نامناسب نوار ظرفیت رخ نمیدهد که این موضوع بهدلیل پتانسیل اکسیداسیون بسیار بالای آن است. بنابراین، این موضوع پذیرفته شده است که جذب و احیا O2 بهعنوان مرحله تعیینکننده سرعت واکنش، نقش مهمی را در فرآیندهای فوتوکاتالیستی مربوط به تخریب آلایندهها ایفا میکند. رادیکالهای تولید شده قادر به اکسید کردن طیف وسیعی از ترکیبات آلی و غیرآلی هستند. درحقیقت، بسیاری از ترکیبات آلی توسط رادیکال هیدروکسیل میتوانند اکسید شوند و تبدیل به گونههای CO2 و H2O شوند. بهعبارتی چنین واکنشهایی میتوانند مخرب هرگونه آلاینده آلی باشند.
بهطور مشابه برای کاهش فوتوکاتالیستی CO2 همانطوری که درشکل (2- ج) مشخص است، نوار رسانش نیمهرسانا باید منفیتر از پتانسیل واکنش موردنظر برای دستیابی به واکنش اکسیداسیون آب باشد. بهطور کلی، برای رسیدن به هر کدام یک از این ساز وکارها پتانسیل واکنشهای اکسایش و کاهش باید در محدوده سطح انرژی نوارهای ظرفیت و هدایت قرار گیرد. امکان انجام واکنش کاهش در صورتی که پتانسیل واکنش کاهش منفیتر از پتانسیل نوار رسانش باشد، وجود ندارد و همچنین امکان انجام واکنش اکسایش در حالتی که پتانسیل واکنش اکسایش مثبتتر از انرژی پتانسیل نوارظرفیت باشد، وجود ندارد. باید خاطرنشان کرد که تمامی پتانسیلهای واکنشهای اکسایش-کاهش و سطوح انرژی در نوارهای ظرفیت و رسانش وابستگی خطی به میزان pH با شیب 0.059- V دارند (به غیر از E(O2/O2–) که مستقل از مقدار pH است).
2-2- لازمه انجام واکنشهای فوتوکاتالیستی از دیدگاه سینتیکی
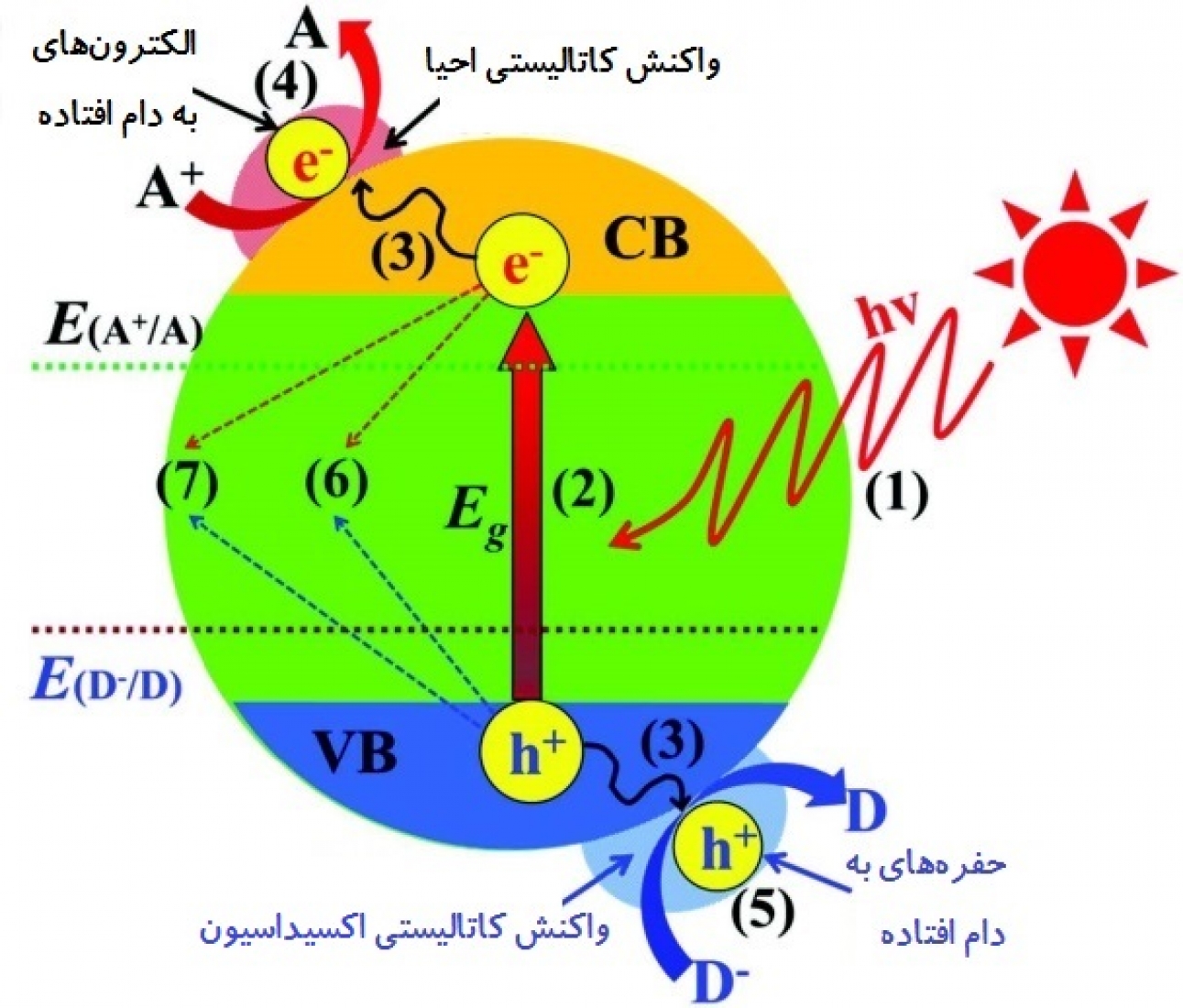
علاوه بر خواص ترمودینامیکی مناسب شامل شکاف انرژی و سطوح نوارهای ظرفیت و رسانش، عوامل سینتیکی بسیاری در دستیابی به بازده مناسب از ماده فوتوکاتالیست نقش دارند که از جمله آنها میتوان به مواردی چون میزان جذب نور، بازده جدایش/انتقال بار، سینتیک جذب/نفوذ واکنشدهندهها و دینامیک واکنش سطحی اشاره کرد. لازمه انجام واکنشهای فوتوکاتالیستی در فوتوکاتالیستهای ناهمگن از دیدگاه سینتیکی در شکل 3 آورده شده است. بهطور معمول واکنشهای فوتوکاتالیستی در فوتوکاتالیستهای ناهمگن را میتوان به 7 مرحله شامل (1) جذب نور، (2) برانگیختگی بار، (3) جدایش و انتقال بار، (4) واکنشهای احیا سطحی، (5) واکنشهای اکسیداسیون سطحی، (6) بازترکیب بار در توده ماده و (7) بازترکیب بار در سطح ماده، تقسیمبندی کرد. این 7 مرحله را نیز میتوان به سه مرحله اساسی تقسیمبندی کرد: (الف) جذب فوتونهای تابیده شده (مراحل 1 و 2)، (ب) جدایش و انتقال بار (مراحل 3، 6 و 7) و (ج) شرکت کردن بارهای سطحی در واکنشهای فوتوکاتالیستی (مراحل 4 و 5).
بازده فرآیندهای فوتوکاتالیستی را میتوان با اندازهگیری بازده فوتونی (ζ) محاسبه کرد که عبارت است از نرخ تشکیل واکنشهای نهایی فوتوکاتالیستی نسبت به شار اولیه فوتونی. به طور معمول این نسبت مقدار بسیار کمی دارد. مطالعات نشان میدهد که بیشتر زوج الکترون-حفرههای تشکیل شده (در حدود 90 درصد آنها)، پس از تشکیل به سرعت بازترکیب میشوند. این موضوع دلیل آهنگ پایین بازده فوتوکاتالیستی بیشتر واکنشهای فوتوکاتالیستی بر پایه نیمهرسانا است.
بازده کلی واکنش فوتوکاتالیستی وابسته به بازده هر یک از مراحل این واکنش است که در رابطه 1 آورده شده است.
(1)
ηc بازده تبدیل انرژی خورشید (منبع تابشی)، ηabs بازده جذب نور، ηcs بازده جدایش بار، ηcmt بازده مهاجرت و انتقال بار و ηcu بازده میزان واکنش بارهای سطحی در فرآیندهای فوتوکاتالیستی است.
3- انواع مواد فوتوکاتالیست
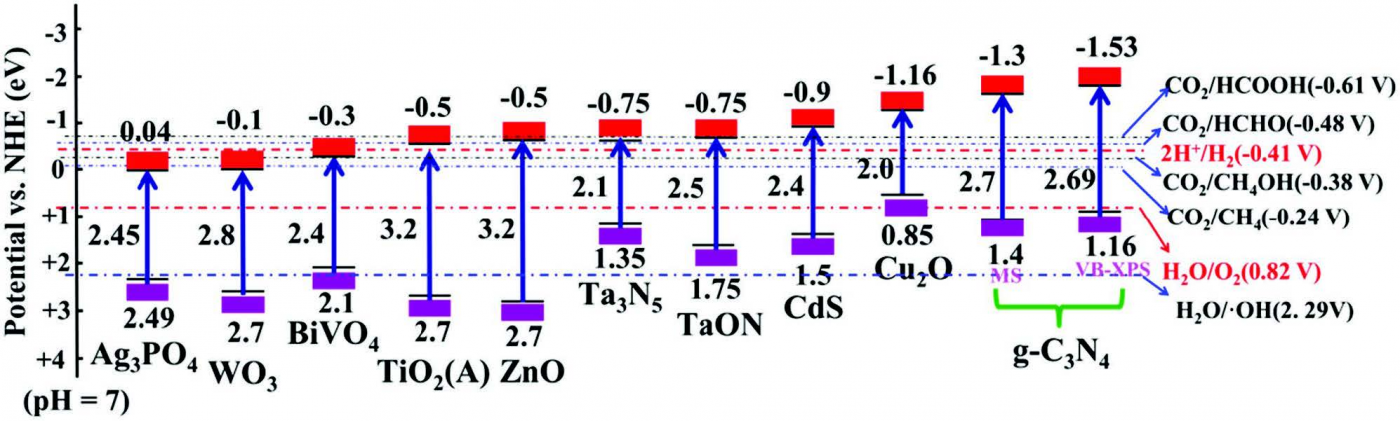
نیمهرساناهای مختلفی از جمله اکسیدهای فلزی و سولفیدها (TiO2، ZnO، Fe2O3، WO3، CdS و SnO2) بهدلیل دارا بودن خواص الکترونی منحصر به فرد میتوانند بهعنوان مواد فوتوکاتالیست عمل کنند. چنین موادی نوار ظرفیت پر و نوار رسانش خالی دارند. پتانسیل این مواد بر مبنای الکترود نرمال هیدروژن(NHE،Normal Hydrogen Electrode) در شکل 4 نشان داده شده است.
فوتوکاتالیستهای نیمهرسانا بهدلیل دربرداشتن ویژگیهای ممتازی مانند الف) ارزان قیمت بودن، ب) غیرسمی بودن یا سمیت کم داشتن، ج) قابل تغییر بودن خواص (بهعنوان نمونه میتوان خواص آنها را با کاهش اندازه، آلاییدن یا حساس کردن بهبود بخشید)، د) قابلیت شکلگیری فرآیند انتقال چندالکترونه (Multielectron transfer process) و ه) قابلیت گسترش محدوده کاربرد (بدون کاهش در فعالیت فوتوکاتالیستی) در تخریب آلایندههای آلی بسیار مورد استفاده قرار میگیرند.
مواد نیمهرسانا بخش مهمی از تحقیقات در زمینه فوتوکاتالیستهای ناهمگن را به خود اختصاص میدهند. در میان نیمهرساناهای فوتوکاتالیست اکسیدی و غیراکسیدی، TiO2 به دلیل دربرداشتن ویژگیهای ممتازی چون موقعیت مکانی مناسب نوار ظرفیت و نوار رسانش، غیرسمی بودن، پایداری شیمیایی خوب، کم هزینه بودن، قدرت اکسیدکنندگی بالا و مقاومت بسیار خوب نسبت به خوردگی نوری، فوتوکاتالیستی شاخص تحت تابش نور فرابنفش محسوب میشود. فعالیت فوتوکاتالیستی TiO2 وابستگی بسیاری به خواص فیزیکی و شیمیایی آن و به خصوص فازهای بلوری، سطح بیرونی بلور (Exposed crystal facet) و نقایص سطحی/تودهای دارد. بسیاری از فوتوکاتالیستهای نیمهرسانای مطرح شده محدودیتهایی از جمله موارد زیر را دارند:
1) شکاف انرژی بزرگ که برای برانگیختگی نوری الکترونها نیاز به پرتو فرابنفش (λ < 400 nm) وجود دارد.
2) ناپایداری در محیط مایع که منجر به تجزیه ماده فوتوکاتالیست میشود.
3) نرخ بالای بازترکیب الکترون-حفره.
نور فرابنفش تنها 5-4 درصد از طیف خورشیدی را تشکیل میدهد، در حالی که تقریباً 40 درصد از فوتونهای خورشیدی در محدوده نور مریی هستند. عیب عمده TiO2 خالص، شکاف انرژی بزرگ آن است. به این معنی که این فوتوکاتالیست تنها با فوتونهای نوری تابیده شده در ناحیه فرابنفش فعال میشود (طول موجهای کمتر از 387 نانومتر). بنابراین کارایی آن را برای کاربردهای خورشیدی با محدودیت مواجه میسازد. از اینرو برای افزایش بازده فعالیت فوتوکاتالیستی TiO2 در برابر تابش خورشیدی، نیاز به اصلاح نانوماده جهت جذب در ناحیه مریی وجود دارد. محققین بهدنبال روشهای جدیدی برای گسترش محدوده جذب TiO2 به محدوده نور مریی هستند. در راستای رسیدن به این هدف بایستی سه نکته کلیدی مورد توجه قرار گیرند: (1) مهندسی شکاف انرژی و کاهش آن به کمتر از 3 الکترون ولت، (2) پتانسیل مناسب نوارهای رسانش و ظرفیت و (3) تحرک بالای حاملهای بار درون نوارهای ظرفیت و رسانش. از جمله روشهایی که برای گسترش محدوده جذب TiO2 به ناحیه مریی به کار رفته است شامل آلاییدن با کاتیونها و آنیونها، کوپل کردن با نیمهرسانایی با شکاف انرژی کوچک، و حساس کردن به کمک رنگدانهها هستند.
4- عوامل مؤثر بر تخریب فوتوکاتالیستی آلایندهها در فرآیند تصفیه آب
عوامل مختلفی در دستیابی به تخریب نوری کارآمد تأثیرگذار هستند که از جمله آنها میتوان به غلظت آلاینده، غلظت ماده فوتوکاتالیست، pH محلول، اندازه و مورفولوژی ماده کاتالیست، دمای واکنش، یونهای غیرآلی، شدت نور و زمان تابشدهی منبع تابشی و اکسیژن محلول در آب اشاره کرد. هر یک از این موارد در ادامه به تفصیل آورده شده است.
1-4- غلظت آلاینده
میزان آلاینده جذب شده روی سطح ماده فوتوکاتالیست، تأثیر بسیار زیادی بر واکنشهای فوتوکاتالیستی دارد. تنها آلایندههایی که جذب سطح ماده فوتوکاتالیست شدهاند در واکنشهای فوتوکاتالیستی شرکت میکنند، میزان آلایندهای که بهصورت تودهای در محلول وجود دارد، نقشی در آن ندارد. غلظت اولیه آلاینده از عوامل مهم در میزان تخریب نهایی است. بهطور کلی میتوان گفت در صورت وجود غلظت ثابتی از ماده فوتوکاتالیست، با افزایش غلظت آلایندهها درصد تخریب آلایندهها کاهش مییابد. با افزایش غلظت آلایندهها، مواد آلی بیشتری جذب سطحی ماده فوتوکاتالیست میشوند، بهطوری که تعداد فوتونهای کمتری به سطح کاتالیست میرسند و بنابراین رادیکالهای کمتری تشکیل میشوند و در نهایت درصد تخریب کاهش مییابد.
2-4- غلظت ماده فوتوکاتالیست
نرخ تخریب آلایندهها وابستگی بسیار بالایی به میزان غلظت ماده فوتوکاتالیست دارد. با افزایش میزان غلظت ماده فوتوکاتالیست، آهنگ تخریب نوری آلایندهها افزایش مییابد. افزایش غلظت ماده فوتوکاتالیست، مکانهای فعال روی سطح ماده فوتوکاتالیست را افزایش میدهد و بنابراین منجر به تشکیل رادیکالهای بیشتر و در نهایت میزان تخریب بیشتر میشود. افزایش میزان غلظت ماده فوتوکاتالیست تا حدی موجب بهبود نرخ تخریب میشود، اما پس از آن محلول کدر میشود و مانع از رسیدن نور منبع تابشی به ماده فوتوکاتالیست خواهد شد که بهدنبال آن نرخ تخریب کاهش مییابد.
3-4- pH محلول
میزان pH محلول بر نرخ تخریب نوری آلایندهها بسیار تأثیرگذار است. تغییرات pH محلول، بارهای سطحی ذرات فوتوکاتالیست و همچنین پتانسیل واکنشهای کاتالیستی را تغییر میدهد و در نتیجه روی میزان جذب آلاینده روی سطح تأثیر میگذارد. بهعنوان نمونه، ذرات TiO2، همان طور که در رابطههای (2) و (3) آورده شده است، در محیط اسیدی یا قلیایی به ترتیب پروتون دریافت میکنند و از دست میدهند.
(2)
(3)
بنابراین سطح ذرات TiO2 در محیط اسیدی دارای بار مثبت و در محیط قلیایی دارای بار منفی خواهد بود. نانوذرات TiO2 در محیط اسیدی فعالیت اکسیدکنندگی بالاتری از خود نشان میدهند، اما یون اضافی +H میتواند موجب کاهش نرخ واکنش شود. در این حالت ذره TiO2 بهدلیل بار مثبت سطحی خود مانند یک اسید لوئیس قوی و آلاینده دارای بار منفی مانند پایه اسید لوییس قوی رفتار میکند و میتواند روی سطح مثبت TiO2 جذب شود. میزان جذب آلاینده به میزان اولیه و ماهیت ماده آلاینده، مساحت سطحی ماده فوتوکاتالیست و pH محلول بستگی دارد. میزان pH محلول بار سطحی ماده فوتوکاتالیست را تعیین میکند. هنگامی که pH محلول در نقطه ایزوالکتریک (نقطه دارای بار صفر، Isoelectric point) باشد، میزان جذب آلاینده به سطح ماده فوتوکاتالیست به حداقل خود میرسد. در pHهای کمتر از نقطه ایزوالکتریک سطح ماده فوتوکاتالیست TiO2 دارای بار مثبت و در pHهای بالاتر آن دارای بار منفی است.
4-4- اندازه و مورفولوژی ماده فوتوکاتالیست
از آنجا که تمام واکنشهای شیمیایی در سطح ماده فوتوکاتالیست رخ میدهند، اندازه ذره و مورفولوژی ماده فوتوکاتالیست تأثیر مستقیمی در میزان مساحت سطحی و بهدنبال آن نرخ تخریب فوتوکاتالیستی دارد. مواد نانوساختار با اندازه کریستالیت/اندازه دانه کمتر از 20 نانومتر، خواص فیزیکی بسیار متفاوتی از نوع تودهای خود نشان میدهند و بنابراین در این زمینه بسیار مورد توجه هستند. با کوچک شدن اندازه ذرات، مساحت سطحی ماده فوتوکاتالیست افزایش مییابد و قابلیت بیشتری برای جذب آلایندهها و فوتونهای بیشتر را خواهد داشت.
5-4- دمای واکنش
افزایش میزان دمای واکنش بهطور معمول موجب افزایش فعالیت فوتوکاتالیستی میشود، اما دمای واکنش بالاتر از 80 درجه سانتیگراد علاوه بر اینکه موجب افزایش میزان بازترکیب حاملهای بار میشود، مانع جذب آلایندهها روی سطح ماده فوتوکاتالیست نیز خواهد شد. دمای واکنش پایینتر از 80 درجه سانتیگراد برای جذب آلاینده روی سطح فوتوکاتالیست مطلوب است اما با کاهش بیشتر دما تا صفر درجه سانتیگراد انرژی فعالسازی واکنشهای فوتوکاتالیستی افزایش مییابد. بنابراین محدوده دمایی 80-20 درجه سانتیگراد بهعنوان محدوده دمایی مطلوب برای تخریب نوری آلایندهها در نظر گرفته میشود.
6-4- یونهای غیرآلی
انواعی از یونهای غیرآلی موجود در آب آلوده از جمله یونهای منگنز، آهن، روی، مس، فسفات، نیترات، سولفات و کلراید میتوانند روی نرخ تخریب فوتوکاتالیستی آلایندههای آلی تأثیرگذار باشند زیرا این یونها میتوانند جذب سطحی ماده فوتوکاتالیست شوند. مطالعات گوناگونی در مورد تأثیر یونهای غیرآلی بر میزان تخریب فوتوکاتالیستی آلایندهها روی سطح TiO2 انجام شده است، نتایج این مطالعات نشان میدهد برخی از کاتیونها مانند مس، آهن و فسفات اگر در غلظتهای مشخصی وجود داشته باشند، بازده تخریب نوری را کاهش میدهند، در حالی که کلسیم، منگنز و روی تأثیر کمی بر نرخ تخریب نوری دارند زیرا این کاتیونها در بیشترین میزان درجه اکسایش خود وجود دارند و نقش بازدارنده در فرآیند تخریب را ایفا نمیکنند. آنیونهای غیرآلی مانند نیترات، کلراید، کربناتها و سولفاتها فعالیت سطح ماده فوتوکاتالیست را متوقف میکنند. وجود نمکها، پایداری کلوئیدی را کم میکند، انتقال جرم را افزایش میدهد و تماس سطحی بین آلاینده و ماده فوتوکاتالیست را کاهش میدهد. یون کلر نیز رادیکال •OH را به دام میاندازد.
7-4- شدت نور و زمان تابشدهی منبع تابشی
هر دو عامل شدت نور و زمان تابش روی تخریب آلایندهها تأثیرگذار است. در شدتهای نوری پایین 20-0 (mW/cm2) ، با افزایش شدت نور، نرخ تخریب آلایندهها افزایش مییابد. در حالی که در شدتهای متوسط نور 25 (mW/cm2) نرخ تخریب وابسته به جذر شدت منبع نوری است. در شدتهای بالای منبع نوری، نرخ تخریب وابسته به شدت نوری نیست، زیرا در واکنشهایی که در شدت منبع نوری کم انجام میشود، تشکیل الکترون-حفره غالب است و میزان بازترکیب الکترون-حفره ناچیز است. از طرف دیگر، هنگامی که شدت منبع نوری افزایش مییابد، جدایش زوج الکترون- حفره با بازترکیب آنها رقابت میکند، بنابراین تأثیر کمتری بر نرخ واکنش تخریب خواهد داشت.
8-4- اکسیژن محلول در آب
اکسیژن محلول در آب در واکنشهای فوتوکاتالیستی نقش الکترونگیرنده را دارد. این گونه الکترون برانگیخته شده به نوار هدایت را به دام اندازد و از بازترکیب آن جلوگیری کند. اکسیژن محلول در آب تأثیری روی میزان جذب آلایندهها روی سطح کاتالیست TiO2 ندارد و در واقع نقش پایدارکننده رادیکالهای حد واسط را ایفا میکند.
5- رآکتور فرآیندهای فوتوکاتالیستی
انواعی از رآکتورهای فوتوکاتالیستی وجود دارد که انتخاب نوع آن بنا بر شرایط آزمایش و کاربرد آن صورت میگیرد. بهطور کلی میتوان آنها را به دو دسته تقسیمبندی کرد. در حالت اول سوسپانسیونی از ماده کاتالیست استفاده میشود و در حالت دوم لایه نازکی از ماده کاتالیست به کار میرود. رآکتورهایی که سوسپانسیونی از ماده فوتوکاتالیست را به کار میبرند نسبت به رآکتورهایی که از لایه نازک استفاده میکنند ارجحیت بیشتری دارند که بهدلیل مساحت سطحی بالا ماده فوتوکاتالیست در تماس با مواد آلاینده است. در این حالت، تعداد فوتونهای بیشتری به ماده کاتالیست برخورد میکند و منجر به ظرفیت بالای جذب میشود.
در مسیر توسعه رآکتورهای فوتوکاتالیستی کارآمد، طراحی مؤثر رآکتورها برای کاربردهای صنعتی و تجاری، چالشی بزرگ محسوب میشود. به منظور دستیابی به رآکتور تجاری کارآمد، انواعی از عوامل مؤثر در طراحی باید در نظر گرفته شوند، از جمله آنها میتوان به مواردی از جمله انتخاب منبع تابشی شامل توان خروجی، کارآیی منبع، توزیع طیفی، هندسه، ابعاد، نگهداری از تجهیزات (دورههای گرمایشی و سرمایشی) و همچنین طراحی ادوات تابشی رآکتور شامل آینهها، منعکسکنندهها و پنجرهها، مواد سازنده آنها، شکل و ابعاد لامپها و ماده فوتوکاتالیست اشاره کرد.
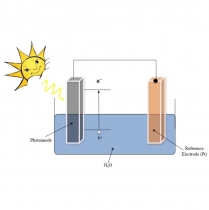
ارزیابی نور منبع تابشی و نحوه توزیع آن درون رآکتور فوتوکاتالیستی برای برونیابی نتایج آزمایشگاهی به کاربردهای در مقیاسهای بزرگ و مقایسه میزان بهرهوری در بارگذاریهای مختلف بسیار اساسی است. نمونهای از یک رآکتور فوتوکاتالیستی در شکل 5 نشان داده شده است.
نتیجه گیری
روش فوتوکاتالیستی در میان انواع روشهای فیزیکی و شیمیایی حذف آلودگیهای زیستمحیطی، روشی کارآمد و مقرون به صرفه برای پاکسازی محیطزیست و به خصوص برای تصفیه آب محسوب میشود. از آن جا که در کشورمان ایران حدود دو سوم از سال (حدود 300 روز از سال) آفتابی است، میتوان از انرژی خورشیدی بهعنوان منبع انرژی تجدیدپذیر و بینهایت در این زمینه بهره کافی را برد. برای تخریب آلایندهها به روش فوتوکاتالیستی، لازم است ابتدا ماده فوتوکاتالیست و واکنشهای آن از دو دیدگاه ترمودینامیکی و سینتیکی بررسی شوند و در صورت نیاز به بالا بردن آهنگ تخریب میتوان خواص ماده فوتوکاتالیست را به روشهای گوناگونی چون آلاییدن با عناصر دیگر، کوپل کردن با نیمهرسانا و حساس کردن با رنگدانهها بهبود بخشید. عوامل مختلفی بر در دستیابی به تخریب فوتوکاتالیستی کارآمد تأثیرگذار است که از جمله آنها میتوان به غلظت آلاینده، غلظت ماده فوتوکاتالیست، pH محلول، اندازه و مورفولوژی ماده کاتالیست، دمای واکنش، یونهای غیرآلی، شدت نور و زمان تابشدهی منبع تابشی و اکسیژن محلول در آب اشاره کرد. انواعی از رآکتورهای فوتوکاتالیستی با طراحیهای گوناگون وجود دارند که به منظور دستیابی به رآکتوری در مقیاس بزرگ و کارآمد باید عوامل گوناگونی از جمله منبع تابشی، ادوات منبع تابشی شامل لامپها، منعکسکنندهها و هندسه آنها بهینه شوند.