خواص کاتالیستی نانومواد و عوامل مؤثر بر آن

این مقاله شامل سرفصلهای زیر است:
1- مقدمه
2- بررسی خاصیت یک نانوکاتالیست
3- دلایل پیدایش رفتار کاتالیستی در نانومواد
4- عوامل موثر بر خواص کاتالیستی نانومواد
1-4- اندازه نانوذرات
2-4- نحوه توزیع نانوذرات
3-4- شکل نانوذرات
4-4- بستر تهیه نانوذرات
5-4- شرایط انجام واکنش
نتیجهگیری
1- مقدمه
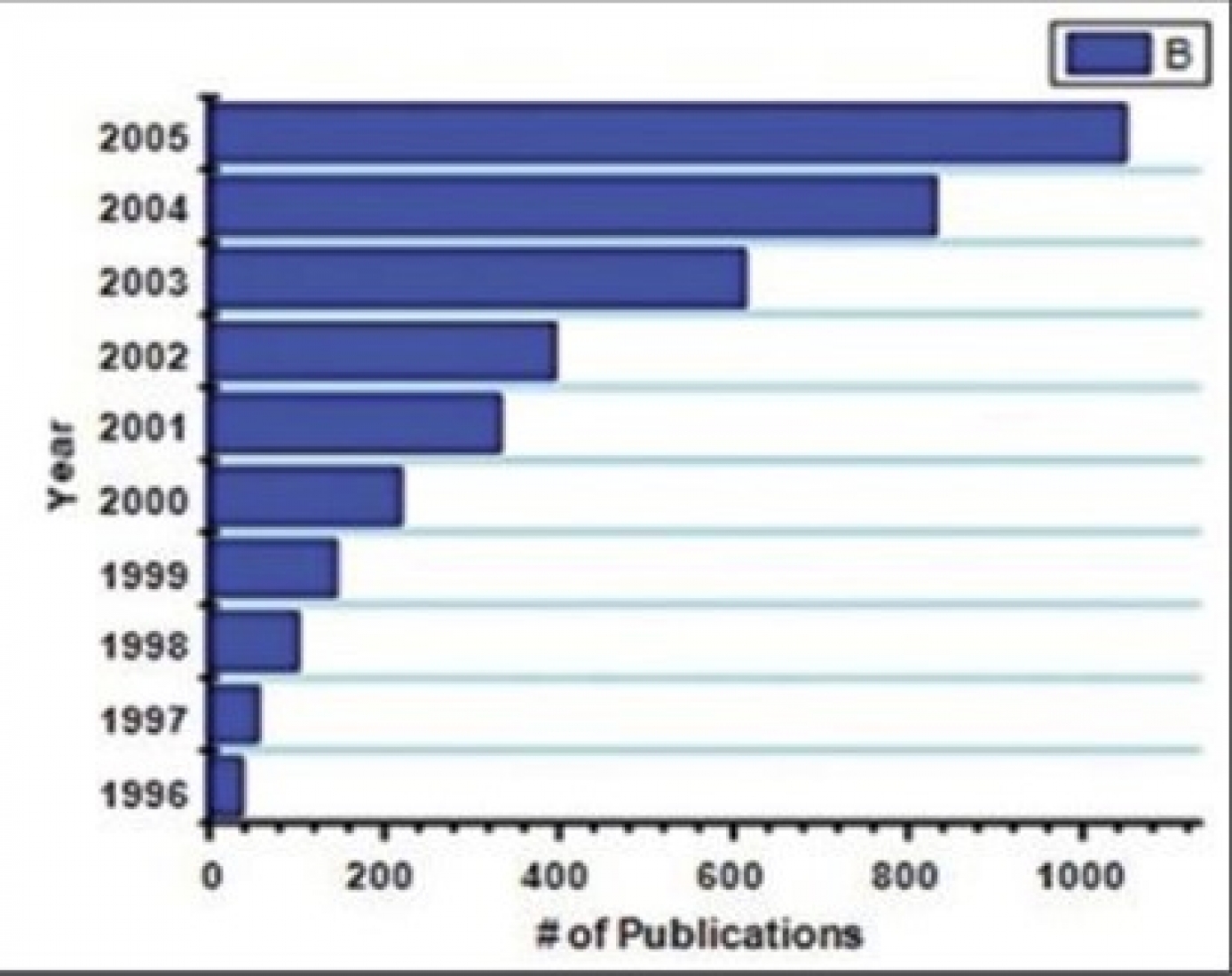
امروزه از کاتالیستها بهطور گسترده در تولید مواد شیمیایی و دارویی استفاده میشود. برای نشان دادن اهمیت این مواد، بنزین مورد استفاده در اتومبیلها، مثال خوبی است. بنزین در مسیر تبدیل از نفت خام، حداقل به ده نوع کاتالیست مختلف نیاز دارد. بسیاری از فرآوردههای دیگر نیز نیازمند استفاده از کاتالیست هستند. براساس تخمینهای انجام شده، بالای بیست درصد از تولید ناخالص ملی کشورهای صنعتی به کاتالیستها اختصاص دارد. امروزه، مهندسین فناوری نانو، تلاشهای زیادی برای وارد کردن نانومواد در تهیه کاتالیستها انجام میدهند که رویکرد موفقیتآمیزی نیز به نظر میرسد. با توجه به اهمیت نانوکاتالیستها، این مواد یکی از مهمترین حوزههای تحقیقاتی فناوری نانو (به ویژه نانوشیمی) را تشکیل میدهند و تعداد مقالات و کتابهایی که درباره آنها منتشر میشود رو به افزایش است (شکل 1را ببینید) [8]. بسیاری از واکنشهای مهم توسط نانومواد کاتالیزوری میشوند و این نانوکاتالیستها بازده تولید محصول را بهطور چشمگیری افزایش میدهند. از جمله این واکنشها میتوان به موارد زیر اشاره کرد:
· اکسیداسیون (Oxidation) مونوکسید کربن و تبدیل آن به دیاکسید کربن
· تجزیه گازهای سمی مانند دیاکسید نیتروژن (Nitrogen dioxide)
· اکسایش متانول و دیگر سوختها در پیلهای سوختی
· واکنشهای کراکینگ (Cracking) و واکنشهای هیدروژندار کردن که در صنعت پتروشیمی بسیار حائز اهمیت هستند.
هماکنون، در بسیاری از فرایندهای نفتی و شیمیایی از کاتالیستهای اقتصادی برای بهبود گزینشپذیری و کاهش ضایعات و آلودگیها استفاده میکنند. برای نمونه، واکنش هیدروژناسیون فرایندی مهم برای تولید محصولات باارزش در صنعت پتروشیمی است؛ محصولاتی که در زندگی روزمره مورد استفاده قرار میگیرند. با استفاده از این فرایند موادی با ساختار جدید و خواص شیمیایی و فیزیکی متفاوت ایجاد میشود. یکی از موارد مهم استفاده از فرایند هیدروژناسیون بهبود کیفیت بنزین از طریق هیدروژناسیون انتخابپذیر دیاولفینهای موجود در برشهای نفتی مختلف است. فرایند هیدروژناسیون گرمازا است و در غیاب کاتالیزور حتی در دمای بالا با سرعت کمی انجام میشود. استفاده از نانوکاتالیستهای حاوی نانوذرات فلزی مثل پالادیم بر روی بسترهایی مانند نانولوله کربنی سرعت انجام این واکنش را بسیار بالا میبرد. متانول بهعنوان یک سوخت مایع دارای چگالی انرژی بسیار بالایی است و میتواند از تودههای زیستی زنده تولید و بهراحتی در پیلهای سوختی متانولی مستقیم ذخیره شود و بهعنوان یک منبع انرژی در دسترس برای کاربردهای حمل و نقل مورد استفاده قرار گیرد. نانوذرات فلزی بهدلیل داشتن نسبت سطح به حجم بسیار بالا و فعالیت الکتروکاتالیستی برای اکسایش متانول بهکار گرفته میشوند، بهویژه پلاتین که ثابت شده است برای اکسایش متانول بسیار موثر است و اکسایش الکتروشیمیایی متانول را بهطور قابل توجهی تسهیل میکند. تحقیقات انجام شده نشان میدهد استفاده از پلاتین در پیلهای سوختی در اکثر مواقع ضروری و بهترین گزینه است. یکی از متداولترین روشها، استفاده از پلاتین بهصورت نانوذره به همراه بسترهایی از نانولوله کربنی (تکدیواره، چنددیواره) یا پلیمرها است [9].
2- بررسی خاصیت یک نانوکاتالیست
اصولاً زمانی که از بررسی خاصیت یک نانوکاتالیست صحبت میشود منظور این است که یا فعالیت کاتالیستی مورد بررسی قرار گرفته، یا انتخابپذیری نانوکاتالیست بررسی شده، و یا پژوهشی به منظور فهم مکانیسم عملکرد نانوکاتالیست صورت گرفته است. از بین موارد ذکرشده، بیشترین تحقیقات بر روی «فعالیت نانوکاتالیستها» صورت گرفته است. هدف تمامی این بررسیها، بهبود فعالیت کاتالیستی نانوکاتالیستها بوده است [9]
3- دلایل پیدایش رفتار کاتالیستی در نانومواد
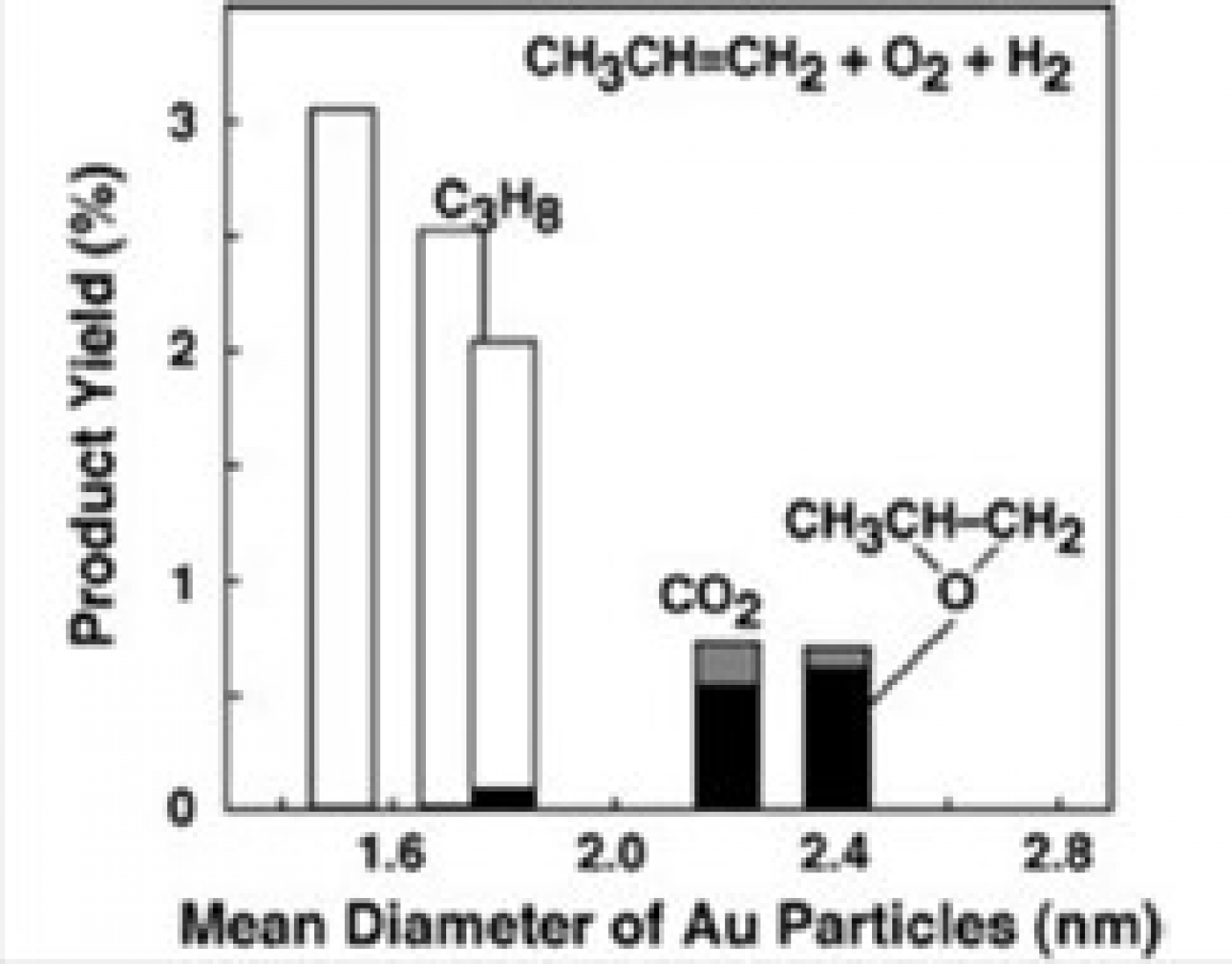
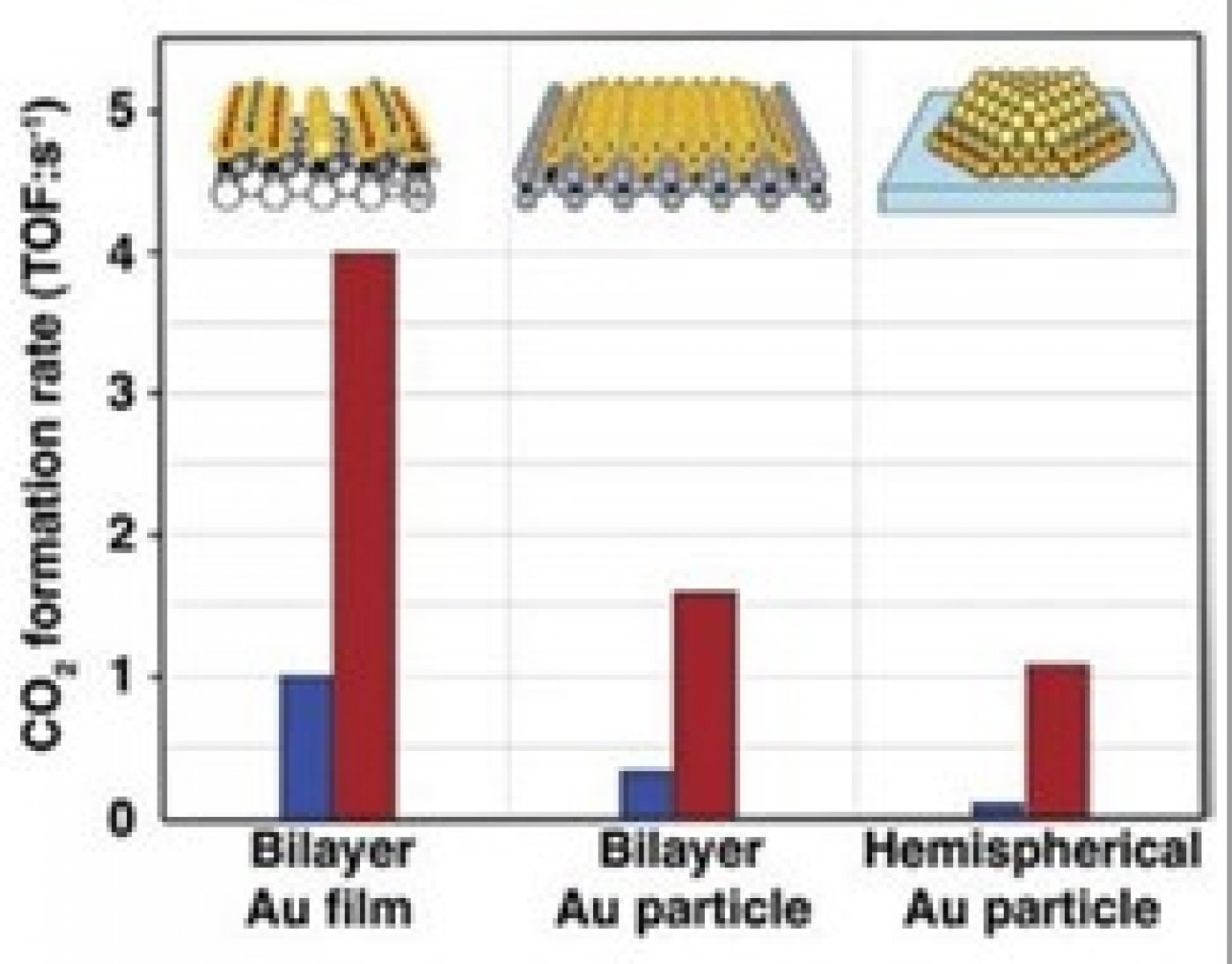
وقتی ابعاد یک ماده به مقیاس نانو کاهش مییابد، بسیاری از خواص آن دستخوش تغییر میشود؛ ویژگیهای بارزی مانند خواص الکتریکی، نوری، و مغناطیسی. پیدایش سه خصلت زیر نیز از جمله این تغییرات است: اندازه بسیار کوچک، نسبت سطح به حجم بسیار بالا، و افزایش تعداد اتمهای واقع بر روی سطح. این سه عامل اخیر، مهمترین دلایل پیدایش خاصیت کاتالیستی در نانومواد هستند [9]. اصولاً وقتی ذرات خیلی کوچک میشوند (مقیاس نانو)، بهدلیل انحنای بسیار بالایی که پیدا میکنند، دارای اتمهای زیادی روی سطح خود هستند که این اتمهای سطحی پیوند بسیار ضعیفی با اتمهای توده شبکه دارند. به همین جهت، این ذرات انرژی سطحی بسیار بالایی دارند و به شدت فعالاند و اصطلاحاً گفته میشود اتمهای سطح در حالت ناپایدار فیزیکی و فعال شیمیاییاند و مستعد برای انجام بسیاری از واکنشهای شیمیایی هستند. میتوان گفت که دلیل اصلی و تعینکننده پیدایش خاصیت کاتالیستی در نانومواد نسبت سطح به حجم بسیار بالای آنها است. به طور کلی، هر چه این نسبت بیشتر شود، بهدلیل افزایش انرژی سطحی، خاصیت کاتالیستی در نانومواد تقویت میشود. در اصل، دلیل این تغییرات به تغییر در ساختار الکترونی مواد برمیگردد که با مکانیک کوانتوم قابل توجیه است. وقتی اندازه ذرات خیلی کوچک میشود، چگالی حالات نوار ظرفیت دچار تغییر میشود و مجموعهای از ترازهای گسسته انرژی به وجود میآیند. در نتیجه، با کوچک شدن ذرات، اندازه آنها به جایی میرسد که فاصله اتمهای سطح ذرات، مضربی از طول موج الکترون میشود. در این وضعیت، میتوان ترازهای انرژی را با رفتار مکانیک کوانتومی یک ذره در یک جعبه مدلسازی کرد. این اثر را اثر اندازه کوانتومی مینامند. از آنجایی که ساختار الکترونی نانوذرات به اندازه ذره بستگی دارد، قابلیت آنها در واکنش دادن با دیگر عناصر نیز به اندازه آنها بستگی دارد [1]. این تغییرات و اثر آنها بسیار محسوس است. برای نمونه، یکی از فلزاتی که رفتار بسیار متفاوت در حال توده و مقیاس نانو دارد فلز طلا است. طلا درحالت توده دارای خاصیت کاتالیستی بسیار پایینی است و یکی از غیرفعالترین فلزات است، اما وقتی به مقیاس نانو برده میشود فعالیت کاتالیستی بسیار بالایی از خود نشان میدهد (شکل 2 را ببینید). جالب آنکه طلا یکی از متداولترین فلزات واسطهای است که در سنتز نانوکاتالیستها مورد استفاده قرار میگیرد، بهویژه در سنتز کاتالیستهایی که برای واکنش اکسیداسیون کربن مونوکسید و تبدیل آن به کربن دیاکسید استفاده میشوند (شکل 3 را ببینید) [6].
4- عوامل موثر بر خواص کاتالیستی نانومواد
عوامل موثر بر خواص کاتالیستی نانومواد عبارتاند از: (1) اندازه نانوذرات، (2) شکل نانوذرات، (3) نحوه توزیع نانوذرات، (4) بستر تهیه نانوذرات، و (5) شرایط انجام واکنش. در ادامه، به تاثیر هرکدام از این موارد پرداخته میشود.
1-4- اندازه نانوذرات
در اکثر موارد، هرچه اندازه نانوذرات کوچکتر شود، خاصیت کاتالیستی افزایش مییابد، اما در بعضی از موارد، با کاهش اندازه نانوذرات، خاصیت کاتالیستی بهبود پیدا نمیکند. برای نمونه، در واکنش اکسیداسیون کربن مونوکسید با استفاده از نانوذرات روتنیوم در بستر PVP (PolyN-vinyl-2–pyrolidone)، زمانیکه ابعاد نانوذرات روتنیوم، در حدود 6 نانومتر است، فعالیت کاتالیستی آنها هشت برابر زمانی است که اندازه آنها در محدوده 2 نانومتر قرار میگیرد [4]. به عنوان یک مثال دیگر، زمانیکه نانوذرات طلا با ابعاد کمتر از 5 نانومتر مورد استفاده قرار گیرند، بیشترین فعالیت و انتخابپذیری را از خود نشان میدهند [2]. نانوذرات فلزات واسطه میتوانند اندازههایی در حدود کمتر از 1-100 نانومتر داشته باشند، اما بیشترین فعالیت کاتالیستی آنها زمانی مشاهده میشود که اندازهشان در حدود 1-10 نانومتر باشد.
2-4- نحوه توزیع نانوذرات
نحوه توزیع مکانی نانوذرات نیز میتواند بر خاصیت کاتالیستی آنها اثرگذار باشد. هر قدر توزیع مکانی نانوذرات گستردهتر شود، خاصیت کاتالیستی آنها افزایش مییابد زیرا در این حالت، تعداد اتمهای سطحی بیشتری در دسترس واکنش قرار میگیرند (به شکل ۳ مراجعه کنید). در مقابل، ثابت شده است که هرچه توزیع اندازه نانوذرات باریکتر باشد فعالیت کاتالیستی آنها بهبود مییابد.
3-4- شکل نانوذرات
همانطور که قبلاً گفته شد، زمانی که ذرات در مقیاس نانو هستند، انحنای بیشتری داشته و اتمهای سطحی آنها ناپایدارترند. این اثر به ویژه در ذرات غیرکروی بیشتر نمود پیدا میکند؛ ذراتی که مانند چهاروجهی، هشتوجهی، و مکعبی دارای مکانهای لبهای و گوشهای زیادی هستند. در این حالت، نانومواد به دلیل افزایش نسبت سطح به حجم، خاصیت کاتالیستی بیشتری از خود نشان میدهند. در سنتز نانوذرات کلوییدی به روش برادلی (متداولترین روش سنتز نانوذرات کلوییدی)، با کنترل نسبت غلظت نانوذره به پایدارکننده یا بکارگیری احیاکنندههای متفاوت بسته به نوع واکنش میتوان شکل مورد نظر را سنتز کرد [9].
4-4- بستر تهیه نانوذرات
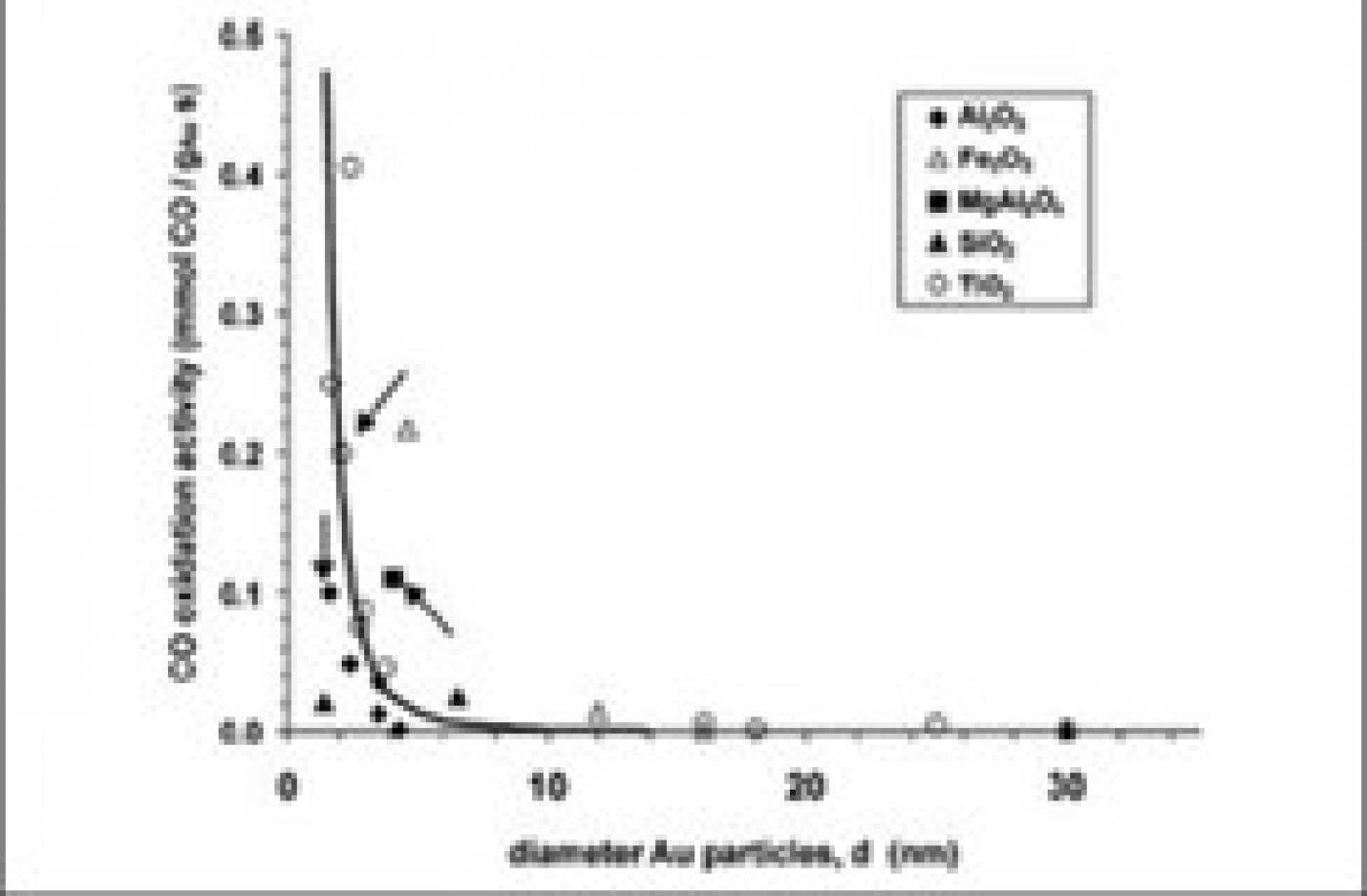
مواد در مقیاس نانو دارای انرژی سطحی بسیار بالایی هستند و تمایل دارند به یکدیگر بچسبند. در اکثر موارد، نانوذرات بر روی یک بستر به روشهای مختلف نشانده شده و سپس در واکنش بکار گرفته میشوند. دلیل این کار این است که بستر از تجمع پیدا کردن نانوذرات و اصطلاحاً کلوخهای شدن آنها جلوگیری میکند، زیرا وقتی نانوذرات تجمع پیدا کنند از حالت نانو بودن خارج میشوند. بستر از طریق برهمکنشهای الکترواستاتیک و فضایی، نانوذرات را در سطح خود به دام میاندازند، انرژی سطحی آنها را کاهش میدهند، مانع تجمع آنها میشوند، و پایداری آنها را بهبود میدهند. اثری که بستر بر روی خاصیت کاتالیستی نانوذرات میگذارد برای نانومواد مختلف متفاوت است و روند خاصی ندارد و بسته به نوع نانوماده و نوع بستر بهکاررفته، خاصیت کاتالیستی میتواند افزایش یا کاهش یابد (شکل 4) [9]. مطالعات نشان میدهند که هرگاه از لیگاند بهعنوان بستر در تهیه نانوکاتالیستها استفاده میشود، در بیشتر موارد، خاصیت کاتالیستی کاهش پیدا میکند [5] و زمانی که از پلیمرها بهعنوان بستر استفاده میشود، در اکثر موارد، خاصیت کاتالیستی افزایش مییابد. بسترهای مختلفی مانند پلیمرها، دندریمرها، اکسیدهای فلزی، و نانولولههای کربنی، و بعضی از لیگاندها، برای تهیه نانومواد مورد استفاده قرار میگیرند، اما بسترهای پلیمری از بقیه متداولترند. براساس نتایج به دست آمده، تشکیل نانوذرات بر روی بسترهای پلیمری، امکان کنترل نانوذرات را فراهم میکند، میتوان حالت نانوذرات را روی سطح تعیین کرد، و در اکثر موارد باعث افزایش خاصیت کاتالیستی نانومواد میشود. در بین بسترهای پلیمری، PVP متداولترین بستری است که مورد استفاده قرار میگیرد و یک پلیمر ارزانقیمت و خطی است که نانوذرات بهطور یکنواخت روی آن پخش میشوند [9].
5-4- شرایط انجام واکنش
شرایط انجام واکنش نیز بر روی راندمان کاتالیست موثر است. برای نمونه، اگر واکنش هک (Heck) (واکنش بین یک آریل هالید با یک آلیل) بین یدو بنزن و پلیمر استایرن توسط نانوذرات پالادیم در بستر پلیونییل پایرولیدون Pt-PVP یک بار در شرایط گرمادهی معمولی و یک بار با استفاده از امواج ماکروویو انجام شود، فعالیت کاتالیستی و انتخابپذیری ماده در حضور امواج ماکروویو نسبت به شرایط معمولی (رفلاکس) بهمراتب بیشتر خواهد بود. دلیل این امر این است که نانوذرات پالادیم امواج ماکروویو را جذب میکنند و با جذب این امواج انتقالات گرمایی تسریع شده و فعالیت کاتالیست بهبود مییابد [3].
نتیجهگیری
در مقاله پیش رو، به مفهوم کاتالیزوری برخی از کاتالیستها پرداخته شد و عامل اصلی پیدایش این خاصیت در نانومواد، «نسبت سطح به حجم بالای آنها» معرفی گردید. بهبود خاصیت کاتالیستی نانومواد به تغییر در خواص الکترونی آنها بازمیگردد. از طرف دیگر، کاهش اندازه نانوذرات همیشه باعث افزایش خاصیت کاتالیستی آنها نمیشود و اغلب عوامل دیگری مانند شکل و بستر بهکاررفته نیز بسیار موثرند. همچنین بهبود عملکرد کاتالیستها با استفاده از نانوذرات این نوید را میدهد که اگر بتوان این نانوکاتالیستها را در مقیاس صنعتی تهیه کرد، میتوان شاهد تحولی عظیم در صنایع، بهخصوص صنعت نفت و پتروشیمی بود.