کاربرد فناوری نانو در مهندسی بافت
بررسی راهحلهای نوآورانه برای بهبود مراقبتهای بهداشتی افراد سالخورده و بیماران همچنان یک چالش جهانی است. در میان تعدادی از استراتژیها برای رسیدن به این هدف، مهندسی بافت به تدریج به یک رویکرد امیدوارکننده برای رفع نیازهای آینده بیماران تبدیل شده است. در مهندسی بافت از داربستها به عنوان پشتیبان برای کشت سلول استفاده میشود، همچنین از موادی جهت چسبندگی و رشد سلولها به داربست استفاده میگردد. از پیشگامان مهندسی بافت میتوان به دکتر گرین در سال 1970 یاد کرد. مطالعات بسیاری طی سالهای بعد در این زمینه انجام گرفت. روشهای مرسوم دارای ایراداتی مانند مقاومت مکانیکی پایین سلولهای مهندسی شده و محدودیت مواد مغذی و … بود. بنابراین با پیشرفت نانوتکنولوژی و ابزارهایی آن، مهندسی بافت نیز با پیشرفتهایی روبرو شد. از آنجایی که مواد با ابعاد نانو دارای ویژگیهای متفاوتی هستند و نانوتکنولوژی در زمینههای تولید داربستها، مهندسی سلولی و دستکاری بیومولکولی دارای کاربردهایی است که در ادامه بحث خواهد شد.
این مقاله شامل سرفصلهای زیر میباشد:
1. مهندسی بافت (tissue engineering) چیست
2. مروری بر استراتژیهای مهندسی بافت
3. تاریخچهای از مهندسی بافت
4. کاربرد نانوتکنولوژی
5. کاربردها نانوتکنولوژی در زمینههای مختلف بافتی
6. نتیجه گیری
1. مهندسی بافت (tissue engineering) چیست؟
ترمیم یا بازسازی کامل بافتها یا اندامهای آسیبدیده و بازیابی عملکرد آنها آرزوی انسان بوده است. به نظر میرسد ظهور مهندسی بافت و پزشکی بازساختی )(TERM) (tissue engineering and regenerative medicine (این امکان را فراهم میسازد. مهندسی بافت سلولها، داربستها و عوامل رشد را برای بازسازی بافتها یا جایگزینی بافتهای آسیبدیده یا بیمار ترکیب میکند. در حالی که پزشکی بازساختی، مهندسی بافت را با سایر استراتژیها، از جمله درمان مبتنی بر سلول، ژن درمانی، و تعدیل ایمنی ترکیب میکند تا بازسازی بافت/ارگان را در داخل بدن القا کند.
مهندسی بافت و پزشکی بازساختی یک علم چندرشتهای است و علوم پایه مانند علم مواد، بیومکانیک، زیستشناسیسلولی و علوم پزشکی را برای تحقق بخشیدن به ترمیم یا بازسازی عملکردی بافت/ارگان ترکیب میکند. با تشدید روند پیری جمعیت جهان، تقاضای فزایندهای برای جایگزینی اعضای بدن وجود دارد. TERM پتانسیل پاسخگویی به نیازهای آینده بیماران را دارد.
هدف TERM ایجاد یک مجموعه سلول/مواد زیستی سه بعدی است که عملکردی مشابه بافت/اندام زنده دارد و ممکن است برای ترمیم یا بازسازی بافت/اندام آسیب دیده استفاده شود. نیاز اساسی این مجموعه این است که بتواند از رشد سلولی، حمل و نقل مواد غذایی و مواد زائد و تبادل گاز پشتیبانی کند[1]
2. مروری بر استراتژیهای مهندسی بافت
دو رویکرد اصلی در این زمینه برای تولید بافت مهندسی شده استفاده میشود.
رویکرد اول، داربست (scaffold) را میتوان به عنوان یک وسیله پشتیبانی سلولی استفاده کرد بدین صورت که در آن سلولها در شرایط آزمایشگاهی کشت (seed) داده میشوند. سپس سلولها تشویق میشوند تا ماتریس را جهت تولید پایههای بافت برای پیوند ایجاد کنند.
رویکرد دوم شامل استفاده از داربست به عنوان عامل انتقال فاکتورهای رشد/دارو است. این استراتژی شامل ترکیب داربست با فاکتورهای رشد است، بنابراین پس از کاشت، سلولهای بدن به محل داربست جذب میشوند و بافت را در سراسر ماتریسها تشکیل میدهند.
این دو رویکرد متقابل نیستند و به راحتی میتوان آنها را با هم ترکیب کرد.
منبع سلول ها نیز یک انتخاب مهم برای داربست است. طیف وسیعی از انواع سلولها را با توجه به نیاز میتوان با داربست ترکیب کرد تا ساختارهای مهندسی بافت تولید شود. این سلولها عبارتند از: سلولهای بنیادی جنینی (Embryonic stem cells)، سلولهای بنیادی مزانشیمی مشتق از مغز استخوان (Bone marrow-derived mesenchymal stem cells)، سلول های بنیادی مزانشیمی مشتق از بند ناف (Cord derived mesenchymal stem cells)، سلولهای کندروسیت (سلولهایی که ماتریس غضروف را ترشح میکند.). و …
1.2. طراحی و ساخت داربست
با پیشرفت رشته مهندسی بافت، نیاز به ساختارهای داربست جدید و تکنیکهای ساخت تکرارپذیر از اهمیت بالایی برخوردار شده است. استفاده از پلیمرهای زیست تخریب پذیر مانند پلی لاکتیک اسید (PLA) گسترده شده است، اما نحوه پردازش این پلیمرها و مواد افزودنی مورد استفاده در زمان ساخت، امکان تنظیم خواص نهایی داربست را فراهم میکند. اسیدهای پلی هیدروکسیل مانند PLA و پلی لاکتیک کو-گلیکولیک اسید (PLGA) به طور گسترده برای روشهای مهندسی بافت مورد استفاده قرار گرفتهاند، زیرا این مواد با هیدرولیز به صورت عمده تجزیه میشوند و مشخصات رهایش دارو و تجزیه قابل کنترل را برای مطابقت با رشد بافت فراهم میکنند. با استفاده دقیق از وزنهای مولکولی، پیوندهای متقاطع و زنجیرههای جانبی، میتوان موادی را با ویژگیهای سفارشی تولید کرد که آنها را برای استفاده در ماتریسهای مهندسی بافت ایدهآل میکند. علاوه بر این، مواد پلی هیدروکسیل اسید نیز سابقه طولانی در استفاده در داخل بدن به عنوان نخ های تجزیهپذیر، دستگاههای دارورسانی و اجزای جراحی زیستتخریبپذیر دارند [2].
3. تاریخچهای از مهندسی بافت
در اوایل دهه 1970 دکتر گرین (W. T. Green, M.D) جراح ارتوپد اطفال در بیمارستان کودکان.، آزمایشاتی انجام داد که میتوان او را از پیشگامان رشته مهندسی بافت قرار داد. دکتر گرین با استفاده ازکشت سلولهای کندروسیت روی اسپیکول های استخوان (اسپیکولهای استخوانی، خارهای استخوانی یا برآمدگیهایی هستند که در امتداد لبه یا بالای استخوانها ایجاد میشوند.) و در نهایت روی موشهای برهنه جای گرفته شد. وی در تلاش برای تولید غضروف جدید بود. اگرچه تلاش او ناموفق بود، اما او به درستی به این نتیجه رسید که با ظهور مواد زیستسازگار جدید، میتوان بافت جدیدی را با کشت سلولهای زنده روی داربستهایی با پیکربندی مناسب تولید کرد.
چندین سال بعد، دکتر برک (Dr. Burke) و دکتر یاناس (Dr. Yannas) از بیمارستان عمومی ماساچوست و M.I.T. در مطالعات آزمایشگاهی و انسانی برای تولید یک جایگزین پوستی با استفاده از ماتریس کلاژن برای حمایت از رشد فیبروبلاستهای پوستی همکاری کردند.
دکتر هوارد گرین (Dr. Howard Green) بعداً صفحاتی از کراتینوسیتها (keratinocytes) را به بیمارانی که دچار سوختگی شدند، منتقل کرد، در حالی که دکتر یوجین بل (Dr. Eugene Bell) ژلهای کلاژن را با فیبروبلاستها کشت داد و از آنها به عنوان ژلهای کلاژن منقبض شده یاد کرد.
همه این نمونهها نشان دهنده شروع رشته جدیدی هستند که اکنون به نام مهندسی بافت شناخته میشود. احتمالاً نکته کلیدی در پیدایش این رشته نوظهور در اواسط دهه 1980 بود، زمانی که دکتر جوزف واکانتی (Dr. JosephVacanti) از بیمارستان کودکان با دکتر رابرت لنگر (Dr. Robert Langer) از MIT با ایدهای جهت طراحی داربست های مناسب برای تحویل سلول به جای کشت سلولها روی سطوح بود.
آگاهی عمومی از مهندسی بافت از زمان پخش برنامهای از ایجاد موش گوشدار در برنامه BBC ایجاد شد (شکل 1). موش «گوشدار» توسط آزمایشگاه واکانتی دانشگاه ماساچوست از طریق مهندسی بافت با استفاده از داربست و سلولهای مناسب ساخته شد و به مظهر مهندسی بافت تبدیل شد.

در سال 1991، یک بیمار جوان مبتلا به سندرم پولاند (Polands Syndrome)، با ناهنجاری مادرزادی در قفسه سینه و عدم وجود جناغ سینه، اولین انسانی بود که یک ایمپلنت مهندسی شده متشکل از یک ایمپلنت داربست پلیمری مصنوعی با سلولهای اتولوگوس کندروسیت (autologous chondrocytes) را دریافت کرد. در این جراحی سه نفر از هشت عضو اصلی هیئت مدیره موسس انجمن مهندسی بافت، دکتر آپتون و دکتر جی. واکانتی و دکتر سی. واکانتی (Dr. J. Upton and Drs. J. and C.Vacanti) حضور داشتند [3].
4. کاربرد نانوتکنولوژی
به طور کلی چهار جزء اساسی در مهندسی بافت وجود دارد، یعنی داربست مواد زیستی، سلولهای عملکردی، زیست مولکولها (به عنوان مثال، فاکتورهای رشد، ECM، سایر مولکولهای عملکردی)، و نیروهای دینامیکی. در ادامه قصد داریم کاربردهای نانوتکنولوژی در مهندسی بافت را در سه بعد مورد بحث قرار دهیم: داربست زیست مواد، مهندسی سلولی و دستکاری بیومولکولی.
1.4. کاربردهای نانوتکنولوژی در داربستهای زیست مواد
داربست بیومتریال محیطی را ایجاد میکند که در آن به سلولها دستور داده میشود تا یک اندام بافتی را به روشی بسیار کنترل شده تشکیل دهند. عملکرد اصلی یک داربست هدایت رفتارهای سلولی مانند مهاجرت، تکثیر، تمایز، حفظ فنوتیپ و مرگ سلولی، از طریق تسهیل پاسخ به محیط در ارتباطات سلول-ماتریس و ارتباطات سلول-سلول است. بنابراین، ویژگیهای فیزیکی مطلوب داربستها برای کاربردهای مهندسی بافت شامل تخلخل بالا، سطح بزرگ، اندازه منافذ بزرگ و ساختارهای متخلخل به هم پیوسته به طور یکنواخت در سراسر ماتریس است. علاوهبراین، داربست باید سیگنالهایی را برای تنظیم سازماندهی سلولها و همچنین ماتریس خارج سلولی مشتق شده از آنها ارائه دهد. با استفاده از فناوری نانو، داربست را میتوان در سطوح اتمی، مولکولی و ماکرومولکولی دستکاری کرد و ساختارهای هندسی و توپولوژیکی خاص در مقیاس 1-100 نانومتر ایجاد کرد. ایجاد داربستهای مهندسی بافت در مقیاس نانو ممکن است ویژگیهای غیرقابل پیشبینی جدیدی را برای مواد به ارمغان بیاورد، مانند مکانیکی (قویتر)، فیزیکی (سبکتر و متخلخلتر)، نوری (انتشار نوری قابل تنظیم)، رنگ، واکنشپذیری شیمیایی (فعالتر یا کمتر خورنده)، خواص الکترونیکی (رسانای الکتریکی بیشتر)، یا خواص مغناطیسی (فوق پارامغناطیس) و ممکن است با عملکردهای جدیدی نیز همراه باشد، که در مقیاسهای میکرو یا ماکرو در دسترس نیستند. از دیگر مزایای استفاده از فناوری نانو برای ساخت داربست میتوان به افزایش سازگاری زیستی، بهبود هدایت تماس، کاهش اصطکاک و در نتیجه سایش برای کاربردهای مفصلی، کاهش نیاز به جراحی تجدیدنظر، تغییر ویژگیهای فیزیکی یا شیمیایی داربست، و ارتقای رشد بافت اطراف ایمپلنت اشاره کرد. به عنوان مثال، مشخص شده است که ویژگی نانویی سطح چنین داربستهایی ممکن است رشد سلول را تحریک کند. سلولها بهسرعت مسیرهای حکاکیشده نانوسکوپی را دنبال میکنند، که منجر به پر شدن سریعتر ماتریس با سلولها یا بافتهای مورد نیاز میشود. مهمتر از آن، برخی از عملکردهای پیچیده بافت خاص را نمی توان به راحتی با داربستهای رزولوشن ماکرو تقلید کرد. داربستهای دقیق در مقیاس نانو را میتوان به سه روش ساخت، عبارتند از: اتم به اتم، مولکول به مولکول (این روش از بالا به پایین (top-down) نامیده می شود)، یا خود مونتاژ (self-assembly) (همچنین خود سازماندهی یا از پایین به بالا (bottom-up) نیز نامیده میشود).
بالا به پایین به معنای ساختن نانودستگاهها از سطح میکرو به سطح نانو است، به عنوان مثال، از بین بردن ذره ویروس برای تشکیل یک قفس ویروسی. در حالی که از پایین به بالا به معنای بدست آوردن نانووسایلهایی است که در آن از اتمها و مولکولهای کوچک (در سطحی کوچکتر از سطح نانو) استفاده میشود، به عنوان مثال، ساختن معماریهای ابر مولکولی از تک مولکولهای کوچک، حتی تکاتمها.
2.4. کاربردهای نانوتکنولوژی در رفتار و مهندسی سلولی
سلولهای برداشت شده از منابع مختلف بافتی را میتوان برای اهداف مهندسی بافت استفاده کرد. به عنوان مثال این سلولها میتواند شامل سلولهای اتولوگ (autologous cells) (از همان فرد)، سلولهای آلوژنیک (allogeneic cells) (از یک فرد متفاوت اما همان گونه)، یا سلولهای اگزوژنیک (xenogeneic cells) (از گونههای متفاوت) باشد. مشکل اصلی سلولها در کاربردهای مهندسی بافت این است که آنها باید جداسازی شوند، به درستی کشت و گسترش داده شوند، به تعداد کافی سلول از یک فنوتیپ واحد برسند تا بتواند عملکرد از دست رفته در نواحی آسیب دیده بازیابی شود. از نظر سلول برای مهندسی بافت، نانوتکنولوژی به دو صورت قابل استفاده است. یکی مهندسی کردن سلولها برای بازسازی بهتر، و دیگری مطالعه رفتار سلول، مانند حرکت سلول، مهاجرت، تکثیر، ردیابی و شناسایی.
3.4. کاربردهای نانوتکنولوژی در دستکاری بیومولکولی
مولکولهای فعال بیولوژیکی، مانند مولکولهای چسبندگی سلولی (فیبرونکتین، لامینین، کلاژن و بسیاری دیگر) و عوامل محلول (عامل رشد اندوتلیال عروقی، فاکتور رشد عصبی و غیره)، سطوح زیستمواد را دارای خواص چسبندگی میکنند و برای اتصال انواع سلولی خاص مجاز هستند. در مقابل، دیگر مولکولهای ماتریس مشتق از سلول مانند خانواده پروتئوگلیکانهای سولفاته، برای رشد سلولی، به عنوان مثال، رشد آکسونی بازدارنده هستند. مولکولهای فعال بیولوژیکی با سلولها از طریق گیرندههای سطح سلولی یا مسیرهای سیگنالدهی داخل سلولی در تعاملند، این مواد باعث بیان یا سرکوب ژنها میشوند و در نتیجه محصولات پروتئینی تنظیمکننده رفتار سلولی را تغییر میدهند. ادغام انتخابی چنین مولکولهای فعال بیولوژیکی در ساختارهای مهندسی بافت، تنظیم دقیق رفتار سلول را ممکن میسازد. سلولها و بافتها به مولکولهای فعال زیستی مانند سیتوکینها، فاکتورهای رشد، عوامل رگزایی و داروها در طول تکامل و بازسازی بافت پاسخ میدهند. بنابراین ترکیب این مولکول ها در طول فرآیند مهندسی بافت، روند بازسازی بافت را تسریع می کند.
با استفاده از فناوریهای نانو، نانوذرات، نانوالیاف، نانوحفرهها، نانولولهها و دندریمرهای (یک پلیمر مصنوعی با ساختاری از زنجیرههای انشعاب مکرر که معمولاً درشت مولکولهای کروی را تشکیل میدهند.) بارگذاری شده با این مولکولها را میتوان در داربستها جاسازی کرد [4].
5. کاربردها نانوتکنولوژی در زمینههای مختلف بافتی
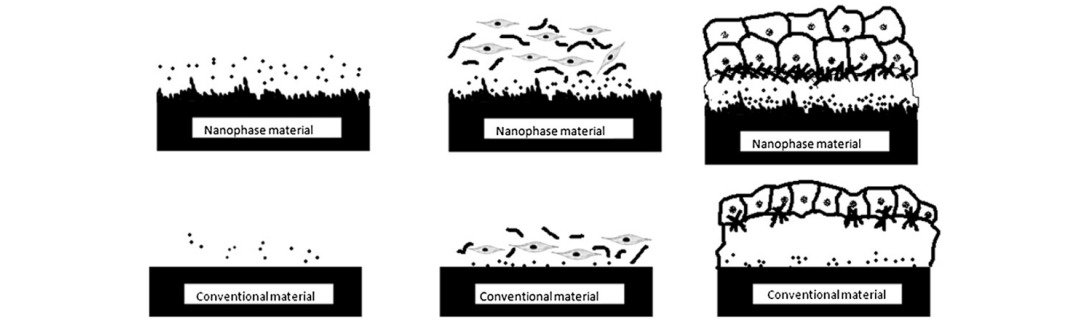
از بحث بالا میتوان نتیجه گرفت که مهندسی بافت از طریق نانوتکنولوژی با استفاده از مواد نانویی در مقایسه با روشهای مرسوم آسانتر است (شکل 2). و در بسیاری از زمینهها برای اهداف مختلف استفاده میشود. در ادامه توضیح داده خواهد شد که برای ایجاد هر یک از بافتهای بنیادی، عصبی، غضروف، استخوان، عروقی و کبدی از چه تکنیکهایی نانوتکنولوژی در مهندسی بافت استفاده میشود تا بتوان بخشهای مختلف هر بافت که دارای تفاوتهای نسبت به یکدیگر هستند را ایجاد کرد.
1.5. مهندسی بافت سلول های بنیادی از طریق میکرو و نانوتکنولوژی
تکنیک های مورد استفاده عبارتند از:
الف) الکتروریسی (Soft lithography) یک تکنیک ریسندگی است که از نیروهای الکترواستاتیکی برای تولید داربستهای فیبری از پلیمرهای زیست سازگار استفاده میکند [6]. الکتروریسی به بهبود چسبندگی و گسترش سلولهای بنیادی/پیشساز خونساز در شبکه نانوالیاف کمک میکند و همچنین در مغز استخوان الکتروریسی بهعنوان نگهدارنده و حامل کارآمدی برای سلولهای بنیادی خونساز میکند.
(2) لیتوگرافی نرم (Soft lithography)، تکنیکی برای ساخت یا تکثیر سازهها با استفاده از قالب و ماسکهای الاستومری (به هر موادی که خاصیت الاستیکی یا ارتجاعی از خود نشان دهد) است. هم چنین نرم نامیده میشود زیرا از مواد الاستومری به ویژه پلی دی متیل سیلوکسان (PDMS) استفاده میشود. لیتوگرافی نرم در تنظیم توزیع، هم ترازی، تکثیر و مورفولوژی سلولهای بنیادی مزانشیمی انسان، شروع تمایز اجسام جنینی با یکنواختی بیشتر در کشت سلولی در شرایط آزمایشگاهی، سهولت در مطالعه رشد و تمایز سلولهای بنیادی جنینی تحت شرایط تعریف شده و تجمع همگن سلولهای بنیادی جنینی استفاده میشود.
2.5. مهندسی بافت سلولهای عصبی از طریق میکرو و نانوتکنولوژی
تکنیکهای مورد استفاده عبارتند از:
الف) الکتروریسی به تمایز سلولی، جهتگیری و رفتار مانند اجسام جنینی که به سلولهای دودمان عصبی بالغ از جمله نورونها، الیگودندروسیتها و آستروسیتها تمایز مییابد، کمک میکند. آنها روی پلیکاپرولاکتون کشت داده میشوند و تمایز سلولهای بنیادی عصبی در پلی (ال-لاکتیک اسید) نانوالیاف بیشتر است.
ب) قالبگیری ماکت (:Replica moulding فرآیندی برای شکل دادن به مواد پلیمری انعطاف پذیر با استفاده از یک قاب یا مدل سفت و سخت کوچک که به آن “mould” گفته میشود). قالبگیری ماکت به حفظ شکل و رفتار سلول کمک میکند.
ج) چاپ میکروکانتکت (Microcontact printing: روشی برای انتقال الگوهای مواد مختلف مانند پلیمرها، پروتئین ها، نانوذرات و غیره بر روی سطح دیگری است. به طور معمول یک تمبر پلیدیمتیلسیلوکسان (PDMS) در محلول یک مادهای که باید طرح ریزی شود آغشته میشود). چاپ میکروکانتکت به ایجاد اتصالات سیناپسی بر روی پروتکل تعریف شده با پلیاستایرن و پلیدیمتیلسیلوکسان کمک میکند همچنین نورونهای هیپوکامپ موش صحرایی زمانی که با اکسید سیلیکون کشت میشوند پتانسیل استراحت را نشان میدهند و پس از 1 روز از کشت قادر به رسیدن به پتانسیل عمل میشوند.
3.5. مهندسی بافت سلولهای غضروف از طریق میکرو و نانوتکنولوژی
تکنیک ها به شرح زیر است:
الف) فوتولیتوگرافی (زیرمجموعهای از میکرولیتوگرافی است که اصطلاح کلی برای فرآیندهایی است که از نور برای تولیدلایههای نازک طرح دار استفاده میکنند. به طور معمول، نور ماوراء بنفش برای انتقال یک طرح هندسی از یک ماسک نوری به یک ماده شیمیایی حساس به نور (مقاومت نوری) پوشش داده شده بر روی بستر استفاده میشود. ). فتولیتوگرافی که برای حفظ رفتار سلولی استفاده میشود، به عنوان مثال کندروسیتهای جدا شده از جناغ پرندگان بر روی ژل آگارز با الگوی ریز که به عنوان داربستهای زیستی عمل میکند کشت داده شدند و به حفظ فنوتیپ غضروفی کمک می کند
ب) قالبگیری ماکت به حفظ محیط کوچک کنترلشده کمک میکند و با میکروسکوپ اینورتد ادغام میشود تا تغییرات اندازه سلول در سلول غضروفی مفصلی را در زمان واقعی نظارت کند.
4.5. مهندسی بافت سلول های استخوانی از طریق میکرو و نانوتکنولوژی
تکنیک های مورد استفاده عبارتند از:
الف) لیتوگرافی نرم که برای حفظ جهتگیری و رفتار سلول استفاده میشود. به عنوان مثال سلولهای پیشساز استخوانی مزانشیمی روی کلاژن کشت میشوند و بنابراین توپوگرافی سطحی مناسب تشکیل استخوان را افزایش میدهد.
(ب) فوتولیتوگرافی توپوگرافی شیار بهتری را برای استئوبلاستهای(سلولهای تولید کننده استخوان) اولیه انسانی فراهم میکند و به چسبندگی سلولی و عملکرد استخوانی و در تعیین پاسخ سلولی نیز کمک میکند.
ج) چاپ میکروکانتکت به ادغام استخوانی استئوبلاست های مشتق شده از سلولهای بنیادی مزانشیمی موش صحرایی که روی پلی (3-هیدروکسیبوتیرات-کو-3-هیدروکسیوالرات) کشت داده شدهاند کمک میکند که میتواند چسبندگی و تراز انتخابی استئوبلاست را هدایت کند.
د) نانوالیاف الکتروریسی نشاسته/پلیکاپرولاکتون مورفولوژی سلول را به کشش وادار میکند و فعالیت و قابلیت زندهمانی را در کشت سلولهای سارکوم استخوانی انسانی افزایش میدهد.
5.5. مهندسی بافت سلول های عروقی از طریق میکرو و نانوتکنولوژی
تکنیکهای مورد استفاده به شرح زیر است:
الف) لیتوگرافی نرم به القای بیان ژن و تغییر در سیگنالدهی سلولی در کشت سلول های بنیادی مزانشیمی با پلیدیمتیلسیلوکسان کمک میکند و همچنین به افزایش احتباس سلولهای اندوتلیال با پلیاورتان کمک میکند که منجر به کاهش ترومبوژنیسیته در طول کاشت آن میشود.
ب) الگوی میکروفلوییدیک به تشکیل ارگانوئیدهای قلبی انقباضی از کاردیومیوسیتها با کمک اسید هیالورونیک کمک میکند و به اتصال سلول به لیگاند و توزیع فضایی برای کشت سلولهای اندوتلیال ورید ناف انسان با پلی (اتیلن گلیکول) کمک میکند.
ج) چاپ میکروکانتکت به واکنش متفاوت با تنش برای کشت سلولهای اندوتلیال آئورت گاوی با پلیدیمتیلسیلوکسان کمک میکند.
د) الکتروریسی به اتصال و مهاجرت سلولها در امتداد محور در کشت سلولهای عضله صاف شریان کرونر انسان با پلی (L-lactid-co ε-کاپرولاکتون) کمک میکند.
6.5. مهندسی بافت سلولهای کبدی از طریق میکرو و نانوتکنولوژی
تکنیکهای مورد استفاده به شرح زیر است:
الف) الکتروریسی تشکیل ساختار یکپارچه الیاف کروی را در کشت سلولهای کبدی اولیه موش صحرایی با پلی (e-caprolactone-coethyl ethylene phosphate) ترویج می کند.
ب) لیتوگرافی نرم همراه با طراحی تعریف شده به ارائه اکسیژن کافی و انتقال مواد مغذی برای حفظ زندهمانی در کشت سلولهای کبدی و کشت سلولهای کبدی اولیه موش صحرایی با پلیدی متیلسیلوکسان و پلیکربنات کمک میکند.
ج) فوتولیتوگرافی به حفظ ساختار سهبعدی سلولی در کشت سلولهای کبدی با پلی(اتیلن گلیکول) کمک میکند و همچنین قادر به حفظ عملکردهای فنوتیپی برای چندین هفته در سلولهای کبدی اولیه و کشت سلولهای کبدی اولیه انسان با پلیدیمتیلسیلوکسان است[5].
6. نتیجه گیری
در این مقاله سعی بر آن شد تا علاوه بر معرفی مهندسی بافت و ذکر تاریخچه ای از این رشته، مشکلات موجود در مهندسی بافت مرسوم و کاربردهای فناوری نانو در این زمینه بیان شود. همان طور که ذکر شد فناوری نانو توانسته با ویژگیهای بخصوص خود در ابعاد نانو در بخش تولید داربست، بیومتریال و سلولهای کشت داده شده به خوبی عمل کند. مهندسی بافت و فناوری نانو هر دو در حال پیشرفت روزافزون هستند، اگرچه ناشناختههای زیادی هنوز در زمینه مهندسی بافت وجود دارد، مهندسی نانو بافت نه تنها یک رویا است، بلکه به سرعت به واقعیت تبدیل میشود. فضای زیادی برای کاربردهای عملی نانوتکنولوژی در مهندسی بافت وجود دارد. مهندسی بافت یک زمینه عالی برای کاوش در کاربردهای عملی فناوری نانو خواهد بود.






