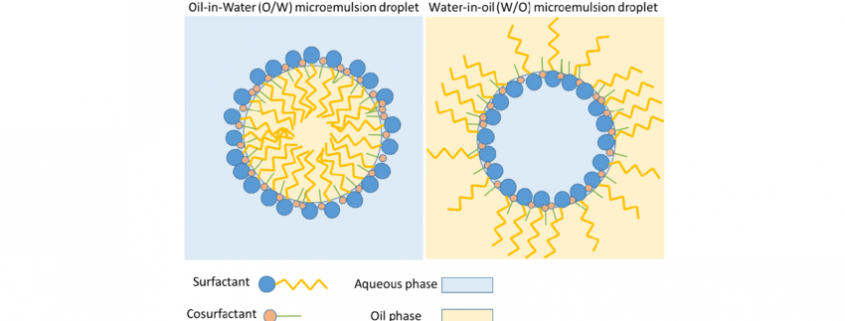
نانوبیوسرامیکها- هیدروکسی آپاتیت

هیدروکسی آپاتیت عضوی از خانواده کلسیم فسفاتها است. این ماده که ترکیبی زیستفعال و زیستسازگار است، اصلیترین جزء معدنی بافت استخوان محسوب میشود. به دلیل شباهت شیمیایی و ساختاری این ترکیب با استخوان، از آن بهطور گسترده در زمینه ترمیم بافت استخوانی و کاربردهای دندانپزشکی و ارتوپدی استفاده میشود. بسیاری از ویژگیهای اساسی هیدروکسی آپاتیت با تغییر مقیاس ذرات آن به نانوذره بهبود و ارتقا مییابد از این رو، در سالهای اخیر روشهای گوناگونی برای سنتز نانوهیدروکسی آپاتیت گزارش شده است. با استفاده از روشهای مشخصهیابی مختلف میتوان کیفیت نانوساختارهای سنتز شده را بررسی کرد. علاوه بر حوزههای مرتبط با استخوان، از نانوهیدروکسی آپاتیت به عنوان حامل نیز در انتقال انواع مواد از جمله داروها، ویتامینها و پروتئینها استفاده میشود.
این مقاله شامل سرفصلهای زیر میباشد:
1. بیوسرامیکها
2. هیدروکسی آپاتیت
3. ساختار شیمیایی هیدروکسی آپاتیت
4. روشهای سنتز نانوهیدروکسی آپاتیت
5. روشهای مشخصهیابی
6. اصلاح سطح نانوهیدروکسی آپاتیت
7. کاربردهای زیستپزشکی نانوهیدروکسی آپاتیت
8. بحث و نتیجهگیری
بیوسرامیکها
از نظر مهندسی، مواد به سه گروه بزرگ غیر فلزی، فلزی و مرکب یا کامپوزیت تقسیم میشوند. سرامیکها و پلیمرها در گروه مواد غیر فلزی جای میگیرند. در مقایسه با فلزات و پلیمرها، سرامیکها را میتوان مواد غیر فلزی و غیر آلی نامید. مواد سرامیکی را که برای کاربردهای کاشتنی پزشکی و دندانپزشکی به کار میروند، بیوسرامیک مینامند. از جمله این بیوسرامیکها میتوان به آلومینا، زیرکونیا، هیدروکسی آپاتیت، تریکلسیم فسفات و شیشههای زیستفعال اشاره نمود [1].
هیدروکسی آپاتیت
“آپاتیت” از واژه یونانی apatáo که به معنی “نادرست و اشتباهی” است گرفته شده چرا که در گذشته، این ترکیب اغلب با بسیاری از مواد معدنی دیگر نظیر فلوئوریت و بریل (سیلیکات برلیوم آلومینیم) اشتباه گرفته میشده است. این اصطلاح نخستین بار در سال 1786 توسط ورنر (Werner) مورد استفاده قرار گرفت [2] و به گروهی از ترکیبات با فرمول عمومی M10(XO4)6Z2اطلاق میشود که در آن M2+یک فلز دوظرفیتی و کاتیون و گونههای XO43- و Z– آنیون هستند. به این ترتیب، نام اختصاصی هر آپاتیت به عناصر M، X و آنیون یکظرفیتی Z بستگی دارد. در مورد هیدروکسی آپاتیت، M کلسیم (Ca2+)، X فسفر (P5+) و Z هیدروکسیل (OH–) است [3]. پس هیدروکسی آپاتیت از نظر شیمیایی، کلسیم فسفات است. نمکهای مختلف کلسیم فسفات در جدول 1 نشان داده شده است. از میان ترکیبات گوناگون کلسیم فسفات، هیدروکسی آپاتیت شاخصترین کمپلکسی است که از نظر شیمیایی و ساختاری با ترکیبات فسفاتی استخوان همخوانی دارد. این ترکیب زیستفعال و زیستسازگار است. البته باید به این نکته توجه کرد که آپاتیت زیستی موجود در بدن بر خلاف هیدروکسی آپاتیت سنتزی، غیر استوکیومتری است و عناصر مختلفی در ساختار آن جایگزین شدهاند که هر کدام از آنها نقش خاصی را ایفا میکنند. علاوه بر شباهت به استخوان، هیدروکسی آپاتیت حامل مناسبی برای رهایش کنترل شده مواد مختلف است چرا که از پایدارترین مشتقات کلسیم فسفات محسوب میشود [1]. از نظر انحلالپذیری، هیدروکسی آپاتیت بعد از فلوئوروآپاتیت، کممحلولترین عضو خانواده کلسیم فسفات است و انحلالپذیری آن در 25 درجه سانتیگراد حدود 0003/0 گرم بر لیتر میباشد [2].
| جدول 1- نمکهای مختلف کلسیم فسفات [1] | |||
| نام | نماد اختصاری | فرمول شیمیایی | نسبت Ca/P |
| تتراکلسیم فسفات | TTCP | Ca4(PO4)2O | 2.0 |
| هیدروکسی آپاتیت | HA یا HAp | Ca10(PO4)6(OH)2 | 1.67 |
| فلوئوروآپاتیت | FA یا FAp | Ca10(PO4)6F2 | 1.67 |
| اکسی آپاتیت | OA یا OAp | Ca10(PO4)6O | 1.67 |
| هیدروکسی آپاتیت با کمبود کلسیم | CDHA | Ca10-x(HPO4)x(PO4)6-x(OH)2-x (0 < x < 1) | 1.67-1.5 |
| آلفا تریکلسیم فسفات | α-TCP | Ca3(PO4)2 | 1.5 |
| بتا تریکلسیم فسفات | β-TCP | Ca3(PO4)2 | 1.5 |
| اکتاکلسیم فسفات | OCP | Ca8(HPO4)2(PO4)4.5H2O | 1.33 |
| کلسیم فسفات آمورف | ACP | CaxHy(PO4)z.nH2O | 1.2-2.2 |
| دیکلسیم فسفات بیآب | DCPA | CaHPO4 | 0.1 |
| دیکلسیم فسفات دوآبه | DCPD | CaHPO4.2H2O | 0.1 |
| منوکلسیم فسفات بیآب | MCPA | Ca(H2PO4)2 | 0.5 |
| منوکلسیم فسفات یکآبه | MCPM | Ca(H2PO4)2.H2O | 0.5 |
ساختار شیمیایی هیدروکسی آپاتیت
هیدروکسی آپاتیت از کلسیم و فسفات تشکیل شده و عضوی از خانواده آپاتیت به شمار میآید. فرمول سلول واحد و فرمول عمومی هیدروکسی آپاتیت به ترتیب Ca10(PO4)6(OH)2و Ca5(PO4)3OH است. شکل 1 ساختار کریستالوگرافی هیدروکسی آپاتیت را نشان میدهد. بدون در نظر گرفتن منبع تهیه، هیدروکسی آپاتیت معمولا مقداری ناخالصی شامل یونهای هیدروکسیل (OH–)، فسفیت (PO33-)، فلورید (F–) و کلرید (Cl–) دارد. یونهای هیدروکسیل و فلورید، استحکام ساختاری را افزایش میدهند در صورتی که یونهای فسفیت و کلرید میتوانند پیکربندی هیدروکسی آپاتیت را تغییر دهند [1].
روشهای سنتز نانوهیدروکسی آپاتیت
اندازه و آرایش ذرات هیدروکسی آپاتیت نقش مهمی در کاربردهای زیستپزشکی این ماده دارد از این رو، روشهای متعددی برای سنتز نانوهیدروکسی آپاتیت گزارش شده است. الکتروریسی (Electrospinning)، سنتز از فاز جامد (Solid-state)، رسوبگذاری شیمیایی (Chemical precipitation)، سل-ژل (Sol-gel)، هیدروترمال (Hydrothermal)، سنتز با کمک ریزموج (Microwave irradiation) و میکروامولسیون (Microemulsion) از جمله روشهای شناخته شده برای سنتز نانوهیدروکسی آپاتیت محسوب میشوند. در روش سنتز از فاز جامد، ترکیبات حاوی کلسیم و فسفات در دمایی حدود 1250 درجه سانتیگراد تحت عملیات حرارتی قرار میگیرند. محدودیت این روش زمان طولانی فرآیند و نیاز به دمای بالا است. با این روش فازهای مختلف کلسیم فسفات (آلفا و بتا تریکلسیم فسفات) تولید میشوند. این فازها منجر به ایجاد تغییرات نامطلوب در ویژگیهای مکانیکی هیدروکسی آپاتیت میشوند و کارایی آن را غیر قابل اطمینان میسازند. رسوبگذاری شیمیایی نیز تکنیک متداولی است اما دستیابی به نسبت ابعادی بالا (high aspect ratio)، استوکیومتری دقیق و بلورینگی زیاد با استفاده از این روش دشوار است. در مقایسه با سایر روشها، روش سل-ژل مزایایی مانند دمای پایین و دستیابی به محصول نانومقیاس همگن را دارد. یک دستورالعمل متداول برای سنتز نانوهیدروکسی آپاتیت با این روش، پیرسازی (Aging) محلول اتانولی با pH=10 از Ca(NO3)2، (NaH)2PO4، NH4OH و PEG در دمای 85 درجه سانتیگراد به مدت 4 ساعت و سپس انجام فرآیند خشک کردن است. جدول 2 برخی از روشهای سنتز نانوهیدروکسی آپاتیت و ویژگیهای محصول بدست آمده از هر روش را نشان میدهد [2و1].
| جدول 2- برخی از روشهای سنتز نانوهیدروکسی آپاتیت [1] | |||||
| روش | توزیع اندازه ذرات | شکل | بلورینگی | خلوص فازی | هزینه |
| الکتروریسی | متغیر | الیاف | زیاد | متغیر | متغیر |
| سنتز از فاز جامد | گسترده | گوناگون | زیاد | کم | کم |
| رسوبگذاری شیمیایی | متغیر | گوناگون | کم | متغیر | کم |
| سل-ژل | باریک | گوناگون | متغیر | متغیر | متغیر |
| هیدروترمال | گسترده | سوزنیشکل | زیاد | زیاد | زیاد |
| سنتز با کمک ریزموج | باریک | گوناگون | زیاد | زیاد | متغیر |
| میکروامولسیون | باریک | سوزنیشکل | کم | متغیر | زیاد |
روشهای مشخصهیابی
برای بررسی نانوهیدروکسی آپاتیت از روشهای مشخصهیابی مختلفی استفاده میشود. تصاویر SEM و TEM نانوذرات هیدروکسی آپاتیت مزومتخلخل توخالی (hollow mesoporous hydroxyapatite nanoparticles) به ترتیب در شکلهای 2-الف و 2-ب نشان داده شده است. درون شکل 2-ب، تصویر میکروسکوپ الکترونی عبوری روبشی (STEM) میدان تاریک این ترکیب دیده میشود. شکل 2-ج، الگوی XRD نانوهیدروکسی آپاتیت سنتز شده با روش هیدروترمال در دمای 180 درجه سانتیگراد و زمانهای مختلف را نشان میدهد. شکل 2-د طیف فوتوالکترون اشعه ایکس (XPS) هیدروکسی آپاتیت است که بررسی عنصری این ترکیب را ممکن میسازد. پیکهای فوتوالکترون شاخص این ترکیب شامل 1/536 الکترونولت (O 1s)، 9/347 الکترونولت (Ca 2p) و 2/133 الکترونولت (P 2p) است. با استفاده از طیفسنجی فروسرخ و طیفسنجی رامان میتوان پیوندهای شیمیایی هیدروکسی آپاتیت را مورد بررسی قرار داد. پیکهای شاخص هیدروکسی آپاتیت در طیف FTIR عبارتاند از: 574، 602 و cm-1 631 (ارتعاش خمشی پیوند O-P-O)، 1032، 1046 و cm-1 1087 (ارتعاش کششی پیوند P-O) و cm-1 3572 (ارتعاش کششی پیوند O-H) (شکل 2-ه). پیکهای طیف رامان در محدوده cm-1 1045-963 ظاهر میشوند. PO43- چهاروجهی در cm-1 963 و پیک ارتعاش کششی نامتقارن P-O در cm-1 1045-1043 مشاهده میشود (شکل 2-و). ظاهر شدن پیکها در این محدوده نشاندهنده آن است که هیدروکسی آپاتیت یکنواخت و همگن است [3و1].
اصلاح سطح نانوهیدروکسی آپاتیت
متداولترین مشکلی که پژوهشگران در مورد نانوهیدروکسی آپاتیت با آن روبرو هستند، تجمع ذرات این ترکیب است. گرد هم آمدن و تجمع نانوذرات به واکنشگرهای مورد استفاده و روش سنتز، مرز آبدوست-آبگریز بین فازها و محلولها، ماهیت شیمیایی و انرژی سطحی بستگی دارد. بنابراین اصلاح سطح نانوهیدروکسی آپاتیت، روشی برای کنترل پخش این ماده و استفاده از آن در کاربرد مورد نظر است. تاکنون از ترکیبات مختلفی برای این منظور استفاده شده است که از آن جمله میتوان به انسولین، استئاریک اسید، هگزانوئیک اسید، دکانوئیک اسید، پیروفسفریک اسید، اولئیک اسید، انواع سیلانها، پلیآکریلیک اسید، اتیلن گلیکول متاکریلات فسفات و … اشاره کرد. این ترکیبات با روشهایی مثل پیوند زدن (Grafting)، واکنش مستقیم (Direct reaction)، پوششدهی (Coating) و پلیمریزاسیون (Polymerization) روی سطح نانوهیدروکسی آپاتیت قرار میگیرند و در نتیجه، سطح اصلاح خواهد شد. همانطور که مشاهده میشود، بخش عمدهای از ترکیبات اصلاحکننده، کربوکسیلیک اسیدها هستند. این مواد با برقراری پیوند هیدروژنی، اتصالی قوی با سطح هیدروکسی آپاتیت ایجاد میکنند. بهطور کلی دو مزیت مهم برای استفاده از کربوکسیلیک اسیدها به عنوان عامل اصلاحکننده وجود دارد. نخست آنکه جانوران شکلهای مختلفی از کربوکسیلیک اسیدها را به صورت ویتامینها، بازدارندههای متابولیکی، چربیها و پروتئینها دارند و بنابراین اتصال نانوهیدروکسی آپاتیت با این اجزا قوی است. دومین مزیت، تغییر ماهیت نانوهیدروکسی آپاتیت از آبدوست به چربیدوست با استفاده از کربوکسیلیک اسیدهای بلندزنجیر است.
کاربردهای زیستپزشکی نانوهیدروکسی آپاتیت
حامل در دارورسانی
بیش از دو دهه از آغاز پژوهشها درباره استفاده از نانوهیدروکسی آپاتیت به عنوان حامل دارو میگذرد. تاکنون نقش نانوهیدروکسی آپاتیت به عنوان حامل برای داروهای گوناگونی نظیر ضد جذب (anti-resorptive)، ضد سرطان، آنتیبیوتیک، داروهای ضد التهاب غیر استروئیدی، ویتامینها و نیز پروتئینها، ژنها و رادیونوکلیدها (radionuclide) مورد بررسی قرار گرفته است [1]. شکل 3 مستقر شدن جهتدار پروتئینها روی سطح هیدروکسی آپاتیت را نشان میدهد [4].
شکل 3. استقرار جهتدار پروتئینها روی سطح هیدروکسی آپاتیت با استفاده از لینکرها [4]
از جمله معروفترین داروهایی که بارگیری آنها در نانوساختارهای هیدروکسی آپاتیت ارزیابی شده است میتوان به دوکسوروبیسین، پکلیتاکسل، سفازولین، آمپیسیلین، جنتامایسین و لووفلوکساسین اشاره کرد [1].
مطالعات نشان میدهد که سینتیک جذب و واجذب مولکول دارو تحت تاثیر ویژگیهای دارو و شکل نانوذرات هیدروکسی آپاتیت قرار میگیرد. دو داروی ضد سرطان آلندرونات (alendronate) با بار منفی و سیسپلاتین با بار مثبت، به خوبی روی نانوهیدروکسی آپاتیت جذب میشوند در حالی که کمپلکس خنثای دی(اتیلن دیآمین پلاتین) مدرونات (di(ethylenediamine platinum) medronate, DPM) تمایل کمی به جذب روی سطح نانوذرات هیدروکسی آپاتیت دارد. از سوی دیگر، سیسپلاتین جذب روی سطح هیدروکسی آپاتیت سوزنیشکل را ترجیح میدهد در صورتی که آلندرونات، سطح صفحهای شکل را انتخاب میکند. سرعت رهایش داروی خنثای DPM بیش از دو داروی باردار آلندرونات و سیسپلاتین است. این دارو از نانوذرات سوزنیشکل هیدروکسی آپاتیت سریعتر از نانوذرات صفحهایشکل آزاد میشود و این در حالی است که دو داروی باردار، با سرعتی مشابه از نانوذرات مختلف هیدروکسی آپاتیت آزاد میشوند [5].
ماده پوششدهنده
از آنجا که هیدروکسی آپاتیت از نظر شیمیایی مشابه استخوان طبیعی است، از نانوذرات این ماده به عنوان پوشش برای ایمپلنتهای پزشکی که از موادی مانند آلیاژ تیتانیوم ساخته شدهاند، استفاده میشود. هدف از این کار افزایش زیستفعالی و زیستسازگاری است [1].
سرامیک
استفاده از مواد خارجی به عنوان ایمپلنت در داخل یا خارج بدن انسان موضوع جدیدی نیست. شواهدی وجود دارد که نشان میدهد بیش از 2000 سال پیش برای ترمیم بافت آسیب دیده استخوانی از مواد مختلفی استفاده میشده است [3]. با این حال از اوایل قرن بیستم بود که توجه پژوهشگران به استفاده از کلسیم فسفاتها برای تولید جایگزین استخوانی در کاربردهای زیستپزشکی معطوف شد [2]. در حال حاضر از نانوهیدروکسی آپاتیت به شکل سرامیکی و کامپوزیتی در زمینه مهندسی بافت استخوان (Bone Tissue Engineering, BTE) استفاده میشود. به عنوان مثال، بیوسرامیک بر پایه هیدروکسی آپاتیت و حاوی زیرکونیوم، ویژگیهای مکانیکی بهتری دارد و به دلیل ساختار اصلاح شده، برای کاربردهای دندانپزشکی و ارتوپدی مطلوبتر است [1].
ماده کامپوزیتی
امروزه کامپوزیتهای مختلف نانوهیدروکسی آپاتیت با ترکیباتی مانند پلیلاکتیک گلیکولیک اسید (PLGA)، کلاژن و پلیمتیلمتاکریلات (PMMA) مورد بررسی گسترده قرار گرفته است و نتایج نشان میدهد که روند تشکیل استخوان با این کامپوزیتها افزایش چشمگیری پیدا میکند [1].
بحث و نتیجهگیری
هیدروکسی آپاتیت یک بیوسرامیک مهم محسوب میشود. در این مقاله خانواده آپاتیتها و همچنین کلسیم فسفاتها که هیدروکسی آپاتیت عضوی از آنها محسوب میشود معرفی شد. از آنجا که اندازه ذرات هیدروکسی آپاتیت نقش مهمی در کاربردهای زیستپزشکی این ماده دارد، روشهای سنتز و مشخصهیابی نانوساختارهای هیدروکسی آپاتیت مورد بررسی قرار گرفت. از جمله کاربردهای نانوهیدروکسی آپاتیت میتوان به نقش آن به عنوان حامل در دارورسانی و همچنین استفاده به عنوان پوشش، سرامیک و کامپوزیت در حوزه مهندسی بافت استخوان اشاره کرد.
منابـــع و مراجــــع
۱ – Munir, M.U., Salman, S., Ihsan, A., Elsaman, T., “Synthesis, Characterization, FunctionalizationBio-Applications of Hydroxyapatite Nanomaterials: An Overview”, International Journal of Nanomedicine, Vol. 17, pp. 1903-1925, (2022).
۲ – Fiume, E., Magnaterra, G., Rahdar, A., Verné, E., Baino, F., “Hydroxyapatite for Biomedical Applications: A Short Overview”, Ceramics, Vol. 4, pp. 542-563, (2021).
۳ – Fazel, R. “Biomedical Engineering- FrontiersChallenges”, 1st Edition, Croatia:InTech, pp 83-84, (2011).
۴ – Yewle, J.N., Wei, Y., Puleo, D.A., Daunert, S., Bachas, L.G., iented Immobilization of Proteins on Hydroxyapatite Surface Using Bifunctional Bisphosphonates as Linkers”, Biomacromolecules, Vol. 13, pp. 1742-1749, (2012).
۵ – Palazzo, B., Iafisco, M., Laforgia, M., Margiotta, N., Natile, G., Bianchi, C.L., Walsh, D., Mann, S., Roveri, N., “Biomimetic Hydroxyapatite-Drug Nanocrystals as Potential Bone Substitutes with Antitumor Drug Delivery Properties”, Advanced Functional Materials, Vol. 17, pp. 2180-2188, (2007).