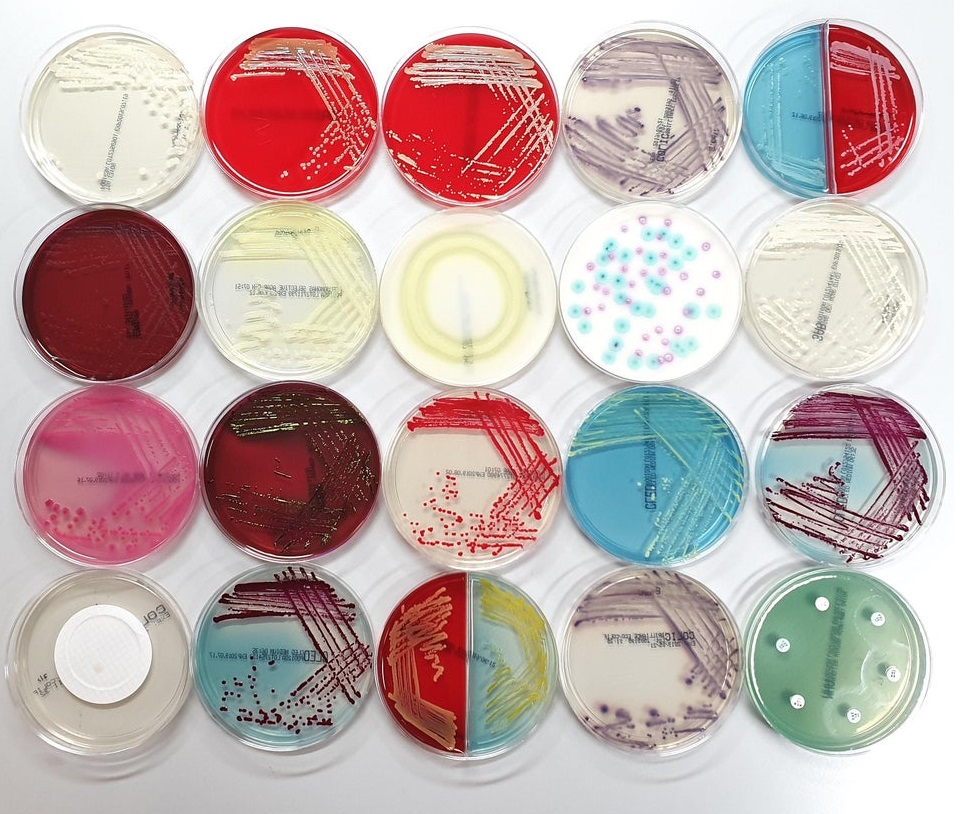
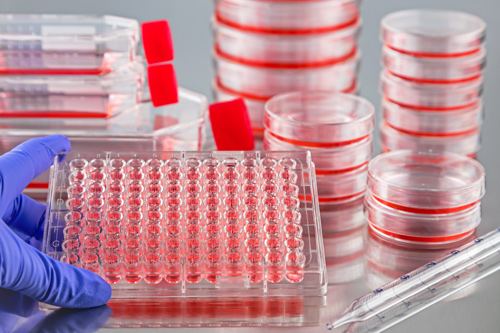
الکتروفورز ژل پلی آکریلامید SDS-PAGE و وسترن بلاتینگ
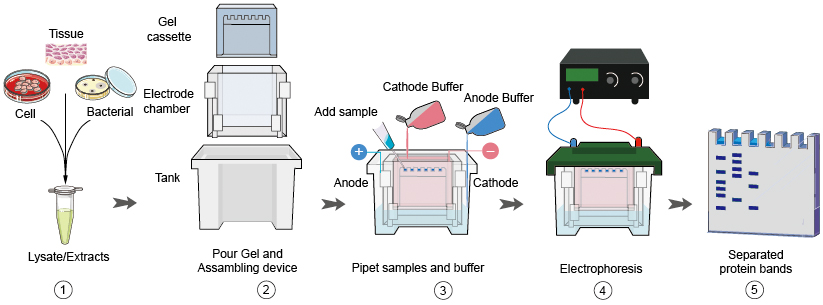
كاربرديترين روش مورداستفاده براي تعيين خلوص پروتئين در نمونههاي بيولوژيكي و تعيين وزن مولكولي زنجيرههاي پلی پپتیدی الكتروفورز SDS-PAGE است. پايه و اساس اين روش حركت مولكولهاي باردار در ميدان الكتريكي است كه سرعت حركت مولكول بهوسیله وزن مولكول تعيين ميشود. از يك صفحه پليمري (پلی آکریلامید) بهعنوان سدي در مقابل حركت مولكولها در ميدان الكتريكي استفاده ميشود. قبل از قرار دادن نمونه در ميدان الكتريكي، نمونه در معرض عوامل دناتوره كننده مانند حرارت، دترجنتها و عوامل احياكننده باندهاي دي سولفيدي قرار ميگيرد. براثر اين عوامل احیاکننده باندهاي دی سولفیدی پروتئين از بين رفته، زیر واحدهای پروتئيني از يکديگر جدا ميشوند. در اين وضعيت، زنجيرههاي پلی پپتیدی به يك نسبت وزني ثابت با SDS باند ميشوند. SDS بهطور كامل زنجيره پلی پپتیدی را پوشانده و به آن كاملاً بار منفي ميدهد. در چنين شرايطي حركت مولكولهاي پروتئين در ميدان الكتريكي صرفاً تحت تأثیر وزن مولكولي قرار ميگيرد و اثر بارهاي درونمولکولی از بين ميرود. پروتئينهاي بزرگتر نسبت به پروتئينهاي کوچکتر چندين بار آهستهتر حركت ميكنند. در اين روش، نمونه پروتئيني درون چاهكهايي روی ژل بارگذاری ميشود كه در ارتباط با بافر الكترود متصل به قطب منفي است. وقتي جريان الكتريسيته برقرار ميشود، پروتئينهاي پوشيده شده با SDS كه داراي بار منفی هستند به سمت پايين ژل حركت ميكنند كه در ارتباط با بافر الكترود متصل به قطب مثبت است.
روش Western blotting
وسترن بلاتینگ، يک روش اختصاصي براي شناسايي يا تعيين کميت پروتئينها در نمونههاي مجهول است. اصطلاح blotting به انتقال نمونههاي بيولوژيك از ژل به غشا و به دنبال آن آشكارسازي غشا كه ايمونوبلات هم ناميده ميشود، اشاره دارد. این روش براي اولين بار در سال 1979 توسط Towbin معرفي شد و امروزه بهعنوان يك روش رایج براي آناليز پروتئینها به كار ميرود. اختصاصی بودن واكنش آنتيبادي–آنتيژن منجر به شناسايي پروتئين هدف در بين مخلوطي از پروتئينها میشود. این روش، دادههاي كيفي و كمي درباره پروتئين را در اختیار پژوهشگر قرار ميدهد.