اهمیت سطح در دنیای نانو
اهمیت سطح در دنیای نانو
همانطور که میدانید، واکنشهای شیمیایی در محلی اتفاق میافتند که ماده با محیط اطراف در تماس است. این محل همان سطح ماده است. واکنش از این منطقه شروع شده و سپس تحت شرایطی به عمق نفوذ میکند. برای بررسی بیشتر، اکسید شدن آلومینیوم را در نظر بگیرید. یک قطعه آلومینیومی سطحی کدر دارد که در صورت سمباده زدن آن، لایههای زیرین که بسیار شفاف هستند، پدیدار میشوند. این لایههای بسیار شفاف، همان آلومینیوم هستند. اما این سطح براق به سرعت به سطحی کدر و مات تبدیل میشود. بررسیها نشان داده است که این لایه بسیار نازک و کدر، ترکیبی از اکسیژن و آلومینیوم است. آلومینا یا اکسید آلومینیوم (Al2O3) یک ماده سرامیکی بسیار سخت است که به شکل یک لایه پیوسته، روی سطح آلومینیوم را میپوشاند. این لایه از تماس لایههای زیرین (که از آلومینیوم هستند) با هوای اطراف جلوگیری میکند. بنابراین، واکنش اکسایش آلومینیوم ادامه پیدا نمیکند و بقیه ماده از اکسید شدن حفظ میشود.
طبق مطالب بیان شده، با تشکیل لایه اکسید روی ِ آلومینیوم، این ماده از نظر شیمیایی غیرفعال شده و واکنش متوقف میشود. به نظر شما این پدیده دارای چه مزیتها و مضراتی است؟
اکسید شدن آهن با اکسید شدن آلومینیوم تفاوت دارد. اگر دقت کرده باشید، زنگ آهن، مادهای است قرمز رنگ که به راحتی میشکند و میریزد. این ماده به راحتی از روی آهن جدا میشود و بنابراین، اکسیژن به قسمتهای داخلی و به زیر لایه اکسیدی نفوذ کرده و واکنش اکسایش ادامه مییابد. به گونهای که ادامه روند این واکنش منجر به تخریب کامل قسمتی از قطعه فولادی شده و در نهایت، موجب انهدام آن میشود.
بنابراین، اگر بخواهیم به دنبال ادامه دادن یک واکنش باشیم، باید راهی برای نفوذ به درون آن ماده بیابیم. یک راه، انتقال مواد از درون حجم ماده به سطح آن است. برای این کار (دسترسی به قسمتهای داخلی حجم ماده) میتوانیم مسیری را درون ماده تعبیه کنیم. این کار را میتوان با ایجاد حفراتی که به هم متصل هستند و تا سطح ماده ادامه دارند، انجام دهیم (شکل 1). به این مواد که ساختاری اسفنج مانند دارند، مواد متخلخل یا فوم میگوییم. در طبیعت نیز میتوان مواد متخلخل را به وفور مشاهده کرد. زئولیتها موادی از این دسته هستند. از مواد متخلخل مصنوعی نیز میتوان به فومهای فلزی اشاره کرد که امروزه کاربردهای بسیاری در صنایع دارند. از مواد متخلخل میتوان برای کاتالیز واکنشهای شیمیایی، فیلترهای مایعات و فیلترهای هوا استفاده کرد. بنابراین، هرچه اتمهای بیشتری در سطح باشند، واکنشهای شیمیایی با سهولت بیشتری رخ میدهند. این رویداد برخی موارد مفید، و در برخی موارد مضر است.

شکل 1. طرحی از مواد متخلخل
یک راه دیگر، کوچکتر کردن اندازه مواد واکنشدهنده است. برای بیان این موضوع، توضیحات را در قالب یک مثال ادامه میدهیم. ممکن است مطالبی را در رابطه با سوختهای جامد شنیده باشید. سوختهای جامد مانند پودر آلومینیوم در برخی کاربردهای خاص مورد استفاده قرار میگیرند. یکی از این کاربردها، استفاده به عنوان سوخت موشک است. همانگونه که قبلاً نیز گفته شد، آلومینیوم واکنشپذیری بالایی دارد و به سرعت اکسید میشود. پودرهای ریز آلومینیوم بر اثر واکنش با اکسیژن، به شدت آتش میگیرند و گرمای زیادی آزاد میکنند.
سوختهای جامد یا Solid Fuel به انواع مواد جامدی گفته میشود که به عنوان سوخت استفاده میشوند و در اثر اشتعال، گرما و انرژی آزاد میکنند، مانند: زغال چوب و زغال سنگ. یکی از کاربردهای این نوع سوخت، استفاده از آن به عنوان سوخت موشک است.
به نظر شما اندازه پودرهای آلومینیوم چه تأثیری بر میزان انرژی آزاد شده و در نتیجه بازده سوخت دارد؟
برای پاسخ به این پرسش، شکل 2 را در نظر بگیرید. در این شکل فرض کردهایم که پودر آلومینیوم به شکل کره است. در صورتی که این ذره پودر در معرض اکسیژن قرار بگیرید و واکنش دهد، یک لایه از اکسید آلومینیوم روی آن قرار میگیرد. با توجه به آنچه در مورد اکسید آلومینیوم گفته شد، این لایه تشکیل شده، از ادامه واکنش اکسایش جلوگیری میکند و مقدار زیادی از قسمتهای داخلی این ذره پودری، از واکنش در امان میماند. اما در صورتیکه اندازه این ذره کمتر باشد، مقدار بسیار کمتری از آن دستنخورده باقی میماند. بنابراین، مقدار بیشتری از سوخت جامد مصرف شده و بازده بیشتر میشود.
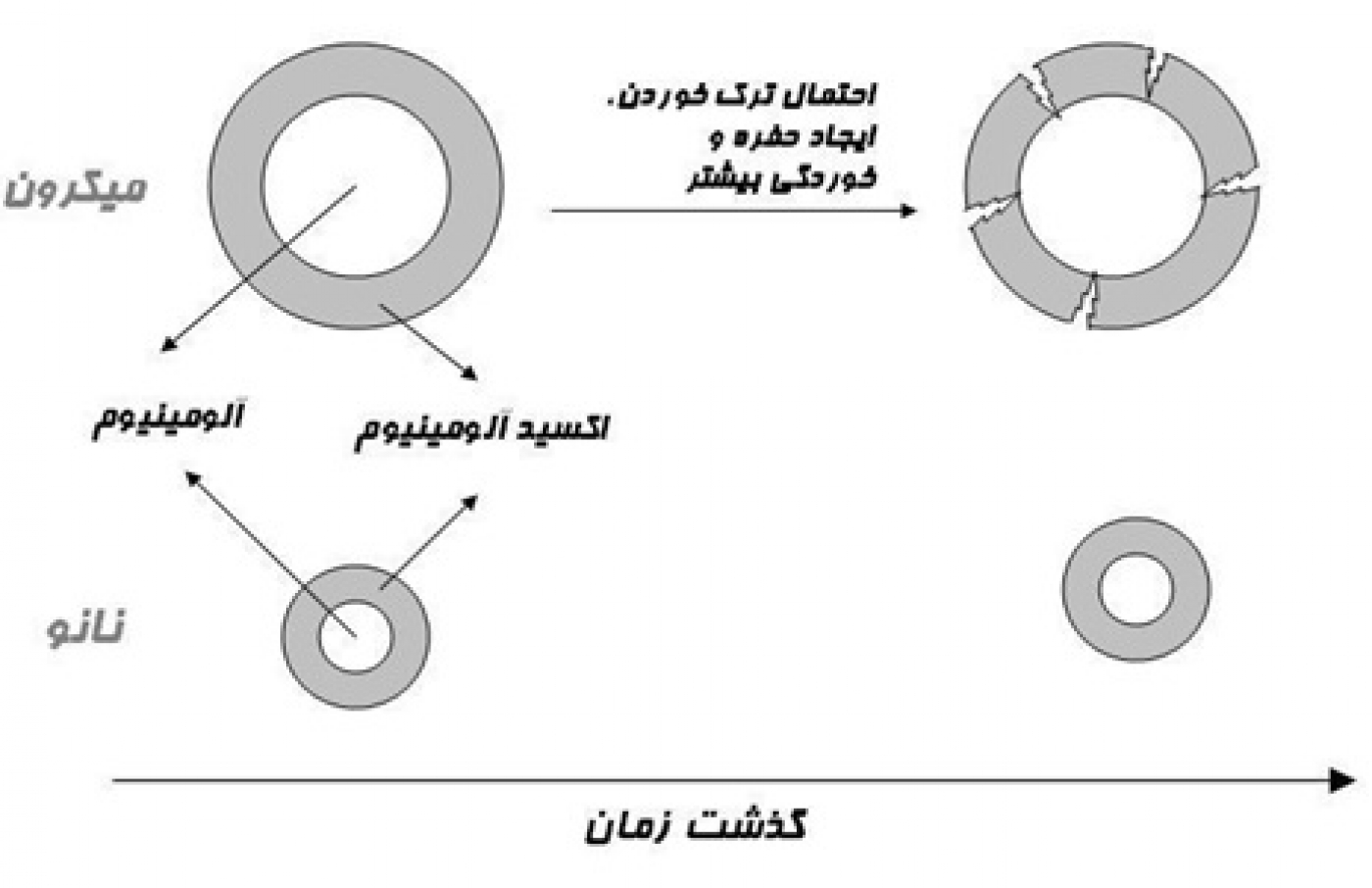
شکل 2. مقایسهای بین اکسید شدن ذرات آلومینیوم با اندازههای مختلف
به طور خلاصه، برای در دسترس قرار دادن مقدار بیشتری از یک ماده، یا باید آن را به شکل متخلخل داشته باشیم یا اندازه ذرات آن را کوچکتر کنیم. در هر دو رویکرد، در واقع؛ مقدار بیشتری از ماده روی سطح قرار میگیرد، یا میتوان گفت که نسبت سطح به حجم افزایش یافته است. اهمیت سطح تنها در واکنشهای شیمیایی مطرح نیست، بلکه برهمکنشهای فیزیکی و مکانیکی ماده با محیط نیز از طریق سطح انجام میگیرد. از این موارد میتوان به پدیدههای اصطکاک و انتقال حرارت اشاره کرد. بنابراین، تغییر مقدار سطح ماده میتواند بر این پدیدهها تأثیر بگذارد.
آیا همیشه با کوچکتر شدن اندازه ماده، خواص آن تغییر میکند؟ این خواص شامل چه مواردی هستند؟
همانگونه که میدانید، در ابعاد نانو، خواص نوری، الکتریکی، مغناطیسی و شیمیایی مواد به شدت تغییر میکند. برای مثال، نقطه ذوب ذرات 50 نانومتری طلا با نقطه ذوب ذرات 10 نانومتری طلا بسیار متفاوت است. رنگ نانوذرات طلا نیز با یکدیگر متفاوت است. اما اگر شمشهای بزرگ طلا را به قسمتهای چند میلیمتری تقسیم کنیم، نقطه ذوبشان تغییر نمیکند و همچنان به رنگ زرد (طلایی) دیده میشوند. چگونه این واقعیت را توجیه میکنید؟ آیا ابعاد نانومتر، محدوده خاصی است که در آن اتفاقات ویژهای میافتد؟
در قبل آموختیم که راههایی برای افزایش سطح ماده و آوردن اتمهای آن از داخل حجم به سطح وجود دارد. همچنین آموختیم که با افزایش سطح ماده، خواص آن تغییر میکند. درک این که چرا واکنشپذیری شیمیایی ماده با افزایش سطح آن بیشتر میشود، بسیار ساده است. اما این سؤال پیش میآید که، چرا این موضوع در ابعاد نانومتری اهمیت بسیار بالایی پیدا کرده است و چرا خواص مختلف ماده در این ابعاد دستخوش تحولات زیادی میشود؟ چنانچه مادهای با مقیاس چند ده متری را کوچکتر کرده و به ابعاد میلیمتری برسانیم، هیچ تغییری در نقطه ذوب، رنگ و خواص مغناطیسی آن ایجاد نمیشود. اما این تغییر در هنگام کوچکتر کردن ماده تا ابعاد نانومتری دیده میشود.
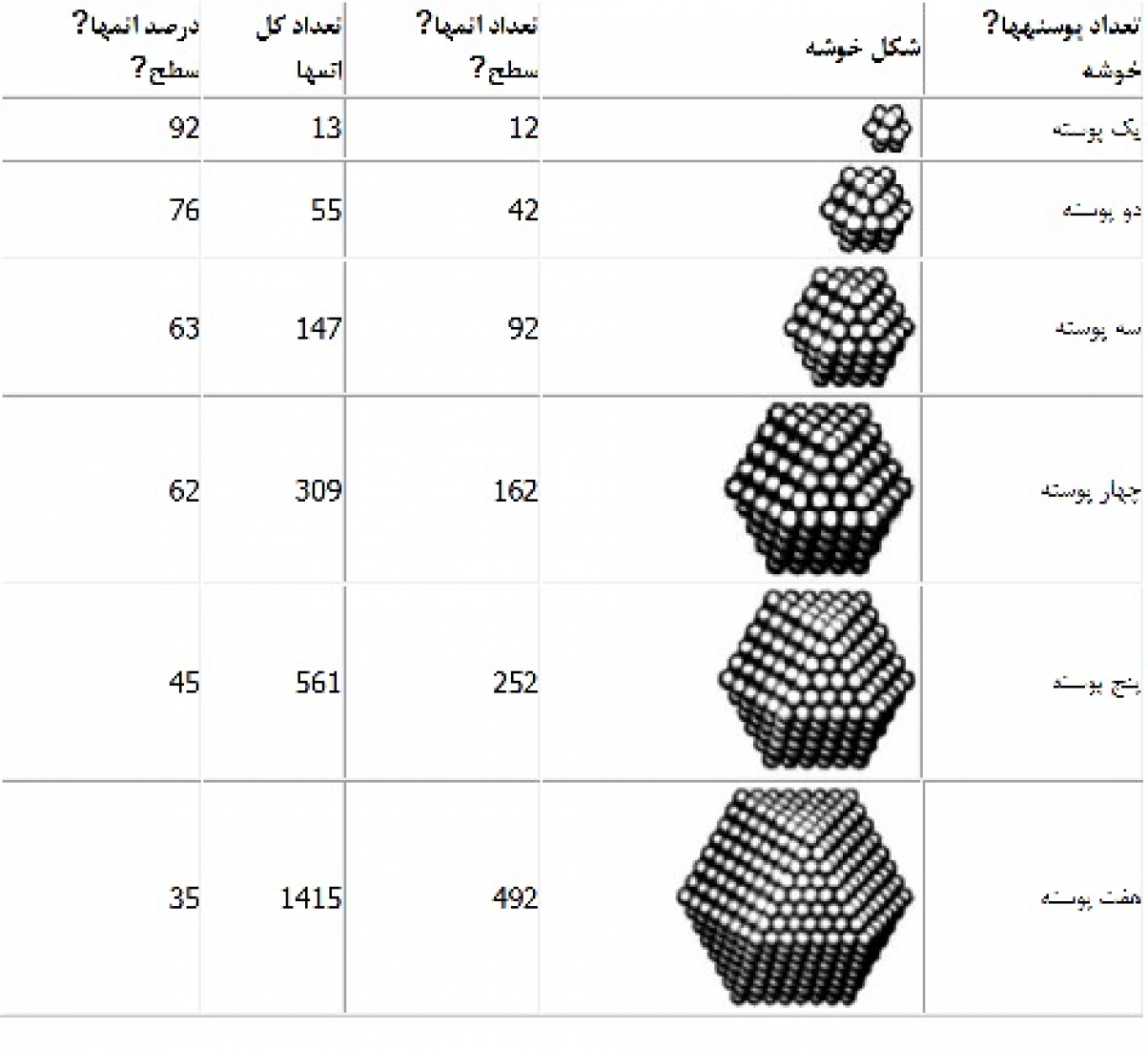
کلید حل این مسأله در این جاست که تعداد اتمهای سطحی در مواد با مقیاسهای بزرگتر از نانومتر، بسیار ناچیز است، اما با ورود به دنیای نانومتری، مقدار این اتمها نسبت به کل اتمهای ماده، بسیار زیاد میشود. برای بررسی دقیقتر و درک این موضوع، به جدول 1 دقت کنید.
همانطور که میدانید، در یک ماده جامد، هر اتم در محل مشخصی نسبت به دیگر مواد قرار گرفته است. در مواد بلوری، با توجه به جنس ماده، فواصل بین اتمها کاملاً قابل محاسبه و مشخص هستند. در اطراف هر یک از این اتمها، تعداد مشخصی اتم دیگر با فواصل معین قرار گرفته است. این اتم با برخی از اتمهای اطراف که کمترین فاصله را با آن دارند، در ارتباط مستقیم است. طبق تعریف، تعداد این اتمها را عدد همسایگی، عدد همآرایی یا عدد کوئوردیناسیون میگوییم.
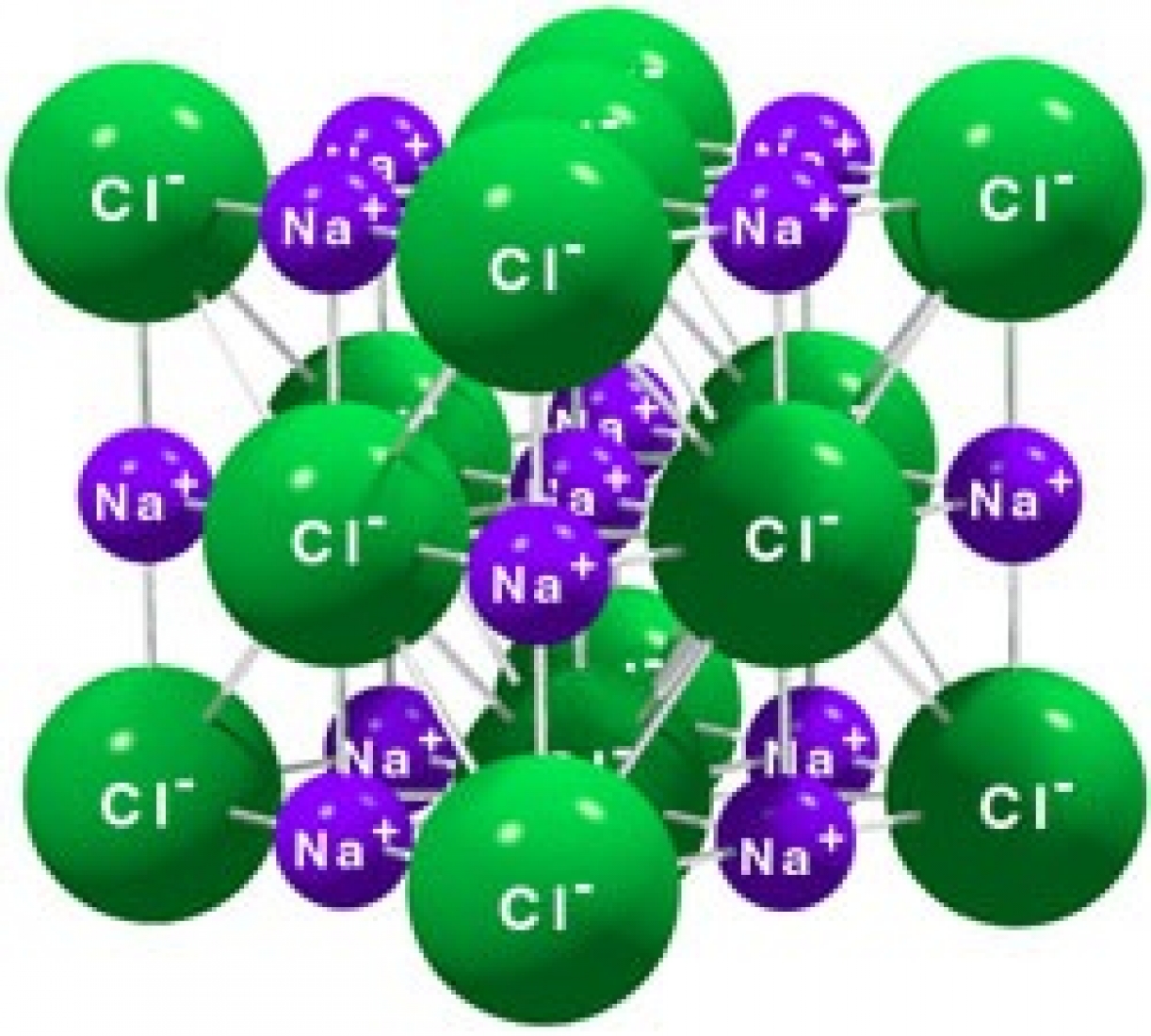
عدد کوئوردیناسیون که برای ساختارهای بلوری به کار میرود، عبارت است از تعداد اتمهایی که نزدیکترین فاصله را با یک اتم دارند. به طور مثال، این عدد برای اتم سدیم در بلور نمک طعام، 6 است که نشان میدهد هر اتم سدیم، توسط 6 اتم کلر احاطه شده است.
در بلور نمک طعام (شکل 1) عدد همسایگی برای اتمهای سدیم و کلر برابر با 6 است. اما نکتهای وجود دارد که باید به آن توجه کرد. یک بلور نمک طعام، اندازه محدودی دارد. یک وجه این بلور را در نظر بگیرید، به نظر شما تعداد نزدیکترین همسایههای اتمهای موجود روی این سطح، برابر با 6 است؟
همانطور که میدانید، این اتمها تنها از یک طرف با دیگر اتمهای بلور در ارتباط هستند. اگر یک بلور نمک طعام را در حالت کاملاً ایدهآل و کامل (بدون نقص) در نظر بگیریم، نزدیکترین همسایههای اتم مستقر روی وجه، برابر با 5، برای اتم مستقر روی یال، برابر با 4 و برای اتم موجود در رأس این مکعب، برابر با 3 است (شکل 3).
شکل 3. بلور نمک طعام
آیا عدد همسایگی یک اتم در تعیین خواص آن نقش دارد؟
2. چرا نانو؟
1.2. یک آزمایش ساده
1.1.2. مواد و وسایل موردنیاز
1- مقوا به اندازه ساخت دو مکعب به اضلاع 10×5×5 سانتیمتر
2- مقداری چسب نواری
3- دویست عدد حبه قند مکعبی
4- مقداری شکر (از نظر جرم برابر با جرم 200 عدد حبه قند)
5- مقداری آب
6- یک گرمکن الکتریکی (هیتر)
7- اسپری آبپاش یا قطرهچکان
2.1.2. شرح آزمایش
با استفاده از مقوا و چسب نواری، دو عدد مکعب به اضلاع 5×5×10 سانتیمتر بسازید. یکی از وجههای 5×10 سانتیمتری آن را خالی بگذارید تا بتوانید درون آن مقداری قند و شکر بریزید.
100 عدد حبه قند مکعبی شکل را به همراه نیمی از شکرها با همدیگر مخلوط کنید و آن را درون یکی از مکعبهای مقوایی که ساختهاید بریزید. این مکعب را مکعب شماره (1) مینامیم. مقدار بسیار کمی آب را با استفاده از اسپری آبپاش یا قطرهچکان، درون مکعب (1) و روی مخلوط حبههای قند و شکر بریزید؛ به گونهای که مقدار کمی رطوبت ایجاد شود. مکعب (1) را در مجاورت گرمکن الکتریکی قرار دهید تا آب آن به سرعت تبخیر شود. پس از تبخیر آب، حبههای قند و شکرها به یکدیگر میچسبند.
در مکعب دیگر که آن را مکعب (2) مینامیم، ابتدا حبههای قند را به صورت منظم کنار یکدیگر قرار دهید. البته آنها را کاملاً به یکدیگر نچسبانید تا فضاهایی خالی بین آنها وجود داشته باشد. سپس مقداری شکر روی آن بریزید به گونهای که علاوه بر پر شدن فضاهای خالی، روی حبههای قند نیز مقداری شکر قرار گیرد. سپس ردیف دیگری از حبههای قند را روی شکرها بچینید و دوباره بر روی آن مقداری شکر بریزید. مکعب (2) را نیز در مجاورت گرمکن الکتریکی قرار دهید تا آب آن به سرعت تبخیر شود.
پس از آن که مطمئن شدید آب درون هر دو مکعب (1) و (2) کاملاً تبخیر شده است، پوشش مقوایی آنها را به آرامی جدا کنید. اکنون دو مکعب بزرگ به اضلاع 5×5×10 سانتیمتر دارید که از مخلوط حبههای قند و شکر تشکیل شده است (شکل 4).

شکل 4. مکعب قندی 1 (سمت چپ) و مکعب قندی 2 (سمت راست)
1- چه تفاوتی بین ساختار دو مکعب (1) و (2) وجود دارد؟
2- فکر میکنید ساختار کدام مکعب (1) یا (2) به آن چه در فناوری نانو مطرح میشود، نزدیکتر است؟
3- آیا خواص مکعب (1) با مکعب (2) تفاوتی دارد یا خیر؟
برای یافتن پاسخ پرسشهای بالا، ادامه مقاله را با دقت بیشتر بخوانید.
2.2. میکرو یا نانو؟
در مکعب (1) ما با تودهای از مواد سر و کار داریم. مخلوطی از حبههای قند و شکر که به صورت کاملاً بینظم و تصادفی در کنار یکدیگر قرار گرفتهاند. هنگام ساختن مکعب (1) با تک تک حبههای قند سر و کار نداشتیم. یعنی اصلاً به آن دسترسی نداشتیم (چون حبههای قند و شکرها را با هم مخلوط کردیم و مخلوط حاصل را به صورت تودهای درون مکعب (1) ریختیم، بنابراین، به تک تک حبههای قند دسترسی نداشتیم).
در مکعب (2) با قرار دادن تک تک حبههای قند در مجاورت یکدیگر، مکعب را ساختیم. یعنی به همه حبههای قند دسترسی داشتیم.
تفاوت در ساختار دو مکعب موجب شده است که بعضی از خواص مکعب (2) با مکعب (1) متفاوت باشد. مثلاً میتوان شکنندگی آنها را با یکدیگر مقایسه کرد. مکعب (2) که دارای ساختار منظمتری است در مقابل ضربه و نیرو مقاومتر و سختتر از مکعب (1) است که ساختار نامنظمی دارد.
اگر حبههای قند را به اتمها (یا مولکولهای) تشکیلدهنده یک ماده تشبیه کنیم، شکرهای بین آنها نقش پیوندهای بین اتمی (بین مولکولی) را دارند. همانطور که حتماً میدانید اندازه اتمها تقریباً 10-10 متر یا به اصطلاح، یک آنگستروم است. اندازه مولکولها هم بسته به این که از چند اتم تشکیل شدهاند و ساختار آنها چگونه است، متفاوت هستند. فاصله بین اتمها (یا مولکولها) در پیوندهای بین اتمی (یا بین مولکولی) نیز با توجه به حالت ماده متفاوت است. در جامدات و مایعات فاصله بین اتمی (یا بین مولکولی) تقریباً 10-10 متر است. دقت کنید که این اعداد چه قدر به ابعاد نانو یعنی 9-10 متر نزدیک است.
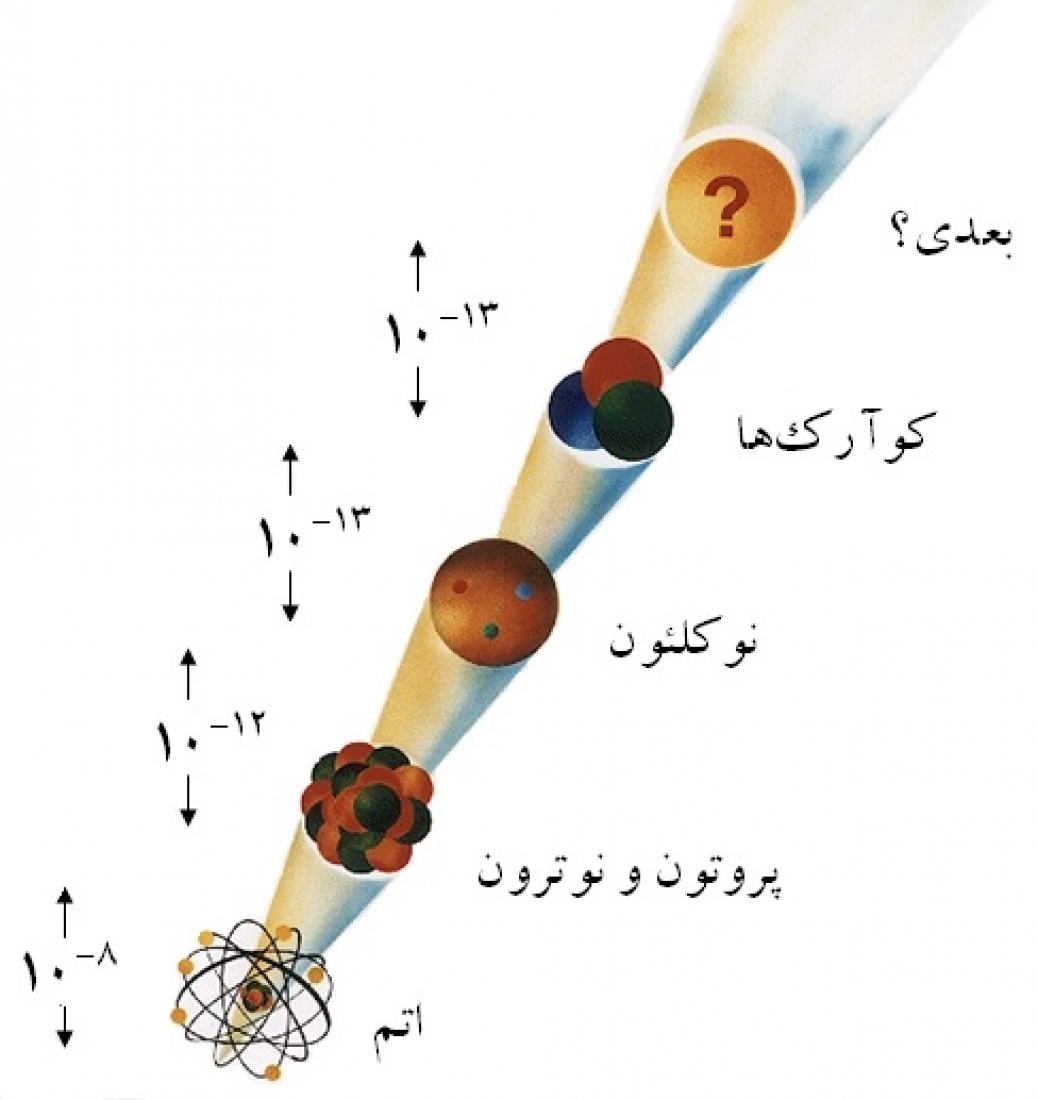
حال که با استفاده از فناوری نانو دسترسی به خواص جدید ممکن میشود، آیا حرکت به سمت فناوریهای کوچکتر نیز مفید است؟ برای پاسخ به این پرسش دقت کنید که اندازه اتمها در حدود 10-10 متر است. اگر بخواهیم به سمت فناوریهای کوچکتر از نانو حرکت کنیم، یعنی باید وارد محدوده اتم شویم. محدوده اتم یعنی محدوده الکترونها، پروتونها، نوترونها و سایر ذرات زیراتمی. یعنی مثلاً ما با استفاده از این ذرات زیراتمی ابتدا یک اتم بسازیم و سپس با کنار یکدیگر قرار دادن اتمها، موادی را با خواص جدید بنا کنیم.
لازم است توجه کنیم نخست آنکه، ما در طبیعت، ذرات زیراتمی مانند الکترون، پروتون و نوترون را به صورت جداگانه نمییابیم. یعنی این ذرات، درون اتمها قرار دارند و برای دسترسی به آنها باید به محدوده درون اتمها وارد شویم. ثانیاً ورود به محدوده درون اتمها معمولاً بسیار گران و پرهزینه است. اگر چه این کار امروزه در بعضی از آزمایشگاههای پیشرفته فیزیک انجام میشود. اما به نظر نمیرسد که در زندگی روزمره کاربرد چندانی داشته باشد. ثالثاً ما میخواهیم با کنار یکدیگر قرار دادن ذرات زیراتمی نظیر الکترون، پروتون و نوترون، اتمها را بسازیم. در حالی که طبیعت، بسیاری از اتمها را در اختیار ما قرار داده است.
ورود به محدوده کوچکتر از نانو (مثلاً محدوده پیکو یا همان 12-10 متر) مانند آن است که بخواهیم ابتدا حبههای قند را کوچکتر کنیم و سپس قطعات حاصل را به یکدیگر متصل کنیم و با حبههای قند حاصل، مکعب نهایی را بسازیم. طبیعی است کار کردن با همان حبههای قند اولیه را نسبت به این که ابتدا حبههای قند را کوچکتر کنیم و سپس دوباره به یکدیگر متصل کنیم، ترجیح میدهیم.
البته توجه به این نکته نیز خالی از لطف نیست که امروزه با استفاده از روشهای دقیق و فناوریهای بسیار گران و پیشرفته، دهها عنصر مصنوعی ساخته شده است که بعضی از آنها در صنایع گوناگون و مخصوصاً توسعه دانش و فناوری کاربرد دارد. لازم به ذکر است که عناصر مصنوعی به دلیل تراکم بسیار ذرات زیراتمی بسیار ناپایدار هستند. یعنی عمر آنها در حدود کسری از ثانیه است.
آن چه فناوری نانو را از چنین فناوریهایی متمایز میکند، گستردگی بسیار زیاد فناوری نانو در همه صنایع از مهندسی الکترونیک، مکانیک، کامپیوتر و هوافضا گرفته تا کشاورزی و دامپروری و حتی علوم پزشکی، داروسازی و زیستفناوری است.