آموزش پیشرفتهآموزش نانو
میکروفلوئیدیک – بخش اول

میکروفلوئیدیک، سیستمهای مهندسی شده به منظور دستکاری، کنترل دقیق، پردازش و تجزیه و تحلیل حجم کوچکی از سیال را توصیف میکند. تراشههای میکروفلوئیدیک وکنترل سیال در حجم کوچک، منجر به حل بسیاری از مشکلات و چالشها در علوم شیمی، پزشکی و بیولوژی شده است. انتقال سیال، جداسازی، تشکیل و تقسیم قطرات، مخلوط کردن سیالهای مختلف، بررسی وقوع واکنشهای شیمیایی در حجم کم از جمله کاربردهای میکروفلوئیدیک میباشد. توسعه میکروفلوئیدیک در ساخت آزمایشگاه روی تراشه، امکان تجزیه و تحلیل سریع و دقیق بدون نیاز به حضور نیروی متخصص را فراهم میآورد.
این مقاله شامل سرفصلهای زیر میباشد.
- مقدمه
- تاریخچه
- انواع سیستمهای میکروفلوئیدیک
- ساخت میکروکانالها
1- مقدمه:
به فناوری که امکان بررسی و پردازش نمونههایی با حجم کم(18-10-9-10 لیتر)، با استفاده از حرکت سیال درکانالهایی با ابعاد چند میکرومتر تا چندصد میکرومتر را فراهم میکند، میکروفلوئیدیک میگویند. حرکت خون در مویرگهای بدن انسان نمونهای از سیستم میکروفلوئیدیک میباشد. میکروفلوئیدیک یک علم بین رشتهای محسوب میگردد که رشتههای مختلفی چون پزشکی، فیزیک، زیست شناسی، علم مواد، مهندسی مکانیک و الکترونیک را درگیر میکند. چهار عامل آنالیز مولکولی، دفاع زیستی، زیستشناسی مولکولی و میکرو الکترونیک، انگیزههای اصلی در ظهور علم میکروفلوئیدیک هستند[1, 2].
میکروکانالها را میتوان بر بسترهای مختلفی چون شیشهها، پلیمرها، پلاستیک، سرامیک و فلزات ایجاد کرد. رفتار سیال در مقیاس میکرو متفاوت از مقیاس ماکرو است. جرم حرارتی کم و نسبت سطح به حجم بزرگ منجر به انتقال سریع حرارت و کنترل دقیق دمایی بیشتر میشود. علاوه بر این، از بین رفتن تجمع حرارتی موجب جلوگیری از واکنشهای شیمیایی ناخواسته میگردد. کوچک بودن کانالها به وضوح نشان از کاهش حجم نمونه مورد نیاز است. کاهش حجم منجر به کاهش تولید ضایعات، کاهش زمان آنالیز و همچنین افزایش دقت و امکان تکرارپذیری بیشتر میگردد. مزیت قابل توجه میکروفلوئیدیک، توانایی تجمع تعداد زیادی از قطعات متعدد با عملکردهای مختلف (به عنوان مثال میکرو پمپ، میکرو دریچه، میکرو میکسر فعال و غیرفعال) روی یک تراشه با مساحت بسیار کم است که امکان انجام عملیات پیچیده را ممکن میکند. با این قابلیت، عملیات به صورت کاملا خودکار انجام شده و به طور قابل توجهی باعث افزایش توان، بهبود تکرارپذیری و کاهش نیروی انسانی میگردد[1].
راه اندازی یک سیستم میکروفلوئیدیک یکپارچه که قادر به انجام فرایندهای زیستی یا شیمیایی (از نمونه برداری تا بازخوانی مستقیم و تجزیه و تحلیل خروجی) میباشد، چشم اندازی از یک آزمایشگاه قابل حمل را فراهم میآورد که کوچکتر از یک تلفن همراه است و از آن به عنوان آزمایشگاه روی یک تراشه یاد میشود. این تکنولوژی Micro Electro Mechanical System(MEMS) نامیده میشود[3].
به طور خلاصه مزیتهای سیستمهای میکروفلوئیدیک نسبت سیستمهای با حجم بالا به شرح زیر است[4]:
-در کانالهای میکروفلوئیدیک، انتشار کند است، بنابراین فاصله کمتری برای وقوع برهمکنش نیاز خواهد بود.
-ابعاد کانال کوچکتر، منجر به کوچک شدن حجم نمونه (فمتولیتر تا نانولیتر) و در نتیجه کاهش مقدار نمونه یا معرف های مورد نیاز برای آزمایش و آنالیز میگردد.
– کاهش ابعاد منجر به تولید دستگاههای قابل حمل میشود.
– استفاده از میکروفلوئیدیک امکان ادغام چندین فرآیند (مانند برچسبزدن، خالصسازی، جداسازی و تشخیص) در یک تراشه را فراهم میکند.
میکروکانالها را میتوان بر بسترهای مختلفی چون شیشهها، پلیمرها، پلاستیک، سرامیک و فلزات ایجاد کرد. رفتار سیال در مقیاس میکرو متفاوت از مقیاس ماکرو است. جرم حرارتی کم و نسبت سطح به حجم بزرگ منجر به انتقال سریع حرارت و کنترل دقیق دمایی بیشتر میشود. علاوه بر این، از بین رفتن تجمع حرارتی موجب جلوگیری از واکنشهای شیمیایی ناخواسته میگردد. کوچک بودن کانالها به وضوح نشان از کاهش حجم نمونه مورد نیاز است. کاهش حجم منجر به کاهش تولید ضایعات، کاهش زمان آنالیز و همچنین افزایش دقت و امکان تکرارپذیری بیشتر میگردد. مزیت قابل توجه میکروفلوئیدیک، توانایی تجمع تعداد زیادی از قطعات متعدد با عملکردهای مختلف (به عنوان مثال میکرو پمپ، میکرو دریچه، میکرو میکسر فعال و غیرفعال) روی یک تراشه با مساحت بسیار کم است که امکان انجام عملیات پیچیده را ممکن میکند. با این قابلیت، عملیات به صورت کاملا خودکار انجام شده و به طور قابل توجهی باعث افزایش توان، بهبود تکرارپذیری و کاهش نیروی انسانی میگردد[1].
راه اندازی یک سیستم میکروفلوئیدیک یکپارچه که قادر به انجام فرایندهای زیستی یا شیمیایی (از نمونه برداری تا بازخوانی مستقیم و تجزیه و تحلیل خروجی) میباشد، چشم اندازی از یک آزمایشگاه قابل حمل را فراهم میآورد که کوچکتر از یک تلفن همراه است و از آن به عنوان آزمایشگاه روی یک تراشه یاد میشود. این تکنولوژی Micro Electro Mechanical System(MEMS) نامیده میشود[3].
به طور خلاصه مزیتهای سیستمهای میکروفلوئیدیک نسبت سیستمهای با حجم بالا به شرح زیر است[4]:
-در کانالهای میکروفلوئیدیک، انتشار کند است، بنابراین فاصله کمتری برای وقوع برهمکنش نیاز خواهد بود.
-ابعاد کانال کوچکتر، منجر به کوچک شدن حجم نمونه (فمتولیتر تا نانولیتر) و در نتیجه کاهش مقدار نمونه یا معرف های مورد نیاز برای آزمایش و آنالیز میگردد.
– کاهش ابعاد منجر به تولید دستگاههای قابل حمل میشود.
– استفاده از میکروفلوئیدیک امکان ادغام چندین فرآیند (مانند برچسبزدن، خالصسازی، جداسازی و تشخیص) در یک تراشه را فراهم میکند.
2-تاریخچه:
تاریخچه میکروفلوئیدیک به دهه 1950 در تولید چاپگرهای جوهر افشان باز میگردد. مکانیزم این چاپگرها مبتنی بر لولههای بسیار کوچکی است که جوهر را برای چاپ حمل میکنند[5]. علارغم اینکه در دهه 1970، یک کروماتوگراف گازی کوچک روی یک ویفر سیلیکونی ساخته شد، فعالیت زیادی در زمینه میکروفلوئیدیک انجام نشد[6]. آندریاس مانز، یکی از اولین کسانی بود که از فناوری ریزتراشه در زمینه شیمی برای کوچک کردن یک آزمایشگاه به اندازه یک تراشه در دهه 90 استفاده کرد . در سال 1990، او مقالهای منتشر کرد که در آن مفهوم کوچکسازی شده «سیستم آنالیز شیمیایی کل» را که به اختصار «μ-TAS» نامیده میشود، برای سنجش شیمیایی معرفی کرد. وایتسایدز و همکارانش در سال 1998ساخت میکروکانال با استفاده از PDMS انجام شد[7]. فایر و همکارانش در سال 2000 سیستم میکروفلوئیدیک دیجیتال را معرفی کرد. در سال 2004 اولین ساختار میکروفلوئیدیک مبتنی بر کاغذ توسط وایتسایدز معرفی شد. میکروفلوئیدیک به سرعت در حال رشد است و باتوجه به کاربردهای فراوان پتانسیل قوی برای توسعه دارد[8]. شکل1 تاریخچه میکروفلوئیدیک را به صورت خلاصه نمایش میدهد.
3- انواع سیستمهای میکروفلوئیدیک:
سیستمهای میکروفلوئیدیک را براساس پارامترهای مختلفی چون نیرو، نوع سیال و نوع ورودی دستهبندی میکنند. به عنوان مثال، سیستمهای میکروفلوئیدیک براساس منبع نیروی اعمالی به دو گروه فعال و منفعل تقسیمبندی میشوند. در سیستمهای فعال، حرکت سیال و چیدمان ذرات، تابع نیروی اعمالی است و در سیستمهای منفعل حرکت سیال به هندسه کانال و نیروی هیدرودینامیکی ذاتی وابسته است.کنترل ذرات در سیستمهای فعال بسیار دقیقتر است[9-11]. به طور کلی سیستمهای میکروفلوئیدیک به چند دسته اصلی تقسیم میشود که شامل میکروفلوئیدیک با جریان پیوسته، قطرهای، دیجیتال و مبتنی بر کاغذ میباشند.
3-1- میکروفلوئیدیک با جریان پیوسته(continues flow ):
در میکروفلوئیدیک جریان پیوسته، سیال در میکروکانالها به صورت پیوسته جریان دارد.کنترل و دستکاری سیال توسط یک منبع خارجی مانند میکرو پمپها یا منبع داخلی مانند نیروی مویینگی انجام میشود. میکروفلوئیدیک پیوسته یک ابزار کارامد برای به دام انداختن یا جداسازی میکروذرات جامد[12, 13]، سلولها[14] یا حتی مولکولهای DNA [15] است. این نوع از میکروفلوئیدیک کنترل خوبی بر ویژگیهای جریان میدهد ولی برای کاربردهایی که نیاز به انعطافپذیری بالا یا کنترل سیال دارند، مناسب نیست. شکل 2 شماتیک میکروفلوئیدیک با جریان پیوسته را نمایش میدهد.
3-2- میکروفلوئیدیک قطرهای(droplet-based or segmented flow):
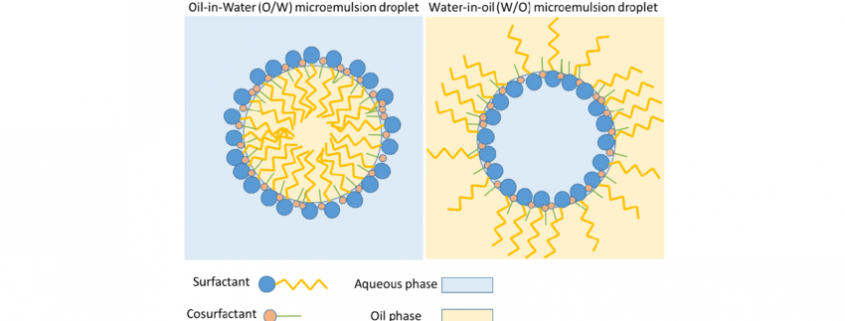
در میکروفلوئیدیک قطرهای، سیال شامل دو یا چند فاز غیرقابل امتزاج (مانند آب و روغن) است که در تماس با یکدیگر هستند. فازها در کنار یکدیگر حرکت کرده و در محل اتصال در مسیرکانال، یک از فازها به قطرات مجزا شکسته میشوند. با بهرهگیری از میدانهای جریان تولید شده، توسط هندسه خاص اتصالات، قطرات با کنترل کامل بر روی حجم و ساختارشان در نرخ های بالا تا 20000 تعداد بر ثانیه تولید میشوند[17]. به عبارت دیگر، جریان قطرهای با تشکیل قطرات ریز مجزا، در یک جریان پیوسته غیرقابل امتزاج در میکروکانال، ایجاد میشود. یکی از مهم ترین مزایای سیستمهای میکروفلوئیدیکی قطرهای این است که هر قطره میتواند به صورت جداگانه کنترل شوند و به عنوان یک میکرو راکتور فردی عمل کند، به صورت جداگانه انتقال یافته با قطره دیگر مخلوط شود و یا اینکه قطرات به قطرات کوچکتری تقسیم شده و مورد تجزیه وتحلیل قرار گیرند. انجام تجزیه وتحلیل کمی جمعیت سلولی تا سطح تکسلول با سیستمهای میکروفلوئیدیکی قطرهای منجر به شناسایی سلولهای نادر و برهمکنشهای پروتئین-پروتئین شده است[18]. شکل 3 تصویر دو مدل مختلف از سیستمهای میکروفلوئیدیک قطرهای را نمایش میدهد. تصویر الف روش نیروی برشی را نمایش میدهد. در این سیستم، تعادلی بین روغن و نرخ محلول آبی شکل گرفته و دو فاز ورودی در یک تقاطع (معمولا به شکل T) به یکدیگر میرسند. همانطور که در شکل3 مشخص است، ورودی محلول آبی میتواند بیش از یکی باشد. در گروهی دیگر از سیستمهای میکروفلوئیدیک، کنترل سیال و قطرهها با هندسه کانال انجام میشود[19]. شکل (ب) تصویری از این نوع سیستم را به نمایش گذاشته است. سیال از سه ورودی وارد میکروکانال شده و پس از آنکه به روزنه باریک میرسند به دلیل حبس شدن، سیال قطعه قطعه شده و قطرات تشکیل میشوند. در این ساختار میتوان با کنترل نرخ جریان ورودی، قطرات با سایزهای متفاوت و حتی کوچکتر از قطر روزنه ایجاد کرد[20].
میکروفلوئیدیک قطرهای کاربردهای زیاد دارد که شکلگیری غشای مصنوعی، آنالیز تک سلول، تکثیر DNA و تولید نانوذرات از جمله این کاربردها هستند[2].
3-3-میکروفلوئیدیک دیجیتالی:
میکروفلوئیدیک دیجیتال یک فناوری پیشرفته برای جابجایی مایعات است که به طور دقیق قطرات نانولیتری را برای انجام پروتکلهای پیچیده آزمایشگاهی دستکاری میکند. میکروفلوئیدیک دیجیتال یکی از زیرمجموعههای میکروفلوئیدیک قطرهای است که بر مبنای electro wetting (توانایی تعدیل ترشوندگی یک سطح بر اثر اعمال ولتاژ) عمل میکند. شکل 4 تصویر قرارگیری قطره آب بر روی سطح آبگریز قبل و بعد از اعمال ولتاژ را نمایش میدهد. در حالت طبیعی وقتی قطره بر روی سطح آبگریز قرار بگیرد، برای کاهش سطح تماس به شکل کروی قرار میگیرد. اعمال ولتاژ بین یک قطره و یک الکترود عایق میتواند باعث پخش شدن قطره بر روی سطح شود.
در میکروفلوئیدیک دیجیتال، سیگنالهای الکتریکی به مجموعهای از الکترودها اعمال میشوند تا اندازه و موقعیت هر قطره را مشخص کنند. قطرات با روشن و خاموش کردن ولتاژ متوالی در الکترودهای مجاور حرکت میکنند. از همین مکانیزم میتوان برای پخش، ادغام و مخلوط کردن قطرات با استفاده از سیگنالهای الکتریکی استفاده کرد. در میکروفلوئیدیک دیجیتال میتوان اجزای حرارتی، مغناطیسی و نوری را برای انجام فرایندهای شیمیایی و زیستی بهکار برد. در این سیستمهای خیلی از فرایندهایی که دستی انجام میشود به صورت خودکار انجام میگردد. این موضوع امکان حفاظت از نمونههای گرانبها را فراهم کرده و خطای انسانی را به طور قابل توجهی کاهش میدهد[21, 22].
3-4- میکروفلوئیدیک مبتنی برکاغذ:
از زمان پاپیروسها، سلولز نقش مهمی در فرهنگ انسان، ایفا کرده است. امروزه این محصول باستانی کاربردهای علمی جدیدی در بخش رو به گسترش فناوری مبتنی بر کاغذ پیدا کرده است. استفاده از کاغذ در انجام آزمایشها به قرنها قبل برمیگردد، اما استفاده مدرن از کاغذ از دهه ١٩۴٠ آغاز شد. در سال ٢٠٠٧ اولین سیستم میکروفلوئیدیکی مبتنی بر کاغذ توسط جورج و همکارانش معرفی گردید[23].
کاغذ از الیاف سلولزی که به طور نامنظم در یگدیگر تنیده و فشرده شده تشکیل شده است. با توجه به اینکه کاغذ مادهای زیست سازگار و کمهزینه است در میکروفلوئیدیک مورد توجه قرار گرفته است. در سیستمهای مبتنی بر کاغذ، سیال با استفاده از مویینگی بر روی سطح جریان پیدا میکند و نیازی به نیروی خارجی وجود ندارد. امکان طراحی انواع هندسه دوبعدی و سه بعدی با استفاده از کاغذ نیز، از جمله علل محبوبیت این گروه از سیستمهاست. علاوه بر این، دستگاه های تشخیص ساده مبتنی بر کاغذ نیازی به سخت افزار یا مهارت فنی خاصی ندارند[24]. اندازه و نوع تخلخل، استحکام، مساحت سطح، واکنش شیمیایی و رنگ از جمله عوامل تاثیرگذار بر کارایی و دقت سیستمهای میکروفلوئیدیک مبتنی بر کاغذ میباشد[23]. شکل 5 شماتیک یک نمونه سیستم میکروفلوئیدیک مبتنی بر کاغذ را نمایش میدهد.
کاغذ از الیاف سلولزی که به طور نامنظم در یگدیگر تنیده و فشرده شده تشکیل شده است. با توجه به اینکه کاغذ مادهای زیست سازگار و کمهزینه است در میکروفلوئیدیک مورد توجه قرار گرفته است. در سیستمهای مبتنی بر کاغذ، سیال با استفاده از مویینگی بر روی سطح جریان پیدا میکند و نیازی به نیروی خارجی وجود ندارد. امکان طراحی انواع هندسه دوبعدی و سه بعدی با استفاده از کاغذ نیز، از جمله علل محبوبیت این گروه از سیستمهاست. علاوه بر این، دستگاه های تشخیص ساده مبتنی بر کاغذ نیازی به سخت افزار یا مهارت فنی خاصی ندارند[24]. اندازه و نوع تخلخل، استحکام، مساحت سطح، واکنش شیمیایی و رنگ از جمله عوامل تاثیرگذار بر کارایی و دقت سیستمهای میکروفلوئیدیک مبتنی بر کاغذ میباشد[23]. شکل 5 شماتیک یک نمونه سیستم میکروفلوئیدیک مبتنی بر کاغذ را نمایش میدهد.
4- ساخت میکروکانالها:
طراحی و ساخت میکروکانالها در میکروفلوئیدیک از اهمیت بسیار بالایی برخوردار است. روش های مختلفی برای ساخت میکروکانالها وجود دارد که مهمترین آنها شامل تکنیکهای زیر هستند:
1- photolithography/optical lithography
2- soft lithography
3- x-ray lithography
4- Laser photo ablution or laser micromachining
hot embossing -5
6- injection modeling
1- photolithography/optical lithography
2- soft lithography
3- x-ray lithography
4- Laser photo ablution or laser micromachining
hot embossing -5
6- injection modeling
4-1- لیتوگرافی:
لیتوگرافی یک واژه یونانی است که از دو قسمت لیتوس (Lithos) به معنای سنگ و گرافی (Graphia) به معنای نوشتن و حکاکی کردن، تشکیل شده است. با ترجمه کلمه به کلمه این واژه به صورت حکاکی بر روی سنگ معنی میشود[26]. این روش شامل تشکیل یک طرح لیتوگرافی از یک الگو روی یک ماده الکترونیک و انتقال آن طرح به مادهای دیگر جهت تولید یک ابزار الکترونیکی یا نوری می باشد[27-29].
کوچک شدن اجزا در سیستمها و مدارهای میکروالکترونیک باعث رشد چشمگیر این صنعت در سالهای اخیر شده است. کوچک شدن ابعاد این اجزا میتواند باعث کاهش مصرف مواد اولیه و انرژی، کاهش قیمت تمام شده این قطعات و افزایش سرعت و بازدهی آنها گردد. بنابراین ساخت و توسعه ابزار الکترونیک با ابعاد کوچکتر و سرعت و بازدهی بیشتر روز به روز اهمیت بیشتری پیدا کرده است.
روش لیتوگرافی یکی از روشهای متداول برای ساخت مدارهای الکترونیکی است. با کمک این روش میتوان ساختارهایی با دقت و ابعاد 10 نانومتری ساخت. پیداکردن تکنیکهایی که با کمک آنها بتوان از این روش برای تولید صنعتی این قطعات استفاده کرد، موضوع مطالعه بسیاری از محققین است.
به طور کلی میتوان گفت که در تمامی تکنیکهای لیتوگرافی، ابتدا طرحی از یک الگو بر روی یک ماده تشکیل میشود و سپس آن طرح به ماده دیگری جهت تولید محصول مورد نظر منتقل میگردد.
کوچک شدن اجزا در سیستمها و مدارهای میکروالکترونیک باعث رشد چشمگیر این صنعت در سالهای اخیر شده است. کوچک شدن ابعاد این اجزا میتواند باعث کاهش مصرف مواد اولیه و انرژی، کاهش قیمت تمام شده این قطعات و افزایش سرعت و بازدهی آنها گردد. بنابراین ساخت و توسعه ابزار الکترونیک با ابعاد کوچکتر و سرعت و بازدهی بیشتر روز به روز اهمیت بیشتری پیدا کرده است.
روش لیتوگرافی یکی از روشهای متداول برای ساخت مدارهای الکترونیکی است. با کمک این روش میتوان ساختارهایی با دقت و ابعاد 10 نانومتری ساخت. پیداکردن تکنیکهایی که با کمک آنها بتوان از این روش برای تولید صنعتی این قطعات استفاده کرد، موضوع مطالعه بسیاری از محققین است.
به طور کلی میتوان گفت که در تمامی تکنیکهای لیتوگرافی، ابتدا طرحی از یک الگو بر روی یک ماده تشکیل میشود و سپس آن طرح به ماده دیگری جهت تولید محصول مورد نظر منتقل میگردد.
1-1-4- لیتوگرافی نوری:
لیتوگرافی نوری در اصل تعمیم یافته عکاسی است. ابتدا چیزی شبیه به نگاتیو عکاسی از طرح کانالها تهیه میگردد. به این نگاتیو در لیتوگرافی فوتوماسک گفته و برای تکثیر طرح روی یک ماده نیمههادی به کار میرود. تهیه نگاتیو به سادگی عکاسی نیست، اما با داشتن آن میتوان به راحتی هزاران نسخه تکثیر کرد. برای ساخت این ماسک ابتدا طرح مورد نظر با استفاده از نرم افزارهای گرافیکی مخصوص مانند اتوکد در ابعاد واقعی، طراحی و سپس بر روی صفحه شفافی چاپ میگردد. بعد تهیه فوتوماسک لیتوگرافی نوری آغاز میگردد.
زیرلایههای استفاده شده در ساخت قالب از جنس پلیمر PMMA (پلکسی تجاری) می باشند. این پلیمر به دلیل داشتن مزیتهایی از قبیل فراوانی، استحکام زیاد و قیمت مناسب، نسبت به زیرلایههای سیلیکونی، مورد توجه می باشد. پس از انتخاب زیرلایه و تمیز کردن سطح آن، لایه نشانی فوتورزیست انجام میگیرد. فوتورزیست موادی حساس به نور هستند، به طوریکه نوردهی به فوتورزیست باعث تغییر حل شوندگی آن در محلول میگردد. فوتورزیستها یکی از پرکاربردترین مواد در ساخت قطعات میکروالکترومکانیک و براساس نوع واکنش شیمیایی با نور، به دو دسته مثبت و منفی تقسیم میشوند.
فوتورزیست مثبت، موادی هستند که ساختار شیمیایی آنها بعد از نوردهی با نور فرابنفش ناپایدار شده و با شستو شو زیرلایه، از روی سطح حذف میشوند[30]. در مواد فوتورزیست منفی، نوردهی موجب تشکیل ساختاری پایدار و محکم میگردد به صورتیکه شستوشو زیرلایه، آسیبی به آن وارد نمیکند. به عنوان مثال، ماده SU-8 یک ماده فوتورزیست منفی است[31].
در شکل 6 شماتیک لیتوگرافی نوری در دو حالت فوتورزیست مثبت و منفی نمایش داده شده است. وقتی نور به سطح فوتورزیست میتابد، اگر فوتورزیست مثبت باشد، نقاطی که ماسک پوشش نمیدهد و در معرض تابش قرار میگیرد، بعد از شستشو حذف میشود، اما فوتورزیست منفی، برعکس عمل میکند. به عبارت دیگر، بعد از تابش نور به فوتورزیست مثبت، ساختاری مشابه با ساختار ماسک و در فوتورزیست منفی، ساختاری معکوس با ساختار ماسک ایجاد میشود.
زیرلایههای استفاده شده در ساخت قالب از جنس پلیمر PMMA (پلکسی تجاری) می باشند. این پلیمر به دلیل داشتن مزیتهایی از قبیل فراوانی، استحکام زیاد و قیمت مناسب، نسبت به زیرلایههای سیلیکونی، مورد توجه می باشد. پس از انتخاب زیرلایه و تمیز کردن سطح آن، لایه نشانی فوتورزیست انجام میگیرد. فوتورزیست موادی حساس به نور هستند، به طوریکه نوردهی به فوتورزیست باعث تغییر حل شوندگی آن در محلول میگردد. فوتورزیستها یکی از پرکاربردترین مواد در ساخت قطعات میکروالکترومکانیک و براساس نوع واکنش شیمیایی با نور، به دو دسته مثبت و منفی تقسیم میشوند.
فوتورزیست مثبت، موادی هستند که ساختار شیمیایی آنها بعد از نوردهی با نور فرابنفش ناپایدار شده و با شستو شو زیرلایه، از روی سطح حذف میشوند[30]. در مواد فوتورزیست منفی، نوردهی موجب تشکیل ساختاری پایدار و محکم میگردد به صورتیکه شستوشو زیرلایه، آسیبی به آن وارد نمیکند. به عنوان مثال، ماده SU-8 یک ماده فوتورزیست منفی است[31].
در شکل 6 شماتیک لیتوگرافی نوری در دو حالت فوتورزیست مثبت و منفی نمایش داده شده است. وقتی نور به سطح فوتورزیست میتابد، اگر فوتورزیست مثبت باشد، نقاطی که ماسک پوشش نمیدهد و در معرض تابش قرار میگیرد، بعد از شستشو حذف میشود، اما فوتورزیست منفی، برعکس عمل میکند. به عبارت دیگر، بعد از تابش نور به فوتورزیست مثبت، ساختاری مشابه با ساختار ماسک و در فوتورزیست منفی، ساختاری معکوس با ساختار ماسک ایجاد میشود.
لایه فوتورزیست با استفاده از لایه نشانی چرخشی روی زیرلایه نشانده میشود. برای این منظور زیرلایه روی یک صفحه چرخان قرار داده شده و سپس SU-8 روی زیرلایه ریخته میشود، سپس صفحه با چرخش و با استفاده از نیروی گریز از مرکز روی ماده را روی زیرلایه پخش میکند. ضخامت لایه فوتورزیست لایه نشانی شده با این روش به سرعت چرخش و همچنین مدت زمان چرخش بستگی دارد. بعد از لایه نشانی SU-8 روی زیرلایه مرحله پخت باید انجام شود تا حلالهای موجود در آن تبخیر شده و ساختار آماده نوردهی گردد. به این مرحله مرحله پیش پخت میگویند.
بعد از مراحل مطرح شده مرحله نوردهی فرا می رسد. برای نوردهی باید از منبع نور مناسب از نظر توان و طول موج استفاده شود. ناحیه حساسیت موادی مثل SU-8 در ناحیه فرابنفش نزدیک است. ماسک را روی زیرلایه لایه نشانی شده با SU-8 قرار داده و سپس آن را در معرض تابش فرابنفش قرار میدهیم. نور را به صورت موازی با ماسک و زیرلایه برخورد کند. نمونهها بعد از نوردهی مجدد باید پخته شوند تا ساختار نورخورده پایدار شود. این فرایند پس پخت نامیده میشود. مدت زمان پس پخت به ضخامت پلیمر لایهنشانی شده وابسته است. در شکل 7 مراحل لیتوگرافی نوری به صورت خلاصه بیان شده است.
بعد از مراحل مطرح شده مرحله نوردهی فرا می رسد. برای نوردهی باید از منبع نور مناسب از نظر توان و طول موج استفاده شود. ناحیه حساسیت موادی مثل SU-8 در ناحیه فرابنفش نزدیک است. ماسک را روی زیرلایه لایه نشانی شده با SU-8 قرار داده و سپس آن را در معرض تابش فرابنفش قرار میدهیم. نور را به صورت موازی با ماسک و زیرلایه برخورد کند. نمونهها بعد از نوردهی مجدد باید پخته شوند تا ساختار نورخورده پایدار شود. این فرایند پس پخت نامیده میشود. مدت زمان پس پخت به ضخامت پلیمر لایهنشانی شده وابسته است. در شکل 7 مراحل لیتوگرافی نوری به صورت خلاصه بیان شده است.
2-1-4- لیتوگرافی نرم:
لیتوگرافی نرم تکنیکی میکروساختاری برای ایجاد ابزار میکروفلوئیدیکی پلیمری شامل میکروکانالها، مخزنها و دریچهها برای کنترل سیال میباشد. در لیتوگرافی نرم از یک ماده پلیمر کشسان (عمدتا PDMS) برای قالبگیری طرح آماده شده در مرحله لیتوگرافی نوری استفاده میشود[32]. در مرحله لیتوگرافی نوری، قالب آماده شده و در مرحله لیتوگرافی نرم، نوبت به قالب گرفتن از طرح می باشد. شکل8 شماتیک مراحل لیتوگرافی نوری و لیتوگرافی نرم را به شکل خلاصه نمایش میدهد.
برای آمادهسازی PDMS، از دو ماده پایه و عامل پخت با نسبت مشخص استفاده میشود. ترکیب این دو ماده موجب به وجود آمدن حباب هوا میگردد که با چشم قابل روئیت هستند. پس از انجام عملیات حبابگیری، PDMS به صورت یکنواخت در داخل قالب ریخته میشود. پس از ریختن PDMS در قالب، مرحله پخت انجام شده و حلالهای موجود در محلول تبخیر میشوند. پس از مرحله پخت، PDMS حالت لاستیک به خود گرفته و طرح مورد نظر بر روی PDMS شکل میگیرد. با توجه به کاربرد مدنظر بر روی PDMS سوراخهایی به منظور ایجاد ورودی و خروجی سیال، ایجاد میگردد.
برای تبدیل طرح ایجاد شده به میکروکانال و ساخت تراشه،یک لام شیشهای بر روی PDMS طرح دار شده چسبانده میشود. برای چسباندن لام شیشهای و PDMS از دستگاه پلاسما DBD استفاده میگردد. در دستگاه پلاسما، دو سطح مدنظر، در معرض پلاسما قرار گرفته و علاوه بر از بین رفتن آلودگی سطح آنها، رادیکال های فعال بر روی این سطوح ایجاد شده و باعث ایجاد پیوند کووالانسی میگردد. در شکل 9 مراحل لیتوگرافی نرم نمایش داده شده است.
برای تبدیل طرح ایجاد شده به میکروکانال و ساخت تراشه،یک لام شیشهای بر روی PDMS طرح دار شده چسبانده میشود. برای چسباندن لام شیشهای و PDMS از دستگاه پلاسما DBD استفاده میگردد. در دستگاه پلاسما، دو سطح مدنظر، در معرض پلاسما قرار گرفته و علاوه بر از بین رفتن آلودگی سطح آنها، رادیکال های فعال بر روی این سطوح ایجاد شده و باعث ایجاد پیوند کووالانسی میگردد. در شکل 9 مراحل لیتوگرافی نرم نمایش داده شده است.
3-1-4- لیتوگرافی x-ray:
لیتوگرافی نوری ابزار غالب در ساخت میکروکانالهاست و شامل الگوبرداری از بستر با استفاده از برهمکنش پرتوهای فوتون یا ذرات با مواد است[34]. لیتوگرافی اشعه ایکس مشابه با لیتوگرافی نوری است که در بخش قبلی مطرح شد، با این تفاوت که به جای پرتو فرابنفش از اشعه پرتو ایکس استفاده میشود. برای کاهش ابعاد ساختارهای ایجادشده با لیتوگرافی نوری، طولموج نور فرودی باید کاهش یابد. پرتوهای ایکس آخرین حد طولموج به کار رفته در لیتوگرافی است که نانو لیتوگرافی را نیز ممکن ساخته است[35]. در این روش، رزولوشن لیتوگرافی نوری به حدود 15 نانومتر رسیده است. باتوجه به اینکه در لیتوگرافی پرتوایکس، به وجود لنز نیاز نیست، این یک روش ساده است و به عنوان نامزدی برای نسل بعدی لیتوگرافی در صنعت نیمههادی میباشد. در لیتوگرافی پرتو ایکس،اگر پرتو خروجی از منبع همسو نباشد، از آینه های همسوکننده یا عدسی های انکساری به جای لنزهای انکساری استفاده میشوند [34]. شکل10 طرح شماتیک لیتوگرافی x-ray را نمایش میدهد.
منابـــع و مراجــــع
۱ – Whitesides, G.M., The originsthe future of microfluidics. nature, 2006. 442(7101): p. 368-373.
۲ – Stanley, C.E., R.C. Wootton,A.J. deMello, Continuoussegmented flow microfluidics: applications in high-throughput chemistrybiology. Chimia (Aarau), 2012. 66(3): p. 88-98.
۳ – Raje, M.G.M. Raje, Micro-fluidics in Disease Diagnosis: Past, Present,Future-An Overview. Br. Biomed. Bull, 2019. 7: p. 1-10.
۴ – !!! INVALID CITATION !!!
۵ – Prakash, S.S. Kumar, Fabrication of microchannels: A review. Proceedings of the Institution of Mechanical Engineers, Part B: Journal of Engineering Manufacture, 2014. 229: p. 0954405414535581.
۶ – Nge, P.N., C.I. Rogers,A.T. Woolley, Advances in microfluidic materials, functions, integration,applications. Chemical reviews, 2013. 113(4): p. 2550-2583.
۷ – Delaquilla, A., History of Microfluidics. Elveflow, 2021.
۸ – Attia, U.M., S. Marson,J.R. Alcock, Micro-injection moulding of polymer microfluidic devices. Microfluidicsnanofluidics, 2009. 7(1): p. 1-28.
۹ – Zhang, J., et al., Fundamentalsapplications of inertial microfluidics: A review. Lab on a Chip, 2016. 16(1): p. 10-34.
۱۰ – Augustsson, P., et al., Microfluidic, label-free enrichment of prostate cancer cells in blood based on acoustophoresis. Analytical chemistry, 2012. 84(18): p. 7954-7962.
۱۱ – Warkiani, M.E., et al., Malaria detection using inertial microfluidics. Lab on a Chip, 2015. 15(4): p. 1101-1109.
۱۲ – Di Carlo, D., Inertial microfluidics. Lab on a Chip, 2009. 9(21): p. 3038-3046.
۱۳ – Gossett, D.R., et al., Inertial manipulationtransfer of microparticles across laminar fluid streams. Small, 2012. 8(17): p. 2757-2764.
۱۴ – Nam, J., et al., Continuous separation of microparticles in a microfluidic channel via the elasto-inertial effect of non-Newtonian fluid. Lab on a Chip, 2012. 12(7): p. 1347-1354.
۱۵ – Kim, J.Y., et al., Lateral migrationfocusing of colloidal particlesDNA molecules under viscoelastic flow. Lab on a Chip, 2012. 12(16): p. 2807-2814.
۱۶ – Lignos, I.G., et al., Segmented Flow Microfluidics, in Encyclopedia of Biophysics, G.C.K. Roberts, Editor. 2013, Springer Berlin Heidelberg: Berlin, Heidelberg. p. 2300-2306.
۱۷ – Kobayashi, I., K. Uemura,M. Nakajima, Formulation of monodisperse emulsions using submicron-channel arrays. ColloidsSurfaces A: PhysicochemicalEngineering Aspects, 2007. 296(1-3): p. 285-289.
۱۸ – Stanley, C.E., R.C.R. Wootton,A.J. deMello, Continuoussegmented flow microfluidics: applications in high-throughput chemistrybiology. Chimia, 2012. 66(3): p. 88-98.
۱۹ – Grigoriev, R.O., M.F. Schatz,V. Sharma, Chaotic mixing in microdroplets. Lab on a Chip, 2006. 6(10): p. 1369-1372.
۲۰ – Anna, S.L., N. Bontoux,H.A. Stone, Formation of dispersions using “flow focusing” in microchannels. Applied physics letters, 2003. 82(3): p. 364-366.
۲۱ – Berthier, J., Micro-dropsdigital microfluidics. 2012: William Andrew.
۲۲ – مهریزی, م.م.ع.ا., میکروفلوئیدیکی بر پایه کاغذ با کاربرد تشخیصی. 1398.
۲۳ – Credou, J.T. Berthelot, Cellulose: biocompatible to bioactive material. Journal of Materials Chemistry B, 2014. 2(30): p. 4767-4788.
۲۴ – Mu, X.Y.S. Zhang. FabricationApplications of Paper-Based Microfluidics. 2017.
۲۵ – Pradeep, T., Nano: the essentials: understanding nanosciencenanotechnology. 2007: McGraw-Hill Education.
۲۶ – Edelstein, A.S.R. Cammaratra, Nanomaterials: synthesis, propertiesapplications. 1998: CRC press.
۲۷ – Guo, Z.L. Tan, Fundamentalsapplications of nanomaterials. 2009: Artech House.
۲۸ – Yang, L., et al., Nano‐fabrication: A review. Journal of the Chinese Institute of Engineers, 2007. 30(3): p. 441-446.
۲۹ – Minteer, S.D., Microfluidic techniques: reviewsprotocols. Vol. 321. 2006: Springer Science & Business Media.
۳۰ – Land, K.J., et al., Low cost fabricationassembly process for re-usable 3D polydimethylsiloxane (PDMS) microfluidic networks. Biomicrofluidics, 2011. 5(3): p. 036502.
۳۱ – Ahrberg, C.D., A. Manz,B.G. Chung, Polymerase chain reaction in microfluidic devices. Lab on a Chip, 2016. 16(20): p. 3866-3884.
۳۲ – Shin-Won, K., Application of Soft Lithography for Nano Functional Devices, in Lithography, W. Michael, Editor. 2010, IntechOpen: Rijeka. p. Ch. 20.
۳۳ – Venugopal, G.S.-J. Kim, Nanolithography. 2013. p. 187-206.
۳۴ – Voves, J., Nanoelectronicsnanolithography. 2009. 10.