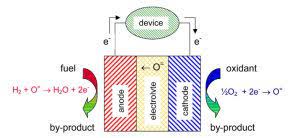
اندازهگیری نیتروژن، کربن و هیدروژن با استفاده از روش احتراق- کروماتوگرافی گازی

ترکیبات آلی اغلب از عناصر کربن، هیدروژن، نیتروژن و اکسیژن ساخته شدهاست لذا بهمنظور تعیین فرمول مولکولی ترکیبات ناشناخته و سنتزی، یا بهمنظور کنترل کیفیت محصولات در خط تولید، نیاز به یک روش سریع، تکرارپذیر وآسان برای تعیین همزمان درصد عناصر تشکیلدهنده است. پرکاربردترین روشها در این زمینه، پیرولیز سریع نمونه و بررسی گازهای حاصل از احتراق نمونه بوده و وجه مشترک در این روشها، اندازهگیری عناصر برپایه گازهای حاصل از احتراق نمونه است (کربن براساس میزان CO2، هیدروژن با H2O، نیتروژن با NOX و سولفور با SO2 تشکیل شده محاسبه میشود).
این مقاله شامل سرفصلهای زیر است:
1- مقدمه
2- کاربردهای روش
3- اصول روش
4- بهینهسازی روش
5- جمعبندی
1- مقدمه
- احتراق آنی نمونه و تزریق مخلوط همگن گازهای حاصل از احتراق و فاز متحرک؛
- قدرت اکسیدکنندگی دستگاه بهطوری که بتواند منجر به احتراق کامل نمونه شود؛
- سختی جداسازی تک مرحلهای مخلوط گازهای احتراق شامل CO2,H2O,N2 ,SO2؛
- جذب سطحی محسوس که باعث تداخل در جداسازی میشود؛
- نسبی بودن اندازهگیری یعنی مقایسه سطح زیر پیک نمونه و استاندارد؛
- پایداری سیستم و مشکلات مربوط به ناخالصیهای حاصل از افزودنیهای دستگاه احتراق.
- اندازهگیری مستقیم آب و بدون تبدیل با آشکارساز رسانش گرمایی [3]؛
- افزایش توان اکسندگی دستگاه[4]؛
- استفاده از فاز ساکن جدید در دستگاه کروماتوگرافی[5]؛
- سیستم انتگرالگیری دیجیتالی از سیگنال[6]؛
- استفاده از دستگاه نمونهگیری خودکار[7]؛
- حذف مواد شیمیایی اکسیدکننده[8].
آنالیز عنصری با این روش شامل گستره وسیعی ازترکیبات زیر است :
- دارویی و شیمیایی؛
- آلی فلزی ،برش نفتی، کاتالیستها، ترکیبات نانوساختار؛
- محصولات سنتزی؛
- پلیمری، صنایع لاستیکسازی، تفلونی؛
- ذغالسنگ و مشتقات روغنی؛
- مواد دیرگداز، گرافیت، کک، روغن سوخته.
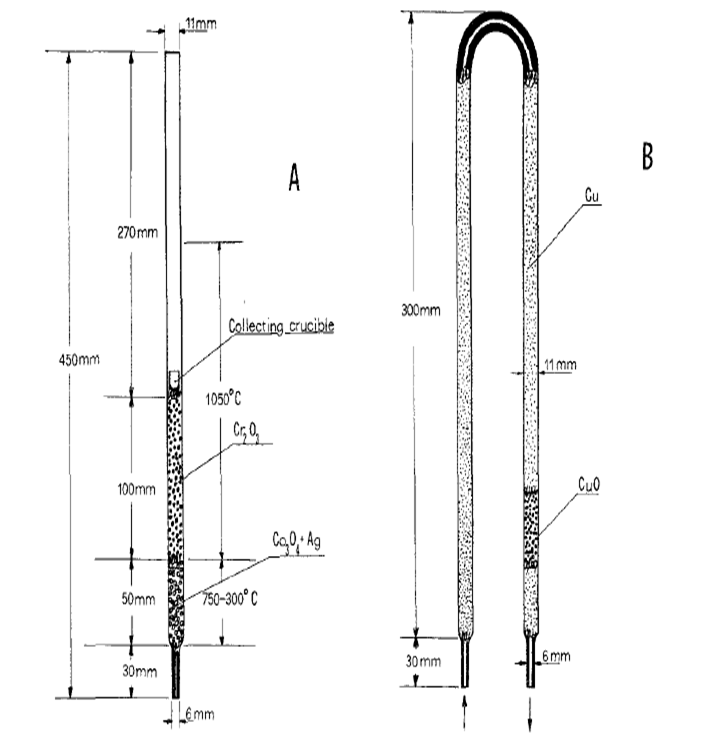
ماده موردنظر در یک ظرف فلزی (قلع، نقره، آلومینیوم) سبک وزن و قابل اکسید شدن بستهبندی شده و از طریق ورودی دستگاه به داخل یک لوله کوارتزی عمودی با دمای حدود 1200درجه سلسیوس انداخته میشود. جریان ثابتی از گاز هلیوم از درون این لوله کوارتزی که لوله احتراق نام دارد، عبور داده میشود. نمونه در حضور گاز اکسیژن بهعنوان عامل اکسنده در دمای بالای لوله احتراق، بهصورت آنی و در یک لحظه میسوزد. واکنش احتراق بهصورت معادله زیر است. ماده پرکننده لوله بر حسب نوع طراحی دستگاه، میتواند دی کرومات، اکسید نیکل یا اکسید مس باشد[4،8 و12].
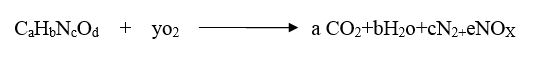
معادله (2):
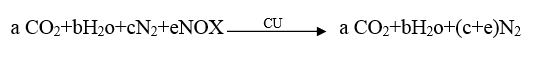
Fc:W×carbone contente/In فاکتور تصحیح کربن
FH:W×Hydrogene contente/In فاکتور تصحیح هیدروژن
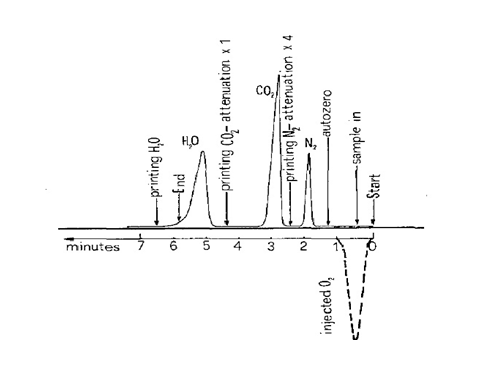
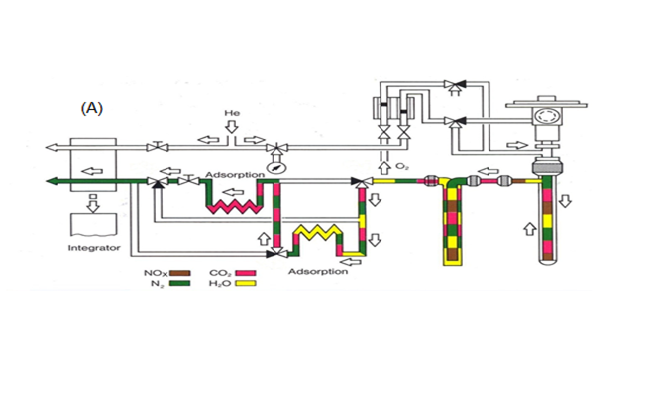
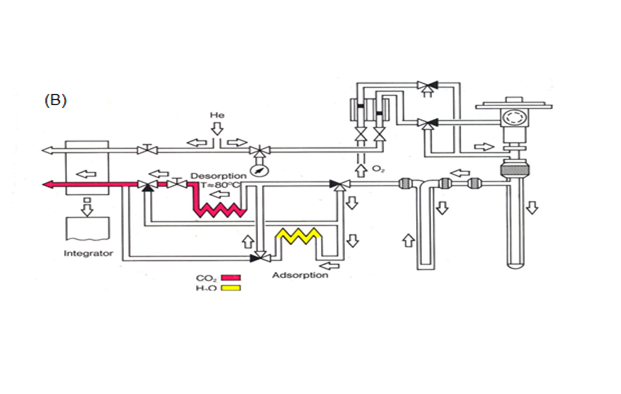
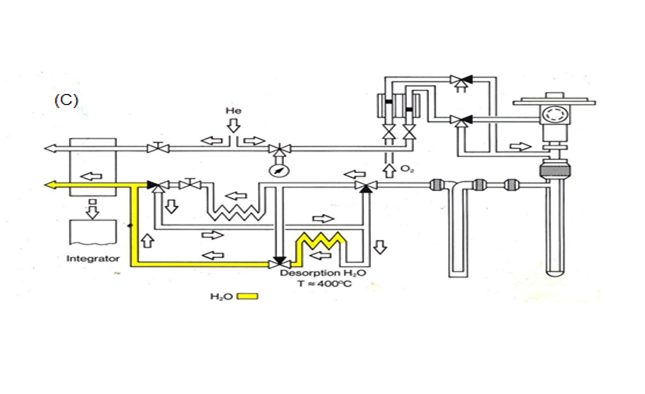
براساس تجربههای بهدست آمده حاصل از سالها تحقیق در زمینه تلفیق روش پیرولیزوکروماتوگرافی گازی عوامل قابل تغییر در این روش برای حصول نتایج دقیق و تکرارپذیر شامل میزان ماده توزین شده، خلوص گازهای بهکار رفته، نوع ظرف نمونه، کاتالیست بهکار رفته در مرحله احتراق ودمای لوله احتراق ودمای لوله احیاء است.
میزان ماده آنالیزی:
مهمترین وتاثیرگذارترین عامل در بحث دقت و تکرارپذیری نتایج، وزن نمونه است که بر حسب نوع نمونه از 0.1 میلیگرم برای ترکیبات با درصد کربن بالا، دیرگداز و پرانرژی و تا 3 میلیگرم برای نمونههای معمولی است[8]. اصل اساسی، احتراق کامل و آنی نمونه بدون اثر حافظه است.
نوع ظرف نمونه بهکار رفته:
سیستم نمونهگیری در این روش به شکل مایع و جامد است. بدیهی است آنالیز ترکیبات فرار با فشار بخار بالا میتواند به نتایج نادرست و تکرارناپذیر منجر شود؛ لذا بهمنظور به حداقل رساندن این مشکل از فویل نقره استفاده میشود ولی متاسفانه در دمای بهکار رفته اکسید نمیشود. قلع پرکاربردترین ظرف است؛ این ظرف نمونه در زمان احتراق، ابتدا ذوب و سپس بهطور کامل اکسید شده و منجر به احتراق آنی نمونه میشود. آلومینیوم در اتمسفر اکسیژن، بدون ذوب شدن، سریع اکسید میشود اما اکسید شدن قلع قدری بیشتر طول میکشد.
تنظیم دمای بهینه:
دمای لوله احتراق تعیینکننده است چرا که دمای بالا منجر به خرابی کاتالیستها شده و دمای پایین سبب احتراق ناقص نمونه، نتایج نادرست و پدیده اثر حافظه میشود. بدیهی است دمای بهینه بر حسب نمونه میتواند متفاوت باشد، گستره دمایی بهکار رفته از 900 تا 1100 درجه سلسیوس است.
دمای لوله احیاء معمولا 550 تا 600 درجه سلسیوس است؛ دمای پایین، منجر به کاهش عملکرد کاتالیستها میشود. دمای ستون کروماتوگرافی باید در حدود 150 درجه سلسیوس باشد.
نوع کاتالیست:
ترکیبات بهکار رفته بهعنوان کاتالیست احتراق باید دارای شرایط زیر باشد:
- اکسایش سریع نمونه؛
- پایداری فیزیکی وشیمیایی در دمای بالا؛
- عدم جذب سطحی گازهای احتراق؛
- مقاومت مکانیکی خوب؛
- عدم واکنش با کوارتز.
کاتالیست بهکار رفته در ستون کاهش، معمولا مس فلزی است که مهمترین مشکل در این بخش، جذب سطحی گازهای حاصل از احتراق است که هر چه دما بالا رود میزان جذب سطحی هم کاهش خواهد یافت.
5- جمعبندی
روش تعیین کربن، هیدروژن و نیتروژن موجود در نمونه براساس احتراق نمونه و جداسازی گازهای حاصل از احتراق به روش کروماتوگرافی گازی و در نهایت اندازهگیری هدایت حرارتی CO2, N2, H2O توصیه میشود. بهمنظور دستیابی به احتراق آنی همه نوع ترکیب آلی، باید از ظروف فلزی قابل اکسایش برای انتقال نمونه به لوله احتراق استفاده کرد. برای اکسایش کامل نمونه، از گاز اکسیژن و بهعنوان فاز متحرک از گاز هلیوم با خلوص بالا استفاده میشود. احتراق آنی نمونه با استفاده از کاتالیستهای اکسایش توسعهیافته، بهبود مییابد. این عوامل همانند اکسید کروم فاقد جذب سطحی و مقاوم حرارتی بوده و دانهای با سطح فعال بالا است. مس عملآوری شده با نقره بهمنظور عامل کاهنده استفاده میشود. ترکیبات گازی ناخواسته با استفاده از CO3O4 حاوی نقره حذف میشوند. اندازهگیری کمی براساس انتگرالگیری از سیگنال بهدست آمده حاصل میشود. فرآیند آنالیز با استفاده از پتانسیومتر کنترل میشود. احتراق کامل و پاسخ خطی آشکارساز در محدوده mg 0.3-1 از نمونه حاصل میشود. به غیر از توزین نمونه و محاسبه نتایج از روی انتگرال تمام مراحل کار بهصورت اتوماتیک کنترل و انجام میشود.
معرفی شرکتهای سازنده تجهیزات C.H.N.O.S

منابـــع و مراجــــع