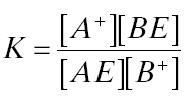جداسازی نانوذرات طلا با استفاده از کروماتوگرافی مایع با کارایی بالا

این مقاله شامل سرفصلهای زیر است:
2- انواع روشهای HPLC
2-2- کروماتوگرافی فاز معکوس (HPLC RP یا RPLC)
3-2- کروماتوگرافی تبادل یونی
4-2- کروماتوگرافی اندازه- طردی (SEC)
3- دستگاه HPLC
4- کاربرد HPLC در آنالیز نانوذرات طلا
1- مقدمه
HPLC یک فرآیند جذب سطحی پویا است. مولکولهای مورد تجزیه، زمانی که از میان دانههای متراکم متخلل حرکت میکنند، جذب سطحی میشوند. بسته به روش HPLC، انواع مختلفی از نیروهای جذب سطحی ممکن است در فرآیند بازداری موثر باشند. برهمکنشهای آبگریز (غیراختصاصی)، اصلیترین برهمکنشها در جداسازی فاز معکوس، برهمکنشهای دوقطبی-دوقطبی (قطبی)، اصلیترین برهمکنش در روش فاز نرمال و برهمکنشهای یونی نیز در کروماتوگرافی تبادل یونی، باعث بازداری ترکیبات میشوند. برهمکنشهای مذکور همگی در رقابت با هم عمل میکنند. مولکولهای مورد تجزیه با مولکولهای حلال شوینده، برای جذب سطحی روی مکانهای فعال فاز ساکن رقابت می کنند. بنابراین هر قدر مولکولهای مورد تجزیه، برهمکنش قویتری با سطح داشته باشند، برهمکنش شوینده ضعیف تر بوده و ماده مورد تجزیه زمان طولانیتری روی سطح فاز ساکن باقی میماند. کروماتوگرافی اندازه طردی، نوع دیگری از کروماتوگرافی است که جداسازی مخلوط به واسطه تفاوت اندازه مولکولها صورت میگیرد و بر پایه عدم وجود هرگونه برهمکنشهای تجزیهای خاص با فاز ثابت میباشد (هیچ نیرویی در این روش استفاده نمیشود). اصل اساسی جداسازی کروماتوگرافی اندازه طردی این است که مولکول بزرگتر، امکان کمتری برای نفوذ در فضای متخلخل جاذب دارد و بنابراین کمتر در ستون بازداری میشود.
2- انواع روشهای HPLC
1-2- کروماتوگرافی فاز نرمال
مواد پرکننده ستون رایج در کروماتوگرافی فاز نرمال، اکسیدهای متخلخلی مانند سیلیکا (SiO2) و یا آلومینا (Al2O3) هستند. سطح این فازهای ثابت با جمعیت انبوهی از گروههایOH که این سطوح را در حالت قطبیت بالایی نگه میدارند، پوشیده شدهاست. بازداری آنالیت روی این سطوح به تغییرات ترکیب فاز متحرک بسیار حساس است. فازهای ثابت اصلاح شده یا تغییر یافته از لحاظ شیمیایی هم میتوانند در کروماتوگرافی فاز نرمال استفاده شوند. سیلیکای تغییر یافته با تریمتوکسی گلایسیدوکسی پروپیل سیلان (نام رایج: دیول-فاز) جزو مواد پرکنندة رایج است که قطبیت سطح در آن کاهش یافته است. چگالی سطح گروههای OH روی فاز دیول، در محدوده اندازه m2/molµ 4-3 است. در حالی که روی سیلانولهای سیلیکای بدون پوشش، چگالی سطح در اندازه m2/molµ8 است. استفاده از فاز ساکن از نوع دیول و ترکیباتی با قطبیت پایین به عنوان اصلاح کننده شوینده (استرها مانند اتیل استات به جای الکلها) باعث جداسازی بهتر و تکرارپذیرتر در مقایسه با سیلیکای بدون پوشش میشود.
قدرت جذب سطحی ترکیبات شیمیایی در کروماتوگرافی فاز نرمال به ترتیب زیر افزایش مییابد:
هیدروکربنهای سیر شده، اولفینها، آروماتیکها، سولفیدها، اترها، ترکیبات نیترو، استرها-آلدهیدها- کتونها، الکلها، آمیدها، اسیدهای کربوکسیلیک.
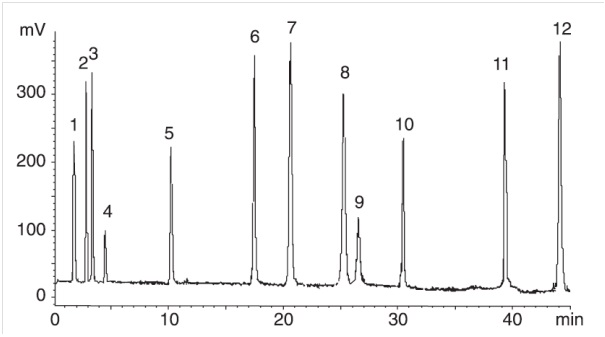
انتخاب استفاده از کروماتوگرافی فاز نرمال به عنوان روش کروماتوگرافی منتخب معمولا به حلالیت نمونه در فازهای متحرک خاص بستگی دارد. از آنجایی که رایج است در روش فاز نرمال از حلالهای غیرقطبی استفاده شود، این روش برای ترکیبات آبگریز (ترکیباتی که برهمکنشهای قویتری در کروماتوگرافی فاز معکوس از خود نشان میدهند) و در حلالهای قطبی یا آبی حل نمیشوند کاربرد دارد. شکل (1) کاربرد کروماتوگرافی فاز نرمال را برای جداسازی مخلوطی از چربیهای مختلف نشان میدهد.
شکل 1- جداسازی نمونههای انتخابی از دستههای چربی مختلف: 1- پارافین، 2- n-هگزادسیل پالمیتات، 3- کلسترول پالمیتات، 4- استئاریک اسید متیل استر، 5- گلیسرول تریپالمیتات، 6- هگزادسیل الکل، 7- استئاریک اسید، 8- کلسترول، 9- گلیسرول-1و3-دیپالمیتات، 10- گلیسرول-1و2-دیپالمیتات، 11- گلیسرول مونوپالمیتات، 12- اروسیل آمید. ستون مورد استفاده Liکروسفر® دیول(125×3میلی متر) قطرذرات پر کننده ستون mμ-5. حلال شوینده به صورت گرادیانی است که از 100% ازایزواکتان شروع شده و به تدریج درصد متیل تری ترسیوبوتیل اتر( MTBE) افزایش می یابد تا درصد آن طی 34 دقیقه به 60% برسد و سپس 10 دقیقه در این درصد به صورت ایزوکراتیک نگهداری می شود.
2-2- کروماتوگرافی فاز معکوس (HPLCRP یا RPLC)
کروماتوگرافی فاز معکوس تا به امروز متداولترین روش کروماتوگرافی است و تقریبا 90 درصد تمام تجزیههای نمونههایی با وزن مولکولی پایین، با استفاده از کروماتوگرافی فاز معکوس انجام میشود. یکی از عوامل اصلی شهرت و کاربرد زیاد این روش، توانایی تمایز ترکیبات بسیار مشابه و سهولت تغییر بازداری و گزینشپذیری در آن است. دلیل وجود این مزایا این است که نیروهای پراکندگی که در این نوع جداسازی استفاده میشوند، از ضعیفترین نیروهای بین مولکولی هستند. این انرژی پایین، تشخیص تفاوتهای بسیار کوچک برهمکنشهای مولکولی آنالیتهای بسیار مشابه را ممکن میکند.
مواد جاذب سطحی که در این نوع کروماتوگرافی استفاده میشوند، مواد جامد متخلخل با سطحی آبگریز هستند. بیشتر مواد پرکننده ستون که در کروماتوگرافی فاز معکوس استفاده میشوند، سیلیکاهای متخلخل اصلاح شده شیمیایی هستند. خواص سیلیکا طی سالهای زیادی مورد مطالعه قرار گرفته است و فناوری ساخت ذرات متخلخل کروی با اندازه و تخلخل مشخص، به خوبی توسعه یافته است. با وجود تحقیقات گسترده و رشد فراوان انواع ستون و مواد پرکننده قابل دسترس از لحاظ تجاری، هنوز در مورد خصوصیات بهینه برای فاز ساکن در این نوع کروماتوگرافی برای تجزیة دستههای متنوع ترکیبات(مانند دارویی، زنجیرههای آلکیلی خطی، حلقههای آروماتیک و هتروسیکلها)، نظر جامعی وجود ندارد.
3-2- کروماتوگرافی تبادل یونی
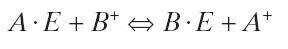
ثابت تعادل برای این فرایند در معادله زیر نشان داده شدهاست:
چهار نوع اصلی مراکز تبادل یون که معمولا به کار گرفته میشود عبارتند از:
– 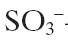
– 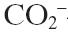
– آمین نوع چهارم: مبادلهکننده آنیون قوی؛
– آمین نوع سوم: مبادلهکننده آنیون ضعیف.
نگهداری آنالیت و گزینشپذیری در کروماتوگرافی تبادل یون بستگی زیادی به pH و قدرت یونی فاز متحرک دارد.
4-2- کروماتوگرافی اندازه- طردی (SEC)
این تنها روش جداسازی کروماتوگرافی است که در آن باید از هرگونه برهمکنش مثبت آنالیت با فاز ساکن اجتناب شود. در کروماتوگرافی اندازه- طردی هرچه وزن مولکولی آنالیت بالاتر باشد، شعاع هیدرودینامیکی آن بزرگتر است و در نتیجه سریعتر از ستون عبور میکند. در عین حال، اگر یک مولکول آنالیت با فاز ساکن برهمکنش نماید (که نامطلوب است)، بازداری مولکولهای بزرگتر افزایش مییابد و ممکن است جداسازی مولکولها منحصرا بر اساس شعاع هیدرودینامیک را مغشوش کند . به همین علت انتخاب مواد پر کننده ستون و فاز متحرک باید با دقت انجام شود به نحوی که مولکولهای فاز متحرک با سطح فاز ساکن، قویتر از پلیمر برهمکنش نمایند که در نتیجه از برهمکنش پلیمر با سطح جلوگیری میشود.
تعیین وزن مولکولی پلیمر بر اساس رابطه بین شعاع هیدرودینامیکی مولکول و وزن مولکولی است. شعاع تقریبا با ریشه سوم وزن مولکولی متناسب است. بنابراین ریشه سوم وزن مولکولی با میزان بازداری آنالیت متناسب است. این رابطه فقط در ناحیه کامل مولکولهای پلیمر از فضای متخلخل فاز ساکن صحیح است.
3- دستگاه HPLC
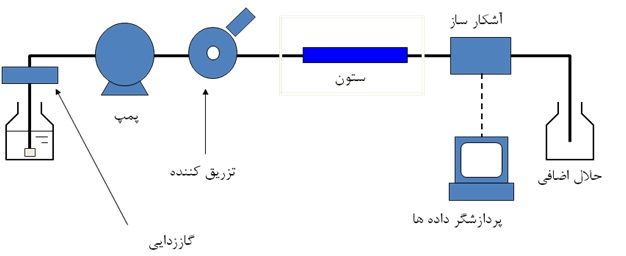
4- کاربرد HPLC در آنالیز نانوذرات طلا
روشهای کروماتوگرافی مایع که به طور معمول برای جداسازی مولکولها و پلیمرها بر اساس اندازه و خواص شیمیایی آنها به کار میرفتند، امروزه برای آنالیز توزیع اندازه ذرات نانوذرات طلااستفاده میشوند [1]. علاوه بر این، میانگین اندازه و خواص نوری نانوذرات طلا را میتوان با استفاده از یک تک نمونه که حجمی در حد چند میکرولیتر دارد در طی زمان کوتاهی به دست آورد [2 و 3]. این روشها را میتوان بر اساس شیوه عمل آنها طبقهبندی کرد که به عنوان مثال کروماتوگرافی اندازه طردی [11-4]، کروماتوگرافی مایع با عملکرد بالا [14-12] و کروماتوگرافی تبادل یونی [15] جزو این دسته از روشها هستند.
از آنجا که طیف نوری وابسته به اندازه نانوذرات را میتوان به آسانی به وسیله سیستمهای کروماتوگرافی و آشکارسازهای دیودی آرایهای ثبت نمود، از کروماتوگرافی اندازه طردی در تلفیق با TEM برای تعیین اندازه ذرات طلا در محدوده 3 تا 20 نانومتر استفاده شدهاست [16]. از این روش تلفیقی همچنین برای آنالیز دیگر ذرات کلوئیدی مانند سیلیکا [17] و نیمههادیها [21-18] استفاده شدهاست. کروماتوگرافی اندازه طردی همچنین این توانمندی را نیز دارد که از طریق گردآوری بخشهای جداسازی شده از یک مخلوط پلیدیسپرس، فرمهای مونودیسپرس ایجاد نماید [22]. چنین گزارشهایی موید این مطلب است که روشهای کروماتوگرافی قادر به جداسازی نانوذرات مختلفی است.
جداسازی با روش اندازه طردی مستلزم انتخاب فاز ساکن با اندازه تخلخل مناسب و علاوه بر آن، انتخاب فاز متحرک مناسب است. با این وجود، جذب سطحی برگشتناپذیر نانوذرات روی فاز ساکن از مشکلات استفاده از روشهای کروماتوگرافی برای جداسازی است و مساحت سطح بالای فاز ساکن و فعالیت سطحی بالای نانوذرات، مشکل برگشت ناپذیری جذب سطحی را دو چندان میسازد.
الکتروفورز مویینه میتواند این مشکل را با کاهش اثر سطح در سیستم جداسازی کاهش دهد [23]. اما در این صورت جداسازی نمونه برای به دست آوردن ذرات مونودیسپرس یکی از چالشهای عمده است. برای حل این مشکل در کروماتوگرافی اندازه طردی میتوان به فاز متحرک، سورفکتانت اضافه نمود. سورفکتانت به فاز ساکن متصل میشود و بر رفتار بازداری آنالیت اثر میگذارد. از سورفکتانتها برای کنترل اندازه نانوذرات استفاده میشود اتصال سورفکتانت به نانوذرات، آنها را از طریق اثرهای فضایی و یا الکتروستاتیکی پایدار میسازد و از تجمع آنها جلوگیری میکند.
به تازگی جداسازی و آنالیز نانوذرات طلای نامحلول (مانند نانوذرات طلای پوشیده شده با آلکانتیولاتها) با استفاده از کروماتوگرافی فاز معکوس و در تلفیق آن با آشکارساز آرایهای دیودی برای تعیین مونودیسپرس بودن نسبی نانوذرات طلابا اندازه کمتر از nm2، انجام شدهاست [28- 24]. همچنین از آشکارساز ولتامتری متناوب برای آشکارسازی نانوذرات کوچک (با قطر هسته کمتر از 2 نانومتر) که از طریق HPLC فاز معکوس جداسازی شده بودند، استفاده شد.
السومالی گزارش نمود که یک ستون مایکروژل هیدروفوب متخلخل که با سیستم کروماتوگرافی اندازه طردی قابل بازیافت کار میکند، آنالیز با میزان تفکیک بالایی برای نانوذرات طلای پایدار شده با آلکان تیولات با اندازه کوچک تر از nm3 به دست می دهد[29].
روشهای جداسازی برای آنالیز نانوذرات طلای محلول در آب (به عنوان مثال نانوذرات طلای پایدار شده با سیترات) نیز شایان اهمیت هستند و علت اهمیت آنها، کاربردهای بیوتجزیهای و دارویی آنهاست. افزودن سورفکتانت (به عنوان مثال سدیم دو دسیل سولفات) به فاز متحرک از جذب سطحی نانوذرات طلا روی ستون و تجمع آنها جلوگیری میکند و باعث تسهیل در جداسازی بر اساس اندازه ذره میشود[10].
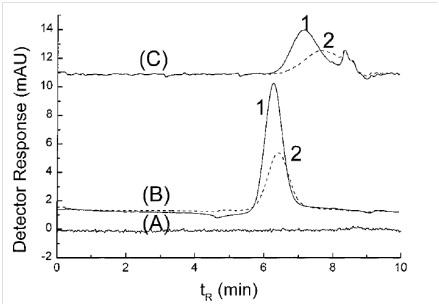
برای نخستین بار، روش کروماتوگرافی اندازه طردی برای جداسازی اشکال مختلف کروی و میلهای نانوذرات طلا به وسیله وی و همکارانش به کار گرفته شد[30.] از جمله مشکلات روش SEC برای جداسازی نانوذرات، جذب سطحی برگشتناپذیر آنها به وسیله مواد پرکننده ستون است. ترکیبات متنوعی از فاز متحرک برای جداسازی نانوذرات طلا به منظور بررسی مشکل جذب سطحی استفاده شدند. کروماتوگرامهای شکل (3) اثر فازهای متحرک مختلف را نشان میدهند. زمانی که از آب به عنوان تنها شوینده استفاده میشود هیچ پیکی مشاهده نمیشود و جذب سطحی بسیار شدید است (نمودار A در شكل 3). با افزودن SDS به عنوان شوینده، هر دو پیام مربوط به اشکال مختلف ذرات طلا، در یک محدوده مشاهده میشود (نمودار B در شكل 3). با استفاده از مخلوط سورفکتانتها (SDS و Brij-35) همان طور که در نمودار C شکل 3 نشان داده شدهاست، جداسازی نانوذرات کروی و میلهای را میتوان انجام داد.
آرایش مولکولهای کافی از SDS در حول نانوذرات طلا که به وسیله سورفکتانتهای کاتیونی پایدار میشوند و مانند ذرات باردار مثبت عمل میکنند [34] باعث میشود بار ذرات به منفی تغییر کند. دادهها حاکی از آن است که نانوذرات طلا در غلظت بالای SDS غلیظ، مانند گونههایی با بار منفی عمل میكند و میتوان انتظار داشت که هم مواد پر کننده ستون و هم نانوذرات طلا، با SDS برهمکنش کرده و بار منفی روی سطح آنها پدید آید. دافعه به وجود آمده میان ذرات و ماده پرکننده ستون باعث جلوگیری از جذب سطحی نانوذرات روی فاز ساکن پرکننده ستون میشود.
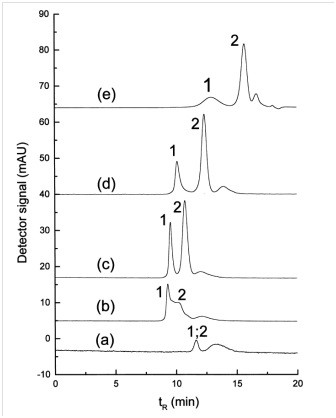
در بررسی دیگری توسط وی و لییو از سورفکتانت برای جداسازی اندازههای مختلف نانوذرات طلا استفاده شد. رفتار بازداری و کارایی جداسازی در کروماتوگرافی اندازه طردی برای نشان دادن مزیت سورفکتانت یونی در فاز متحرک در تحقیق مذکور مورد بحث قرار گرفته است[35]. همانگونه که پیشتر نیز اشاره شد، نوع ستون مورد استفاده در SEC بسیار مهم است و به علت جذب نانوذرات روی آن، محدودیتهای خاصی دارد. به عنوان مثال از ستونهای Nucleosil (500,1000) برای جداسازی نانوذرات طلا استفاده شدهاست. در تحقیق مذکور سیترات نه تنها به عنوان شوینده بلکه به عنوان پایدارکننده هم مورد استفاده قرار گرفته است. استفاده از ستون Nucleogel به همراه سیترات به عنوان شوینده باعث جذب سطحی شدید گردید. شایان ذکر است که Nucleosil یک ماده پرکننده بر پایه سیلیکا است و Nucleogel یک پلیمر (پلی استایرن – دی وینیل بنزن) است و شرایطی که برای Nucleosil استفاده میشود، برای Nucleogel مناسب نیست حتی اگر اندازه تخلخل یکسانی داشته باشند و این به علت مشکل جذب سطحی نانوذرات روی بستر است. غلظتهای مختلف محلول SDS به عنوان فاز متحرک برای کاهش اثر جذب سطحی استفاده شد. تأثیر غلظتهای مختلف از محلول SDS به عنوان فاز متحرک را میتوان در شکل (4) مشاهده نمود. دادهها نشان دهنده آن است که بدون حضور SDS پیامهای کوچک دیده میشود و هیچگونه جداسازی انجام نمیگیرد. اندازه پیام به دست آمده و تفکیک در جداسازی با افزایش غلظت SDS افزایش مییابد.
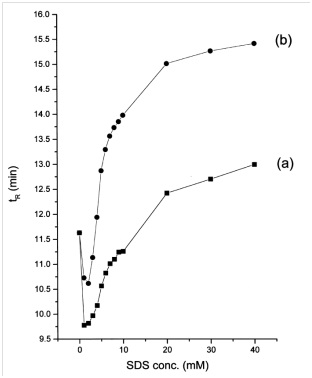
طیف جذب در شکل (6) نشان داده شدهاست و آشکار است که حضور SDS باعث افزایش جذب میشود و این موید آن است که افزودن SDS به نمونه باعث کاهش جذب سطحی نانوذرات به وسیله فاز ساکن شدهاست. بهبود پیام به دست آمده به برهمکنش سورفکتانت و مواد پرکننده ستون نسبت داده میشود که باعث ایجاد بار منفی روی سطح فاز ساکن و جلوگیری از جذب ذرات طلا روی آن میشود. همچنین تئوری کروماتوگرافی اندازه طردی بر این اساس است که ذرات طلای بزرگتر سریعتر از ستون عبور میكنند و حجم بازداری کمتری دارند. کاهش زمان شستشو با افزایش غلظت SDS (شکل 3) باعث ایجاد این فرضیه میشود که SDS اندازه ذره را افزایش داده و در نتیجه زمان شستشو کاهش را كاهش میدهد.

گزارشهای مذکور، پتانسیل SEC برای جداسازی اشکال و اندازههای مختلف نانوذرات طلا را نشان میدهد. مشکل جذب سطحی برگشتناپذیر نانوذرات طلا روی مواد پرکننده ستون را میتوان با افزودن سورفکتانتهایی به حلال شوینده (به عنوان مثال SDS) حل نمود. در این زمینه، برای افزایش کارایی جداسازی فاکتور جذب سطحی را هم باید به فاکتور فضایی که در SEC دخیل است اضافه نمود. با این وجود برای نانوذراتی با اشکال مختلف نمیتوان خط پایه مناسبی به دست آورد ولیکن سیستم آشکارساز آرایههای دیودیرا میتوان برای تفسیر شکل نانوذرات مورد استفاده قرار داد. تلفیق DAD و SEC از لحاظ مطالعه خواص اسپکتروسکوپی نانوذرات، بر TEM ارجحیت دارد. اما همچنان به مطالعات بیشتری برای تعیین مکانیسم برهمکنش سورفکتانت و نانوذرات طلا نیاز است.