بررسی عوامل موثر در پخش شدن مناسب نمونهها برای تصویربرداری با TEM

یکی از دغدغههای پژوهشگران در عرصه فناوری نانو، بررسی صحیح نمونهها است که به دلیل کوچکی مقیاس ممکن است با دشواریهایی همراه باشد. یکی از این مشکلات تجمع نانوساختارها یا کلوخه شدن آنها است. به دلیل وجود نیروی جاذبه واندروالس میان نانوساختارها، این مواد میتوانند به سمت هم جذب شده، به هم بچسبند. در چنین شرایطی، تعیین مشخصات نانوساختارها دچار خطا میشود. همچنین با تجمع ذرات، نسبت سطح به حجم در نانوساختارها کاهش مییابد که موجب تنزل برخی رفتارهای نانوساختارها میشود. برای نمونه، مقدار فعالیت کاتالیستی نانوذرات در اثر کلوخه شدن به شدت کاهش مییابد. اهمیت بررسی کلوخه شدن نانوساختارها به قدری است که آژانس حفاظت از محیط زیست آمریکا با اعطای بودجهای 375 هزار دلاری، پروژهای را برای بررسی تاثیر کلوخه شدن روی سمیت نانوذرات تصویب کرد. این پروژه در سال 2008 به پایان رسید و نتایج آن در دسترس عموم قرار گرفت[1]. از این رو تحقیق پیرامون این مسئله امری اجتناب ناپذیر و در برخی موارد حیاتی است.این مقاله شامل سرفصلهای زیر است:
1- مقدمه
2- اولتراسونیک
3- سورفاکتانت
4- pH محلول و دیسپرسانت
5-دما
6- تعیین مقدار بهینه سورفاکتانت
7- شبکه آزمایشگاهی فناوری راهبردی
8-نتیجه گیری
1- مقدمه
- قسمت درونی: شامل یونهایی است که به صورت قوی با سطح خارجی غشا اتصال پیدا کرده است؛
- قسمت بیرونی: یا ناحیه پراکنده که یونها در آن قسمت در حالت تعادل یونی به سر میبرند.
اما چگونه پتانسیل زتا روی کلوخه شدن ذرات تاثیر میگذارد ؟ کاهش پتانسیل زتا موجب کاهش اختلاف پتانسیل بین فاز پخش شده و محیط اطراف آن -که عامل اصلی دافعه بین نانوذرات است- میشود. در چنین شرایطی نیروی واندروالسی قدرت عمل پیدا کرده، میتواند موجب چسبیدن نانوذرات به یک دیگر شود. از این پدیده در تصفیهخانهها برای زدودن ذرات کلوئیدی استفاده میشود. در آنجا، مواد منعقد کننده مانند سولفات آلومینیوم یا آلومینات سدیم به آب اضافه میکنند که این باعث لخته شدن و انتقال ذرات معلق در آب میشود.
سوالی که در اینجا مطرح میشود این است که چگونه میتوان نانوساختارهای کلوخه شده را از هم جدا کرد؟ عوامل متعددی در جدا شدن نانوساختارها موثر است که از آن جمله میتوان به اولتراسونیک کردن، افزودن دیسپرسانت مناسب، تغییر pH، تغییر قدرت یونی محلول و تغییر دما اشاره کرد.
2- اولتراسونیک
3- سورفاکتانت
یکی از عوامل موثر در تغییر پتانسیل زتا، سورفاکتانتها هستند. این ترکیبات معمولا به دو دسته یون و غیریونی تقسیم میشوند. گاهی از یونهای ساده معدنی مانند یون پلی متافسفات و گاهی از پلیمرهای آلی که دارای گروههای باردار در زنجیره پلیمری هستند، برای پخش کردن ذرات استفاده میشود. هر دو دسته روی سطح نانوذرات جذب میشوند و موجب باردار شدن (معمولا بار منفی) آنها میگردند. با این عمل، ذرات یکدیگر را دفع میکنند و مانع از کلوخه شدن میگردد.

سیس و همکارانش [3] به بررسی تاثیر دو سورفاکتانت آنیونی و غیر یونی روی پتانسیل زتا و میزان پخش شدن پودر کربن سیاه پرداختند. نتایج کار آنها نشان داد که سورفاکتانت آنیونی اولئات سدیم و سورفاکتانت غیریونی نونیلفنول اتیوسیلات میتوانند مقدار پتانسیل زتا را تغییر دهند. البته سورفاکتانت غیریونی در محدوده pH 3 تا 11، مقدار پتانسیل زتا را کاهش میدهد، درحالی که اولئات سدیم در pHهای 3 تا 8/7، پتانسیل منفی را افزایش میدهد. دلیل آن تفاوت بین ساختار مولکولی این سورفاکتانتها است. سورفاکتانت غیریونی با استفاده از نیروی فضایی و سورفاکتانت آنیونی با استفاده از نیروی الکترواستاتیک موجب پایدار شدن و پخش شدن بهتر کربن سیاه میشود. نتایج کار این گروه تحقیقاتی نشان داد که سورفاکتانت غیریونی نسبت به همتای آنیونی خود، موجب پخش شدن بهتر نمونه در محیط آبی میشود. برای به دست آوردن ذرات ریزتر، استفاده از نونیلفنول اتیوسیلات توصیه شدهاست. این گروه دریافت که اگر برای پخش کردن کربن سیاه از اولئات سدیم استفاده شود، باید در کنار آن، نونیلفنول اتیوسیلات نیز به کار رود تا ذرات کوچکتر و پایداری به دست آید.

ژینگزنیگ گئو و همکارانش [4] به بررسی پخش کردن نانوپودر TiN در محیط آبی پرداختند. این موضوع یکی از چالشهای پژوهشگران در ساخت سیمانهای مبتنی بر Ti(C,N) است. ذرات TiN دارای ویژگیهای بسیار جالبی نظیر سختی بالا، پایداری شیمیایی، هدایت الکتریکی و ضریب اصطکاک پایین است. در دهه 70 میلادی، از این ماده در سیمان استفاده شد و امروزه نیز از آنها در سیمانهای مبتنی بر Ti(C,N) استفاده میشود. نتایج تحقیقات نشان میدهد که در صورت استفاده از نانوذرات TiN، خواص سیمان متاثر از میزان پخش شدن نانوذرات در سیمان است. ذرات کوچک تر از یک میکرومتر TiN، به دلیل نیروی جاذبه واندروالس به هم چسبیده و موجب تجمع و آگلومره شدن آنها میشود. بنابراین چگونگی جدا کردن این نانوذرات در فرآیند تولید سیمانهای مبتنی بر Ti(C,N) به صورت چالشی باقی مانده است.
پیش از این، ژانگ و همکارانش [5] نشان دادند که برای تولید ذرات TiN به ابعاد 2/30 میکرومتر باید از دیسپرسانت PEI درpH 9/5 استفاده کرد. برای پایداری این ذرات از ترکیبات مختلفی مانند نمک آمونیومی پلی متاآکریلیک اسید در pHهای مختلف استفاده شد. پتانسیل زتا نشان داد که نقطه ایزوالکتریک ذرهای شدن TiN در pH 4 است و دفع استریک PMAA-NH4 در محدوده اسیدی دارای یک سهم مثبت نسبت به دیسپرسانت است. بنابراین چنین نتیجهگیری شد که کیفیت پخش شدن پودرهای سرامیکی، رابطة نزدیکی با چگونگی جذب سورفاکتانت روی سطح پودر دارد. در تحقیق دیگری، نانوپودر TiN با میکروپودر TiN درون هاون ریخته و 5 دقیقه ساییده میشود. سپس درون پروپانول ریخته و با اولتراسونیک هم زده میشود. در ادامه دوباره به درون هاون ریخته و 3 دقیقه دیگر ساییده میشود. با این کار تجمع ذرات به حداقل مقدار خود میرسد.
در این پروژه، محققان نانوپودر TiN را در محیط آبی با اولتراسونیک به هم زدند و سپس Tween80 به عنوان سورفاکتانت به آن اضافه کردند. بیشتر تمرکز این پروژه روی تأثیر زمان اولتراسونیک و افزودن Tween80 به محلول حاوی نانوذرات TiN است. همانطور که در بخش قبل عنوان شد، زمان اولتراسونیک در پخش شدن نمونهها تاثیر زیادی دارد اما همیشه افزایش زمان موجب بهبود پخش شدن نمیگردد. هدف اصلی از انجام این پروژه بررسی پخش شدن نانوذرات TiN در محیط آبی و ارتباط آن با شیمی سطح ذرات است. این مقاله در ادامه کار تحقیقاتی اخیر این گروه روی سیمانهای حاوی ذرات بسیار کوچک Ti(C,N) انجام شدهاست. نانوذرات TiN از شرکت Hefei Kaier با میانگین ابعاد 20 نانومتر تهیه شد. توزیع اندازه ذرات آن نیز با دستگاه DLS ساخت انجام شد. از TEM نیز برای تصویربرداری استفاده شد. ترکیبات لایههای موجود در سطح ذرات نیز با کمک XRD مورد بررسی قرار گرفت. برای بررسی جذب گروههای عاملی سورفاکتانت Tween80 به سطح ذرات، از طیفسنجی FTIR استفاده شد.
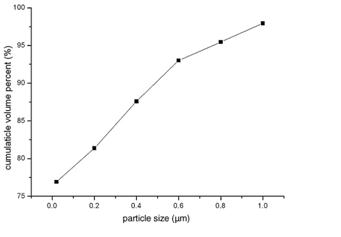
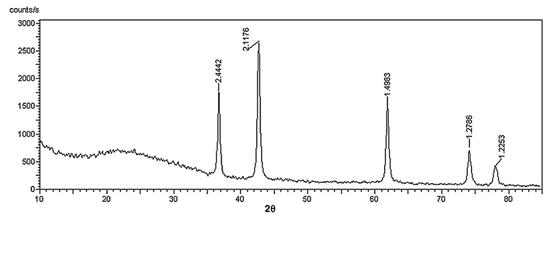
شکل (2) نانوپودر TiN اولیه را نشان میدهد که از طریق واکنش فاز گازی آمادهسازی شدهاست. ذرات به شکل تقریبا کروی هستند که غالبا به هم چسبیده و متجمع شدهاند. قطر ذرات به هم چسبیده، تا چند صد نانومتر نیز میرسد. شکل (2) و (3)، نشان میدهند که توزیع اندازه ذرات، طیف بسیار محدودی دارند. شکل (4)، الگوی XRD را برای نانوپودر TiN نشان میدهد. پیکهای مربوط به صفحات بلوری (111)، (200)، (220)، (311) و (222) در این الگو دیده میشود اما هیچ اثری از ناخالصیهایی نظیر TiO2 و TiO در طیف دیده نمیشود. اما نتایج طیف سنجی XPS نشان داد که در سطح پودر مورد آزمایش، TiN و TiO2 وجود دارد.
اکنون نانوذرات خریداری شده که در بالا مورد آزمایش قرار گرفته است، در محلول آبی با غلظت 10 درصد وزنی ریخته میشود. معمولا در این شرایط، ذرات زیر 1 میکرومتر به دلیل جاذبه واندروالس به هم برخورد کرده، متجمع میشوند. بنابراین اولتراسونیک میتواند موجب شکستن این کلونیهای متجمع شده بشود. شکل (5) تصاویر TEM گرفته شده از سوسپانسیون TiN را در زمانهای مختلف اولتراسونیک شدن نشان میدهد. در مقایسه با شکل (2)، که مربوط به نانوذرات پیش از پخش شدن در آب است، در شکل (5-a)، پس از 10 دقیقه اولتراسونیک، ذرات آگلومره کمتری دیده میشود و بیشتر ذرات انفرادی هستند. زمانی که اولتراسونیک به محلول اعمال میشود، حبابهایی در مقیاس میکرو درون محلول ایجاد میشوند. وقتی قطر این حبابها به حد مشخصی رسید، میترکند و این ترکیدن منجر به افزایش فشار و دما در آن نقطه میگردد که به آن نقطه، نقطه داغ گفته میشود. شوک حاصل از ترکیدن موجب خرد شدن و از هم جدا شدن ذرات آگلومره شده که در نهایت باعث پخش شدن بهتر نانوذرات میگردد.

سورفاکتانتهای آلی اغلب در طول فرآیند پخش کردن مواد سرامیکی به منظور پخش شدن بهتر و پایداری محلول به آن اضافه میشوند. Tween80 یک نوع پلیمر غیریونی است و به عنوان سورفاکتانت موثر شناخته میشود. Tween80 در این پروژه با یک درصد حجمی استفاده میشود. طیف FTIR برای بررسی سازوکار جذب این سورفاکتانت روی نانوپودرهای TiN گرفته شد. پیکهای مربوط به C=C، C=O، C-O و OH نشان میدهد که Tween80 روی سطح نانوپودرها جذب شدهاند. تغییر محل برخی پیکها نیز این مطلب را تایید میکند.
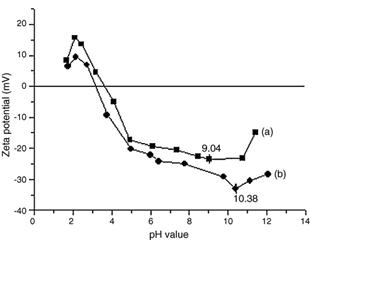
نمودار (6-a) مقادیر پتانسیل زتای محلول دارای TiN و بدون Tween80 را برحسب pH نشان میدهد. پتانسیل زتای پودر از روی یونهای H+ و OH– جذب شده روی سطح ذرات مشخص میشود. در pHهای بسیار اسیدی (کمتر از 2) و بسیار قلیایی (بیشتر از 11)، کاهش شدیدی در پتانسیل زتا دیده میشود که این را میتوان با تئوری DLVO توجیه کرد. در واقع در این شرایط، برای تثبیت pH، مقادیر زیادی اسیدکلریدریک یا سود سوزآور باید به محلول اضافه شود که قدرت یونی را در محلول افزایش میدهد و موجب کاهش ضخامت دولایه الکتریکی اطراف ذره میشود که در نهایت پتانسیل زتا کم میشود. نمودار (6-b) مقادیر پتانسیل زتای محلول حاوی TiN را برحسب pH در حضور Tween80 نشان میدهد. Tween 80 باعث تر شدن سطح پودر میشود. پودر TiN دارای بار منفی است و Tween80 میتواند با ایجاد پیوند هیدروژنی به این سطح بچسبد و یک لایه آلی اطراف آن ایجاد کند. این لایه مانع برهمکنش میان ذرات میشود. پتانسیل زتای بالا به معنای دانسیته بار سطحی بالا است که این امر منجر به تولید یک نیروی دافعه دولایه الکتریکی قوی میگردد.
به طور خلاصه نتایج این پروژه نشان داد که مقدار ذرات آگلومره شده در محلول آبی دارای TiN، پس از 10 دقیقه اولتراسونیک کاهش یافت و تعدادی ذرات منفرد نیز دیده شد. بعد از 30 دقیقه اولتراسونیک، صدها ذره به ابعاد 20 نانومتر رویت شد که نشاندهندة پخش شدن رضایتبخش این ذرات است. افزایش زمان اولتراسونیک تا یک ساعت، تاثیر محسوسی در یک نواخت شدن توزیع مواد نداشت. پلیمر غیریونی Tween80 به عنوان سورفاکتانت به محلول اضافه شد. طیف FTIR نشان داد که برهمکنشی میان Tween80 و پودر وجود دارد. از آنجایی که نانوپودر TiN به دلیل هیدورکسیلی شدن دیاکسید تیتانیوم، باردار است بنابراین دیسپرس شدن آن وابسته به رفتارهای الکتروفوریز این ماده دارد. روند تغییرات پتاسیل زتا در حضور و در نبودن Tween80 نيز بررسی شد. نتایج نشان داد که Tween80 موجب منفیتر شدن پتانسیل زتا میشود و در نهایت کاهش برهمکنش ذرات و منفرد شدن آنها را در پی دارد.
4- PH محلول و دیسپرسانت
جینگکن ژیانگ و همکارانش [8] دریافتند که عوامل مختلف با سازوکارهای متفاوت روی پخش شدن ذرات تاثیرگذار هستند. برای مثال تغییر نیروی یونی محلول با تاثیر بر ضخامت دولایه الکتریکی، میزان پخش شدن را تغییر میدهد. در حالی که pH با تغییر پتانسیل زتا این کار را انجام میدهد. با افزایش قدرت یونی یا نزدیک کردن pH به نقطه ایزوالکتریک نانوذرات، میتوان کلوخه شدن نانوذرات را افزایش داد و در نتیجه اندازة هیدرودینامیکی نمونه افزایش مییابد. این درحالی است که افزایش تعداد یونهای محاصره کننده نانوذرات میتواند موجب افزایش پایداری آنها و در نتیجه کاهش مقدار کلوخه شدن گردد.دما تاثیر دوگانهای بر چگونگی پخش شدن ذرات دارد. در برخی نمونهها افزایش دما موجب کلوخه شدنوافزایش اندازه ذرات و در بعضی موارد موجب کاهش اندازه کلونی ذرات میشود. وون یی و همکارانش [8] به بررسی تاثیر دما در میزان پخش شدن کربن سیاه در دیسپرسانت پلی ایزوبوتیلن سوسینایمید پرداختند. نتایج کار آنها نشان داد که افزایش دما موجب بیشتر شدن ذرات آگلومره شد. از آنجایی که ارتباط اندکی میان انرژی پیوندی میان ذرات و دما وجود دارد، محققان به بررسی ریشه این رفتار پرداختند. آنها دریافتند که دما بر دیسپرسانت تاثیر میگذارد و از این طریق موجب افزایش میزان کلوخه شدن میگردد. اما در تحقیقی که روی نانوذرات فلورید لیتیوم[9] انجام شد، نتیجه کاملا برعکس بود. افزایش دما موجب کاهش اندازه دانه شد. بنابراین برای اطلاع از تاثیر دما روی میزان کلوخه شدن ذرات باید سازوکار پخش شدن و برهمکنش دیسپرسانت با نمونه به دقت بررسی شود.
6- تعیین مقدار بهینه سورفاکتانت
در بخشهای پیشین به بررسی تاثیر عوامل مختلف بر چگونگی پخش شدن نانوساختار پرداخته شد. در این بخش روشهای تعیین مقدار بهینه سورفاکتانت بررسی میشود. سورفاکتانتها معمولا موجب تغییر پتانسیل زتا میشوند، بنابراین میتوان با استفاده از دستگاه اندازهگیری پتانسیل زتا مانند DLS، مقدار سورفاکتانت را به دست آورد. با این کار مقدار مناسب برای پخش شدن بهینه نانوذرات قابل استخراج است. اگر مقدار سورفاکتانت کم شود، ممکن است تاثیر مفیدی روی جداسازی نانوذرات نداشته باشد و اگر مقدار آن زیاد باشد، ممکن است کلوخه شدن ذرات را تشدید کند. علاوه بر این، به دلیل گران بودن سورفاکتانتها، استفاده بهینه از آن میتواند از نظر اقتصادی موجب کاهش هزینهها شود.
در روشهای قدیمی معمولا برای یافتن مقدار مناسب، ابتدا مقداری سورفاکتانت به نمونه اضافه میکردند و سپس پتانسیل زتای نمونه را اندازه میگرفتند. برای این کار باید غلظت نانوذرات بسیار کم باشد که برای دستیابی به این منظور، نمونه چندینبار رقیق میشد، اما همین موضوع گاهی موجب تغییر ناگهانی پتانسیل زتا میشد و روی نتیجه کار تاثیر منفی میگذاشت. برای حل این مشکل راهحلهای مختلفی نیز ارایه شدهاست.
یکی از بهترین روشهای جایگزین، استفاده از ZetaProbe و AcoustoSizer است که کاملا بینیاز از رقیقسازی است. در واقع میتوان بدون رقیقسازی، سورفاکتانت را به نمونه اضافه کرد و میزان تغییر پتانسیل زتا را به دست آورد. معمولا با افزایش سورفاکتانت، پتانسیل زتا افزایش یا کاهش مییابد تا جایی که در یک نقطه این روند تغییر میکند که همان نقطة مقدار بهینه است.
7- شبکه آزمایشگاهی فناوری راهبردی
| نام دستگاه |
| میکروسکوپ الکترونی عبوری |
8- نتیجهگیری
نوع و غلظت سورفاکتانت نیز میتواند دانشپژوهان را در جداسازی پودرهای آگلومره یاری کند. انتخاب سورفاکتانت مناسب با استفاده از مراجع قابل انجام است، اما تعیین مقدار بهینه سورفاکتانت تابع عوامل محیطی است که باید از طریق اندازهگیری پتانسیل زتا مشخص گردد. برای راحتی کار میتوان از دستگاههای ZetaProbe و AcoustoSizer استفاده کرد که مزیت آنها بینیازی به رقیقسازی است.






